Medisinsk ekspert av artikkelen
Nye publikasjoner
Ovarielt hyperstimuleringssyndrom
Sist anmeldt: 05.07.2025

Alt iLive-innhold blir gjennomgått med medisin eller faktisk kontrollert for å sikre så mye faktuell nøyaktighet som mulig.
Vi har strenge retningslinjer for innkjøp og kun kobling til anerkjente medieområder, akademiske forskningsinstitusjoner og, når det er mulig, medisinsk peer-evaluerte studier. Merk at tallene i parenteser ([1], [2], etc.) er klikkbare koblinger til disse studiene.
Hvis du føler at noe av innholdet vårt er unøyaktig, utdatert eller ellers tvilsomt, velg det og trykk Ctrl + Enter.
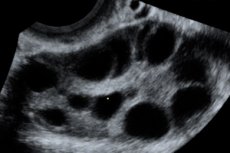
Ovarielt hyperstimuleringssyndrom (OHSS) er en iatrogen komplikasjon basert på eggstokkenes hyperergiske, ukontrollerte respons på administrering av gonadotropiner i eggløsningsstimuleringssykluser og assistert befruktningsteknologi.
Syndromet kan manifestere seg etter eggløsningsinduksjon med klomifen eller ved graviditetsstart i en spontan syklus.
 [ 1 ]
[ 1 ]
Epidemiologi
Forekomsten av ovarielt hyperstimuleringssyndrom varierer fra 0,5 til 14 % med ulike eggløsningsstimuleringsordninger og har ingen tendens til å avta. Sykdommen har varierende alvorlighetsgrad og kan være dødelig på grunn av utvikling av tromboemboliske komplikasjoner eller ARDS. Forventet dødelighet er 1 av 450–500 000 kvinner. Alvorlige former av syndromet, som krever sykehusinnleggelse på intensivavdelingen, forekommer hos 0,2–10 %. I følge det russiske nasjonale registeret over assistert befruktningsteknologi var forekomsten av alvorlig OHSS i 2004 5,6 %.
Årsaker til ovarielt hyperstimuleringssyndrom
Risikofaktorer for utvikling av ovarielt hyperstimuleringssyndrom:
- alder under 35 år,
- astenisk fysikk,
- tilstedeværelsen av polycystiske eller multifollikulære eggstokker,
- modning av mer enn ti follikler i eggløsningsstimuleringsprotokollen,
- bruk av gonadotropinfrigjørende hormonagonister og høye doser gonadotropiner,
- starten av svangerskapet,
- støtte til lutealfasen med hCG-preparater,
- allergiske sykdommer.
Hvordan utvikler ovarielt hyperstimuleringssyndrom seg?
Ovarielt hyperstimuleringssyndrom oppstår mot en bakgrunn av unormalt høy konsentrasjon av kjønnshormoner i blodplasmaet, noe som påvirker funksjonene til ulike kroppssystemer negativt, først og fremst eggstokkene, og er preget av en økning i eggstokkstørrelsen, noen ganger opptil 20-25 cm i diameter, med dannelse av follikulære og luteale cyster i dem mot en bakgrunn av uttalt stromalt ødem. Utløseren for utviklingen av syndromet er introduksjonen av en ovulatorisk dose koriongonadotropin. Utviklingen av syndromet er basert på fenomenet "økt vaskulær permeabilitet", som fører til en massiv frigjøring av proteinrik væske i det tredje rommet, interstitiet, og dens avsetning med utvikling av hypovolemi, hemokonsentrasjon, oliguri, hypoproteinemi, elektrolyttubalanse, økt aktivitet av leverenzymer, dannelse av ascites, hydrothorax, hydroperikard med eller uten hypovolemisk sjokk. Imidlertid er "faktor X" som forårsaker væsketransudasjon fortsatt ukjent. I alvorlige tilfeller forekommer anasarka, akutt nyresvikt, tromboemboliske komplikasjoner og ARDS.
For tiden vurderes ovarielt hyperstimuleringssyndrom (OHSS) fra et SIRS-perspektiv, der massiv skade på endotelet oppstår. Hos pasienter med OHSS ble det funnet høye konsentrasjoner av interleukiner (IL-1, IL-2, IL-6, IL-8) og tumornekrosefaktorer (TNF-α, TNF-(3)) i peritoneal transudat, som forsterker syntesen av prostaglandiner i eggstokkene, ovariell neovaskularisering og vaskulær permeabilitet. Under påvirkning av proinflammatoriske cytokiner skjer systemisk aktivering av koagulasjonsprosesser. Omfanget av leukocytose korrelerer med alvorlighetsgraden av SIRS. Organsystemisk skade ved OHSS ligner på skaden som oppstår ved sepsis. Rollen til den mikrobielle faktoren ved OHSS og dens bidrag til utviklingen av SIRS er for tiden under diskusjon. Det antas at mikroorganismer som koloniserer tarmene og urogenitaltraktene kan trenge utover deres habitat og ha en effekt på kroppen som ligner på den ved sepsis.
Symptomer på ovarielt hyperstimuleringssyndrom
Alvorlighetsgraden av syndromet er direkte relatert til alvorlighetsgraden av hemodynamiske forstyrrelser som forårsaker det kliniske bildet. Syndromets debut kan være gradvis med økende symptomer eller plutselig (akutt), der det oppstår en kraftig omfordeling av væske i kroppen i løpet av få timer med akkumulering i serøse hulrom. Når syndromet manifesterer seg, oppstår det klager over svakhet, svimmelhet, hodepine, flimrende "fluer" foran øynene, kortpustethet i hvile og under fysisk anstrengelse, tørrhoste som intensiveres i liggende stilling, tørr munn, kvalme, oppkast, diaré, oppblåsthet, en følelse av oppblåsthet, spenning, magesmerter ofte uten klar lokalisering, sjelden vannlating, feber, hevelse i de ytre kjønnsorganene og nedre ekstremiteter.
Hos pasienter med ovarielt hyperstimuleringssyndrom kan respirasjonssvikt utvikles på grunn av begrenset lungemobilitet på grunn av ascites, eggstokkforstørrelse eller pleuraeffusjon. Forløpet av alvorlig OHSS i manifestasjonsstadiet kan kompliseres av akutt hydrothorax, ARDS, lungeemboli, lungeemboli, atelektase og intraalveolær blødning. Pleuraeffusjon diagnostiseres hos omtrent 70 % av kvinner med moderat til alvorlig OHSS, og effusjonen kan være ensidig eller tosidig og oppstår mot bakgrunn av ascites. Ved OHSS er det beskrevet forskyvning og kompresjon av mediastinale organer på grunn av massiv høyresidig pleuraeffusjon med utvikling av sjokk, samt et dødelig utfall hos en kvinne med OHSS og hydrothorax på grunn av atelektase, massiv blødning i alveolumen.
Hemodynamiske forstyrrelser. Ved moderat og alvorlig OHSS forekommer arteriell hypotensjon og takykardi.
Ascites. Magen er utspilt, ofte spent, smertefull i alle områder, men oftere i hypogastrium i eggstokkenes projeksjon.
Nedsatt nyre- og leverfunksjon. Urinretensjon, oliguri, anuri og hepatomegali observeres.
Forløpet av OHSS hos 80 % av pasienter med en alvorlig form av syndromet er ledsaget av feber. Hos 20 % av kvinnene oppstår feber mot bakgrunn av en urinveisinfeksjon, hos 3,8 % - på grunn av lungebetennelse, hos 3,3 % - en øvre luftveisinfeksjon. Tromboflebitt på grunn av installasjon av et intravenøst kateter forårsaker feber hos 2 %, betennelse i det subkutane fettet på stedet for punktering av bukveggen under laparocentese - hos 1 % av pasientene. Infeksjon av operasjonssåret forekommer hos 1 %, og abscesser etter injeksjon (intramuskulær administrering av progesteron) hos 0,5 %. Feber av ikke-infeksiøs genese hos annenhver pasient med OHSS er sannsynligvis assosiert med endogene pyrogene mekanismer. Isolerte tilfeller av sepsis ved alvorlig OHSS er beskrevet.
Mot bakgrunnen av utviklingen av syndromet oppstår en forverring av latente kroniske somatiske sykdommer.
Hva plager deg?
Klassifikasjon
Det finnes ingen enkelt klassifisering av ovarielt hyperstimuleringssyndrom. Basert på kliniske og laboratoriesymptomer skilles det mellom fire alvorlighetsgrader av syndromet:
- Mild OHSS. Magesmerter, eggstokker opptil 8 cm i diameter med eller uten cyster, laboratorieparametre er normale. Mild OHSS kalles "kontrollert ovariell hyperstimulering", siden denne tilstanden observeres i absolutt alle sykluser med superovulasjonsstimulering og for tiden ikke regnes som et patologisk syndrom som krever behandling.
- Moderat OHSS. Moderate smerter i alle deler av magen, kvalme, oppkast, diaré, eggstokker 8–12 cm i diameter med cyster, ultralyd og/eller kliniske tegn på ascites, hematokritt overstiger ikke 45 %, leukocytose – 10–16 x 10 9 /l, hyperkoagulasjon (D-dimer – mer enn 0,5 μg/ml, fibrinogenkonsentrasjon – mer enn 400 mg/dl, APTT, INR – innenfor normale grenser).
- Alvorlig OHSS. Hematokritt over 45 %, leukocytose 17–24 x 10 9 /l, hyperkoagulasjon (D-dimer over 5 μg/ml, fibrinogen over 600 mg/dl), eggstokker over 12 cm i diameter med cyster, alle kliniske og laboratoriemessige tegn på moderat OHSS og spent ascites, hydrothorax, leverdysfunksjon, oliguri [diurese mindre enn 0,5 ml/(kg t)].
- Kritisk OHSS. Hematokrit over 55 %, leukocytose over 25 x 109/l, spent ascites, bilateral hydrothorax, hydroperikard, anasarka, forstørrede eggstokker opptil 20–25 cm, oliguri eller anuri, akutt nyresvikt, tromboemboliske komplikasjoner, ARDS.
Ovarielt hyperstimuleringssyndrom er også delt inn i tidlig og sent.
Hvis OHSS oppstår i lutealfasen og implantasjon ikke skjer, forsvinner syndromet plutselig og spontant med menstruasjonens begynnelse, og når sjelden en alvorlig form. Hvis implantasjon skjer, observeres oftest en forverring av pasientens tilstand i løpet av de første 12 ukene av svangerskapet. Sen OHSS er forårsaket av en betydelig økning i hCG i blodplasmaet og er vanligvis assosiert med implantasjon og tidlig graviditet.
Konsekvenser og komplikasjoner
Komplikasjoner ved ovarielt hyperstimuleringssyndrom kan fortsette med utviklingen av tromboemboliske komplikasjoner. Årsaken til trombose ved OHSS er fortsatt ukjent, men hovedrollen i patogenesen av denne tilstanden tilskrives høye konsentrasjoner av kjønnshormoner, proinflammatoriske cytokiner, hemokonsentrasjon og en reduksjon i venøs kretsløp (VCP). Lange sykehusinnleggelser, begrenset motorisk aktivitet, redusert venøs retur på grunn av en økning i eggstokkene, en økning i aktiviteten til koagulasjonsfaktorer, fibrinolysehemmere og blodplater bidrar ytterligere til den høye risikoen for å utvikle trombotiske komplikasjoner forbundet med OHSS. Det er vist at hos 84 % av pasientene med tromboemboliske komplikasjoner som oppsto etter eggløsningsinduksjon og i assistert reproduksjonsteknologi, skjedde utviklingen deres mot bakgrunn av graviditet. I 75 % av tilfellene ble trombedannelse observert i venesengen med en dominerende lokalisering i karene i øvre ekstremiteter, nakke og hode (60 %). En rekke pasienter ble diagnostisert med spontan arteriell trombose lokalisert i hjernekarene. Sjeldnere ble tromber observert i femoral-, popliteal-, carotis-, subclavia-, iliac-, ulnar-, mesenterialarteriene og aorta. Litteraturen presenterer en observasjon av utviklingen av okklusjon av den sentrale retinalarterien med synstap ved OHSS. Forekomsten av lungeemboli hos pasienter med OHSS og dyp venetrombose i underekstremiteter er 29 %, mens hos kvinner med OHSS og dyp venetrombose i øvre ekstremiteter og arteriell trombose er risikoen for denne komplikasjonen betydelig lavere og er henholdsvis 4 og 8 %.
Alvorlige tilfeller av ovarielt hyperstimuleringssyndrom kan være ledsaget av komplikasjoner som krever kirurgisk inngrep - ruptur av en ovariecyste og intraabdominal blødning, torsjon av livmorvedheng, ektopisk graviditet.
Diagnose av ovarielt hyperstimuleringssyndrom
Diagnosen ovarielt hyperstimuleringssyndrom stilles på grunnlag av anamnesedata, en omfattende klinisk, laboratorie- og instrumentell undersøkelse som avdekker forstørrede eggstokker med flere cyster, uttalt hemokonsentrasjon og hyperkoagulasjon hos en pasient som brukte assistert befruktning eller kontrollert eggløsningsinduksjon i denne syklusen for å oppnå graviditet.
Laboratorieforskning
Klinisk blodprøve
Hematokrit over 40 %, hemoglobinkonsentrasjon over 140 g/l, leukocytose opptil 50 x 10 9 /l uten venstreforskyvning, trombocytose opptil 500–600 x 10 6 /l. Hemokonsentrasjon (hematokrit over 55 %) indikerer en potensiell livstruende tilstand.
Biokjemisk blodprøve
Elektrolyttubalanse, inkludert hyperkalemi (mer enn 5,3 mmol/l) og hyponatremi (mer enn 135 mmol/l), som fører til redusert plasmaosmolaritet. Hypoproteinemi (totalt protein mer enn 66 g/l), hypoalbuminemi (albumin mindre enn 35 g/l), høyt C-reaktivt protein, økte levertransaminaser opptil 800 U/l, i noen tilfeller økt GGT eller alkalisk fosfatase, hos noen pasienter - økt kreatininkonsentrasjon mer enn 80 μmol/l og urea mer enn 8,3 mmol/l.
 [ 20 ], [ 21 ], [ 22 ], [ 23 ]
[ 20 ], [ 21 ], [ 22 ], [ 23 ]
Koagulogram
Økte fibrinogennivåer over 400 mg/dl, von Willebrand-faktor over 140 %, reduserte antitrombin III-konsentrasjoner under 80 %, D-dimer over 0,5 mcg/ml. Normale verdier for APTT, PTI, INR.
 [ 24 ]
[ 24 ]
Blodimmunoglobuliner
Redusert konsentrasjon av IgG og IgA i blodplasma. Generell urinanalyse. Proteinuri.
Analyse av sammensetningen av ascitesvæske
Høyt proteininnhold (mer enn 42 g/l) og albumin (mer enn 23 g/l), lavt antall hvite blodlegemer, relativt høyt antall røde blodlegemer, høye konsentrasjoner av alle proinflammatoriske cytokiner, C-reaktivt protein opptil 135 mg/l (normalt 0–8,2 mg/l), globulinfraksjon av proteiner.
 [ 25 ], [ 26 ], [ 27 ], [ 28 ], [ 29 ], [ 30 ], [ 31 ]
[ 25 ], [ 26 ], [ 27 ], [ 28 ], [ 29 ], [ 30 ], [ 31 ]
Tumormarkører i blodplasma
Konsentrasjonen av CA-125, som reflekterer massiv proliferasjon av eggstokkvev, når sine maksimale verdier (opptil 5125 U/ml) innen den andre uken med OHSS-utvikling, når begge eggstokkene er mest forstørrede. Det forhøyede nivået av tumormarkøren vedvarer i opptil 15–23 uker etter tegn på ovarielt hyperstimuleringssyndrom, til tross for behandling.
Procalcitonin i blodserum bestemmes hos 50 % av pasientene i området 0,5–2,0 ng/ml, noe som regnes som en moderat systemisk inflammatorisk reaksjon.
Mikrobiologisk forskning
Ved undersøkelse av urin som skilles ut fra skjeden og livmorhalskanalen, isoleres atypiske patogener Pseudomonas, Proteus, Klebsiella, Enterobacter, E. coli i mengder på mer enn 10 000 CFU/ml.
Instrumentell forskning
Ultralyd av bekkenorganene
Forstørrede eggstokker fra 6 til 25 cm i diameter med flere cyster, normal eller forstørret livmor, tilstedeværelse av fritt væske i bekkenhulen og normal progressiv enkelt- eller flerlingesvangerskap.
Ultralyd av mageorganer
Tilstedeværelse av fri væske i bukhulen i en mengde på 1 til 5-6 liter. Normal størrelse og struktur på leveren eller hepatomegali. Ekkotegn på biliær dyskinesi. Ved undersøkelse av nyrene er calyceal-bekkenkomplekset uendret.
Ultralyd av pleurahulene
Tilstedeværelse av fri væske i ekkokardialhulen. Mot bakgrunn av hemodynamiske forstyrrelser, redusert EF, redusert endediastolisk volum, redusert venøs retur, i noen tilfeller - tilstedeværelse av fri væske i perikardhulen.
EKG
Rytmeforstyrrelser som ventrikulær ekstrasystoli, takykardi, diffuse metabolske og elektrolyttforandringer i myokardiet. Røntgen av thorax. Utføres ved mistanke om ARDS og tromboembolisme. Et karakteristisk røntgenfunn ved ARDS er tilsynekomsten av et "matglassmønster" og diffuse multifokale infiltrater med ganske høy tetthet (konsolidering) med veldefinerte luftbronkier, dvs. utvikling av omfattende skade på lungeparenkymet. Ved lungeemboli avslører røntgenbildet en høy posisjon av diafragmakuppelen, diskoid atelektase, overflod av en av lungerøttene eller en "avskåret" rot, utarming av lungemønsteret over det iskemiske området i lungen, og en perifer trekantet betennelsesskygge.
Indikasjoner for konsultasjon med andre spesialister
På grunn av involvering av alle organer og systemer i den patologiske prosessen, er en undersøkelse av en terapeut obligatorisk. Ved mistanke om trombotiske komplikasjoner er det nødvendig med en konsultasjon med en karkirurg. Ved uttalt hydrothorax er det nødvendig med en konsultasjon med en thoraxkirurg for å avgjøre om man skal utføre en pleurapunksjon.
Hva trenger å undersøke?
Hvordan undersøke?
Hvilke tester er nødvendig?
Behandling av ovarielt hyperstimuleringssyndrom
Fraværet av et klart konsept over patofysiologien til OHSS gjør det umulig å utføre effektiv, patogenetisk underbygget behandling som effektivt og raskt stopper utviklingen av syndromet og flere organsykdommer som følger med alvorlige former for ovarielt hyperstimuleringssyndrom. For tiden finnes det ingen spesifikk terapi for ovarielt hyperstimuleringssyndrom, så behandlingstiltak for disse pasientene reduseres til patogenetisk terapi inntil spontan regresjon av syndromet ettersom konsentrasjonen av hCG i blodplasmaet synker over 7 dager i sykluser der graviditet ikke har oppstått, eller 10-20 dager når graviditet har oppstått. De fleste pasienter som er innlagt på intensivavdelinger er allerede innlagt med en diagnose av OHSS etter poliklinisk behandling, som består av daglig vurdering av vekt og diurese, begrensning av overdreven fysisk aktivitet og seksuell aktivitet, rikelig drikking med tilsetning av løsninger rike på elektrolytter og periodiske blodprøver. Diskusjon av behandlingsstrategien for denne pasientgruppen innebærer omfattende symptomatisk behandling som tar sikte på å forhindre utvikling av PRF ved å gjenopprette CCP, eliminere hemokonsentrasjon, elektrolyttforstyrrelser, forhindre akutt nyresvikt, ARDS og tromboemboliske komplikasjoner.
Fase 1 - vurdering av tilstandens alvorlighetsgrad
Det første trinnet i å bestemme taktikken for behandling av en pasient med ovarielt hyperstimuleringssyndrom er å vurdere hemodynamikk og respirasjonsfunksjon. Det er også nødvendig å gjennomføre en fullstendig fysisk undersøkelse med en grundig undersøkelse av tilstanden til lemmer, hode og nakke for å utelukke dyp venetrombose og installere et perifert venekateter eller sentralvenekateterisering. Subclaviavenekateterisering er mest hensiktsmessig, siden risikoen for trombose i dette tilfellet er den laveste. Kateterisering av blæren er nødvendig for å vurdere diurese. Det er nødvendig å undersøke kliniske blodprøveparametere, blodplasmaelektrolytter, protein, leverenzymaktivitet, kreatinin, ureanivåer og koagulogramparametere daglig. Abdominal ultralyd utføres for å bestemme graden av eggstokkforstørrelse og tilstedeværelsen av ascites.
Fase 2 - infusjonsbehandling
Medikamentell behandling av pasienter med OHSS bør ta sikte på å opprettholde hemodynamikk og mobilisere væske i bukhulen ved å skape en negativ natrium- og vannbalanse. Hovedmålet er å erstatte volumet av sirkulerende væske for å redusere hemokonsentrasjon og opprettholde tilstrekkelig nyrefiltrasjon. Krystalloid- og kolloidløsninger brukes til infusjonsbehandling av ovarielt hyperstimuleringssyndrom.
Valget av krystalloidløsning bestemmes av elektrolyttbalansen. Når man bestemmer mengden administrerte krystalloider, er det nødvendig å ta hensyn til at volumet av disse løsningene ved generell endotelskade bør være 2–3 ganger mindre enn volumet av kolloidløsninger, siden overvekten av krystalloider forverrer væskeopphopningen i serøse hulrom, og i noen tilfeller fører til utvikling av anasarka.
Det foretrukne legemidlet for gjenoppretting og vedlikehold av intravaskulært volum hos pasienter med OHSS er hydroksyetylstivelse 130/0 42 daglig volum - 25-30 ml/kg. Hydroksyetylstivelse 200/0 5 kan også brukes i grunnbehandlingen av OHSS i et volum på 20 ml/(kg x dag). Imidlertid kan det akkumuleres i kroppen, og ved langvarig bruk kan det forårsake leverdysfunksjon og øke nivået av levertransaminaser, noen ganger opptil 800 U/l. Hos denne pasientgruppen er det upassende å bruke hydroksyetylstivelse 450/0 7 på grunn av høy risiko for allergiske reaksjoner, negativ påvirkning på nyre- og leverfunksjon, forverring av hemokoagulasjonsparametere (forlengelse av blodkoagulasjonstid, risiko for hemoragiske komplikasjoner). Indikasjoner for bruk av dekstranløsninger er begrenset av den høye frekvensen av allergiske reaksjoner, negativ påvirkning på hemostasesystemet, frigjøring av von Willebrand-faktor, induksjon av den proinflammatoriske kaskaden og mangel på påvirkning på blodets reologiske egenskaper i de dosene som brukes. Infusjon av dekstraner under forhold med økt kapillærpermeabilitet kan føre til utvikling av det såkalte dekstransyndromet, ledsaget av OL, nedsatt lever- og nyrefunksjon og utvikling av koagulopati. Gelatinløsninger er heller ikke beregnet for infusjonsbehandling ved OHSS.
Ved hypoproteinemi mindre enn 25 g/l brukes en 20 % albuminløsning, det daglige volumet er 3 ml/kg. Det anbefales å kun bruke en 20 % albuminløsning, siden det onkotiske trykket i en 20 % løsning er omtrent 100 mm Hg, og det onkotiske trykket i en 5 % løsning er omtrent 20 mm Hg. Under forhold med høy permeabilitet av det vaskulære endotelet fører infusjon av en 5 % albuminløsning, i motsetning til en 20 % løsning, til en mer intensiv utveksling med det ekstravaskulære bassenget og en kraftig økning i onkotisk trykk i interstitiet, noe som fører til en økning i interstitiell hyperhydrering av lungene.
Diuretika er berettiget ved oliguri, perifert ødem, som når hematokritverdier på 36–38 %. For tidlig eller overdreven forskrivning av diuretika kan provosere frem forverring av hypovolemi og hemokonsentrasjon, noe som øker risikoen for trombotiske komplikasjoner. Furosemid brukes hovedsakelig – 20–40 mg én gang intramuskulært eller intravenøst langsomt i 1–2 minutter.
Prinsipper for infusjonsbehandling for ovarielt hyperstimuleringssyndrom
Etter at den første dosen av krystalloid- og kolloidløsninger er administrert, bestemmes volumet av videre infusjonsbehandling under hensyntagen til følgende parametere: diurese - mindre enn 1 ml/(kg t), hematokrit mindre enn - 40 %, gjennomsnittlig arterielt trykk - mer enn 70 mm Hg, sentralt venetrykk - 8–10 mm H2O. Når de spesifiserte parameterne er nådd, stoppes infusjonsbehandlingen. Det anbefales å administrere det totale daglige volumet av infusjonsløsninger i fraksjoner gjennom dagen. Unnlatelse av å følge disse metodene fører til utvikling av hemodilusjon, som fremkaller rask væskeansamling i serøse hulrom og forverring av pasientens tilstand. En typisk feil i behandlingen av kvinner med OHSS er uberettiget forlengelse av infusjonsbehandling når hemodynamiske parametere har normalisert seg, og et forsøk på å fullstendig stoppe utviklingen av OHSS som en iatrogen tilstand.
Fase 3 - forebygging av komplikasjoner
Forebygging av trombose og tromboembolisme
Grunnlaget for å forebygge trombotiske komplikasjoner ved ovarielt hyperstimuleringssyndrom er eliminering av hemokonsentrasjon. Antitrombotisk behandling er indisert når laboratorietegn på hyperkoagulasjon oppstår. LMWH brukes til dette:
- kalsiumnadroparin (daglig dose - 100 anti-Xa IE/kg 2 ganger subkutant),
- dalteparinnatrium (100–150 anti-Xa IE/kg 2 ganger subkutant),
- enoksaparinnatrium (1 ml/kg/dag) 1–2 ganger subkutant).
Laboratorieovervåking - bestemmelse av plasma-anti-Xa-aktivitet 3 timer etter administrering av LMWH, noe som gjør det mulig å opprettholde en effektiv dose av legemidlet innenfor det trygge terapeutiske området og dermed minimere sannsynligheten for blødning. Antitrombotiske legemidler fortsettes inntil blodkoagulasjonsparametrene er normalisert. Overvåking utføres ved å bestemme konsentrasjonen av D-dimer i plasma ved hjelp av en kvantitativ metode. Varigheten av LMWH-administrering bestemmes individuelt, og i noen tilfeller kan den overstige 30 dager.
Forebygging av smittsomme komplikasjoner
Med tanke på den positive effekten av å foreskrive immunoglobulinpreparater for å forhindre sekundære infeksjoner ved andre sykdommer ledsaget av proteintap, kan man forvente effektiviteten av denne behandlingen hos pasienter med OHSS. For å endelig bekrefte eller avkrefte denne hypotesen fra et evidensbasert medisinperspektiv, er det imidlertid nødvendig å gjennomføre studier. For tiden er indikasjonen for empirisk antibakteriell behandling risikoen for sekundær infeksjon hos pasienter i kritisk tilstand eller med ustabil hemodynamikk. Det empirisk valgte legemidlet endres basert på resultatene av bakteriologisk testing. Ved foreskrivelse av empirisk antibakteriell behandling er det nødvendig å veiledes av informasjon om sykdommens alvorlighetsgrad, risikofaktorer for infeksjon og egenskapene til antibiotikaresistens på en gitt intensivavdeling.
Ernæringsstøtte
Det administreres per os til alle pasienter med alvorlig og kritisk OHSS. Det er nødvendig å følge anbefalingene:
- energiverdi 25–35 kcal/(kg x dag),
- glukose - mindre enn 6 g/(kg x dag),
- lipider - 0,5–1 g/(kg x dag),
- proteiner - 1,2–2 g/(kg x dag),
- standard daglig sett med mikroelementer og vitaminer.
Fase 4 - kirurgiske metoder
Indikasjoner for laparocentese hos kvinner med ovarielt hyperstimuleringssyndrom:
- progressiv spent ascites,
- oliguri mindre enn 0,5 ml/dkg/min),
- en økning i kreatininkonsentrasjon over 80 μmol/l eller en reduksjon i clearance,
- hemokonsentrasjon med en hematokritverdi på mer enn 40 %, ikke mottakelig for medikamentell korreksjon.
Transabdominal eller transvaginal tilgang kan velges for laparocentese. Forstørrede eggstokker skaper tekniske vanskeligheter, og derfor er bruk av ultralydkontroll ekstremt viktig. Langtidsdrenasje av bukhulen (transabdominal laparocentese) fra 14 til 30 dager med porsjonsfjerning av peritoneal transudat med apyrogen cystoFix®-kateter har en rekke fordeler, da det gjør det mulig å unngå engangsevakuering av et stort volum peritoneal transudat og dermed eliminere skarpe svingninger i intraabdominalt trykk som forårsaker hemodynamiske forstyrrelser, stabilisere pasientens tilstand og unngå gjentatte punkteringer av bukhulen for å fjerne ascitesvæske hos denne pasientkategorien. Det totale volumet av evakuert ascitesvæske under behandling av alvorlig OHSS kan variere fra 30 til 90 liter.
Hos pasienter med hydrothorax mot bakgrunn av ovarielt hyperstimuleringssyndrom er en avventende tilnærming berettiget. Når hydrothorax dannes, utføres en punktering av pleurahulen kun ved alvorlig progressiv respirasjonssvikt.
Kriterier for oppstart av respiratorisk støtte ved alvorlig og kritisk ovarielt hyperstimuleringssyndrom:
- mangel på spontan pust og patologiske pusterytmer,
- reduksjon i respirasjonsindeks til mindre enn 200 mm Hg,
- livstruende hjertearytmier,
- vedvarende takykardi over 120,
- alvorlig hypotensjon,
- takypné over 40,
- involvering av accessoriske respirasjonsmuskler.
Ved utvikling av ARDS og overføring til mekanisk ventilasjon brukes følgende:
- små respirasjonsvolumer (6 ml/kg),
- inspirasjonstrykk <30 cm H2O,
- PEEP (>10 cm H2O),
- Den alveolære rekrutteringsmanøveren brukes.
Kirurgisk behandling av ovarielt hyperstimuleringssyndrom er kun berettiget ved akutt patologi med vedhengstorsjon, ruptur av ovariecysten eller blødning fra ovariecysten. Ved ovariell torsjon er laparoskopisk avvridning av eggstokken mest effektiv. En typisk feil i behandlingsstrategien for pasienter med ukomplisert ovariell hyperstimuleringssyndrom er akuttkirurgi og reseksjon av omtrent 30–50 % av eggstokkvevet eller bilateral ooforektomi.

