Medisinsk ekspert av artikkelen
Nye publikasjoner
Intestinal atrofi
Sist anmeldt: 07.06.2024

Alt iLive-innhold blir gjennomgått med medisin eller faktisk kontrollert for å sikre så mye faktuell nøyaktighet som mulig.
Vi har strenge retningslinjer for innkjøp og kun kobling til anerkjente medieområder, akademiske forskningsinstitusjoner og, når det er mulig, medisinsk peer-evaluerte studier. Merk at tallene i parenteser ([1], [2], etc.) er klikkbare koblinger til disse studiene.
Hvis du føler at noe av innholdet vårt er unøyaktig, utdatert eller ellers tvilsomt, velg det og trykk Ctrl + Enter.
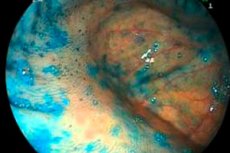
Tarmatrofi er en sekundær patologisk tilstand som oppstår mot bakgrunnen for inflammatoriske reaksjoner i tarmvev - spesielt med et langvarig forløp av kolitt eller enteritt. Sykdommen er preget av periodiske akutte smerteangrep, avføringsforstyrrelser, tap av kroppsvekt, generell svakhet og ubehag. I mangel av rettidig medisinsk behandling, kan farlige komplikasjoner utvikle seg, for eksempel perforering, tarmhindring, blødning, malignisering, etc. Leger anbefaler på det sterkeste at hvis tarmatrofi er mistenkt, er det obligatorisk å kontakte den aktuelle spesialisten og gjennomgå omfattende terapi. [1]
Epidemiologi
Tarmatrofi er en ganske vanlig patologi som finnes både hos voksne og barn. Sykdommen kombinerer elementer i den inflammatoriske prosessen, slimhinnevevsdystrofi, hypotrofi/atrofi av glatt muskel og funksjonsforstyrrelse i tarmen. Denne patologiske tilstanden kan redegjøre (i henhold til forskjellige data) for omtrent 10% av alle kroniske sykdommer i fordøyelsesorganene, med en utbredelse av minst 5-12 tilfeller per 1 tusen populasjon.
Endoskopiske, serologiske, genetiske og morfologiske diagnostiske evner har utvidet seg veldig de siste tiårene. Forskere har utført mange studier som undersøker lidelser i fordøyelseskanalen. Takket være mange vitenskapelige verk, er det ideer om denne patologien, som ikke alltid er symptomatisk manifestert og bekreftet av laboratoriet, noe som gjør statistikk ekstremt vanskelig.
Tarmatrofi har blitt forsket aktivt i mange år, så vel som andre kroniske problemer som påvirker den store og tynntarmen. Likevel er ganske mange problemer fremdeles ikke helt forstått. Fra perspektivet til moderne medisin, blir tarmatrofi betraktet som et klinisk og morfologisk fenomen preget av dyspepsi og smertesyndrom med morfologisk tydelige manifestasjoner av vevsdystrofi/atrofi, skyving av tarmkjertler og formasjon av lymfoplasmacyfiltrasjon av rekinærviddekontroll. Det er visse vevsendringer som er karakteristiske for tarmatrofi, men dette begrepet brukes relativt sjelden i klinisk praksis. Mye oftere kan du høre diagnosen kronisk enterokolitis, irritabelt tarmsyndrom, Crohns sykdom, ikke-spesifikk ulcerøs kolitt.
I ICD-10-listen kan patologien kategoriseres som K52.9-ikke-smittsom gastroenteritt og kolitt uspesifisert.
Svært sjelden er medfødt atrofi av tynntarmsmikrovilli, eller Microvillus inkluderingssyndrom, en sjelden genetisk lidelse arvet på en autosomal recessiv måte. Forstyrrelsen er forårsaket av medfødt atrofi av apikale mikrovilli med intracellulær akkumulering av apikale enzymer i epitelstrukturene i tynntarmen.
Hyppigheten av sykelighet kan variere veldig, avhengig av både de diagnostiske tiltakene som brukes og pasientens vilje til å få medisinsk behandling. Dessverre søker ikke voksne pasienter legehjelp, eller søker det ikke på en riktig måte, men bare på stadiet av komplikasjoner.
En spesiell variant av tarmatrofi - cøliaki - finnes hos en av hundre mennesker i verden, selv om mange ikke søker lege, og prosentandelen av personer med sykdommen kan være mye høyere. I gjennomsnitt etableres en slik diagnose omtrent 5-10 år etter at de første tegnene på lidelsen dukket opp.
Fører til Tarmatrofi
Tarmatrofi er en multifaktoriell patologi. Det er mer enn ti kjente årsaker som kan føre til atrofi av slimhinnevev og som en konsekvens av utviklingen av funksjonell svikt i tarmen. Atrofiske lidelser kan være en konsekvens av patologi eller aldersinfolusjon. Genetisk bestemt hypotrofi eller atrofi av slimhinnevevet i fordøyelsessystemet er ikke uvanlig.
Blant de vanligste årsakene til tarmatrofi anses å være:
- Kroniske inflammatoriske prosesser (kolitt, enteritt, enterokolitis);
- Endringer i lokale og funksjonelle forhold (dette inkluderer dårlig ernæring, stillesittende livsstil, etc.);
- Rus, forgiftning;
- Hormonelle forstyrrelser i kroppen.
I tillegg påvirker psyko-emosjonell stress, en lang historie med røyking og alkoholmisbruk, langvarig eller hyppig bruk av medisiner (spesielt antibiotika, ikke-steroide antiinflammatoriske medisiner og kortikosteroidhormoner) tarmen til tarmen. Sannsynlige provoserende faktorer inkluderer genetisk disposisjon, yrkesfare, samtidig somatiske patologier.
Vi kan skille de hyppigste årsakene til atrofiske forandringer i vevene i forskjellige deler av tarmen:
- Arvelig disposisjon. Hvis de nærmeste pårørende ble funnet å ha tegn på tarmatrofi, øker risikoen for å få denne patologien kraftig til å øke.
- Feil spisevaner. Langvarig faste så vel som hyppige overspising fører til feil funksjon av fordøyelsessystemet.
- Forbruk av lav kvalitet og usunn mat. Noen "usunne" matvarer irriterer tarmen, og bidrar til utviklingen av en kronisk inflammatorisk prosess.
- Forsømmelse av kostholdet foreskrevet av en lege som en del av terapien av enhver patologi i mage-tarmkanalen.
- Langvarig eller alvorlig stress, depresjon, nevrose.
- Langvarig antibiotikabehandling, ubalanse av mikroflora i tarmen, dysbakteriose.
- Rus, inkludert alkoholisk rus. Eventuell rus (forgiftning) påvirker slimhinnene i fordøyelsesorganene negativt.
- Hypodynamia. Mangel på nødvendig fysisk aktivitet svekker muskelsystemet. Tarmens glatte muskler påvirkes også.
- Hyppig bruk av avføringsmedisiner.
- Uavhengig og kaotisk bruk av medisiner som påvirker fordøyelseskanalenes arbeid og tilstand. Dette kan også omfatte feil beregnede doser, ignorere bivirkninger.
Risikofaktorer
Når du vurderer de mulige årsakene til tarmatrofi, bør det tas i betraktning at det i de fleste tilfeller ikke handler om en, men om et helt kompleks av faktorer. I dette tilfellet kaller de ledende årsaken til at mange eksperter kaller fordøyelsesforstyrrelser - det vil si upassende ernæringsmessig karakter og regime. Dette faktum bekreftes av det faktum at prosessene til atrofi alltid er sekundære og oppstår på bakgrunn av andre patologier. Det er ingen hemmelighet at for tiden, ifølge de mest optimistiske beregningene, ikke mer enn 30% av mennesker holder seg til et rasjonelt kosthold. Hovedtyngden av befolkningen overalt krenker matregimet - uordentlig spising, spiser ofte mat "tørr" og "på flukt", overspising, samt irrasjonelt nærmer seg valget av kosthold, spiser mye søt, fet og krydret, misbruk av fastfood, brus og andre skadelige produkter. Og i de fleste tilfeller er feil modus og næring av ernæring til stede i kombinasjon med hverandre.
En viktig rolle i utviklingen av tarmatrofi spiller en viktig rolle i ormeinfeksjoner og tarmfunksjonsbeholdere - spesielt salmonellose, desinfeksjon, Giardiasis, etc., i utviklingen av tarmatrofi. Involvering av kvaliteten på mikrobiell flora er vist ved diagnostisert dysbakteriose, som finnes hos de aller fleste pasienter med tarmatrofi.
Disse faktorene er de ledende når det gjelder årsakene til atrofiske prosesser. Oftest snakker vi om disse hovedkoblingene til patologi:
- Alimentær kobling, som fører til lidelser i tarmmotilitet med videre utvikling av inflammatorisk reaksjon;
- Smittsom-parasittisk kobling, som påvirker tarmvevet direkte med den påfølgende dannelsen av dysbiose, betennelse og ytterligere motoriske lidelser.
Feil kosthold, frekvens og mengde mat som konsumeres, infeksjoner og dysbakteriose, som ofte er kombinert med hverandre, abdominal traumer og arvelig disposisjon - dette er hovedlisten over de mest sannsynlige årsakene til starten av atrofiske prosesser.
Noe rolle spilles også av de såkalte psykogene faktorene som favoriserer begynnelsen og videre forløp av den inflammatoriske reaksjonen. Når du samler anamnesis og intervjuer, avslører tegn på vegetovaskulær dystoni, en tendens til depresjon og hypokonder. Spesialister har nok grunner til å tro involvering av forverret arvelighet. Når det gjelder involvering av psykogene faktorer, er pasienter med tarmatrofi ofte funnet å ha økt angst og usikkerhet, emosjonell labilitet og inntrykkbarhet. På bakgrunn av humørsvingninger og nevrose, forverres tarmmotilitetsforstyrrelser og inflammatoriske reaksjoner.
For gruppen av faktorer som er gunstige for atrofiets utseende, kan vi legge til hypodynamia, unngå fysisk aktivitet, spise hovedsakelig raffinert mat, så vel som mange dårlige vaner - først og fremst som røyking og alkoholmisbruk.
Når det gjelder en slik atrofisk prosess som cøliaki, er flere faktorer involvert i dens utvikling, inkludert gener og kostholdsvaner. Det er en autoimmun sykdom der vevene i tynntarmen er skadet på grunn av forbruk av gluten. Når personer med visse genetiske risikoer spiser mat med gluten, utvikler en immunrespons i form av en respons på glutenproteiner (gliadiner og gluteniner) som angriper tynntarmstrukturer. Under disse angrepene blir villi som letter næringsabsorpsjon skadet. Den skadede villien blir kortere og flatere, og svekker absorpsjonen av næringsstoffer betydelig.
Personer med cøliaki har allelvarianter som HLA-DQ2 eller HLA-DQ8. Å arve disse allelene fører imidlertid ikke alltid til utvikling av cøliaki og tarmatrofi. I tillegg må andre faktorer være til stede, for eksempel forbruk av glutenholdig mat (hvete, bygg, rug, etc.). [2]
Patogenesen
Den patogenetiske mekanismen for tarmatrofi henger ofte sammen med lidelser i tarmbiocenose. Patologisk proinflammatorisk rolle spilles av mikrobielle aminosyrer - metabolske produkter scatol og indol. På grunn av økt aktivitet av opportunistisk flora øker histaminnivået, noe som fører til generell sensibilisering, svekkelse av humoral og cellulær beskyttelse. Siden slik flora perfekt tilpasser seg miljøforhold, undertrykker den gradvis sunn tarmflora. På bakgrunn av bifidobakteriets mangel forstyrres prosessene for fordøyelse, absorpsjon og assimilering av ernæringskomponenter.
En betydelig rolle i den patogenetiske mekanismen for tarmatrofiutvikling spilles av nevroregulerende lidelser av organet, som er basert på svakheten i hemmende effekter av hjernebarken på de nedre seksjonene med et sterkt fall i reaktiviteten til det sympatiske delen av det autonome nervesystemet, så i en økning i reaktiviteten av bioaktive substanser - histisk nervøs.
Et betydelig bidrag til utviklingen av atrofiske prosesser er en svikt i immunologisk reaktivitet. Økning i nivået av immunoglobuliner ledsages av utseendet til tarmsautoantistoffer i blodet, noe som indikerer involvering av sensibilisering for vevsantigener. Med endringer i de biologiske og immunologiske egenskapene til mikroorganismen, blir symbiotiske forhold mellom organismen og tarmmikroflora forstyrret, noe som skaper gunstige forhold for immunologiske lidelser. [3]
Blodsirkulasjonen gjennomgår sterke endringer. Vaskulære permeabilitetsendringer, manifestasjoner av spredt intravaskulært koagulasjonssyndrom forekommer.
Tarmatrofi kan utvikle seg på grunn av rus og giftige metabolske prosesser, endokrine patologier, sykdommer i sentralnervesystemet. Problemet oppstår naturlig når bevegelighetsforstyrrelser eller toksiske effekter på tarmvev.
Gliadin spiller en ledende rolle i patogenesen av cøliaki. Fraksjonene er giftige for personer med cøliaki. Samtidig spiller alfa-gliadin med 33-mer peptid rollen som en aktivator av immunreaksjon, noe som skyldes dens resistens mot effekten av fordøyelsesproteinaser.
Ved cøliaki er forbruket av mat som inneholder gluten en viktig, men ikke den eneste faktoren i utviklingen av patologien. Antigener av det viktigste histokompatibilitetskomplekset er også viktig. Generelt har tarmatrofi ved cøliaki en multifaktoriell opprinnelse. Sammen med genetisk disponering og giftig glutenpåvirkning, spiller interne miljømessige faktorer en ekstra rolle i utviklingen av lidelsen. [4]
Symptomer Tarmatrofi
Ulike patogenetiske mekanismer for utvikling av tarmatrofi bestemmer mangfoldet og uspesifisiteten til symptomatologien til patologien. Forstyrrelsen har ikke slike symptomer, der det vil være mulig å tydelig bestemme tilstedeværelsen av atrofi. Videre, ofte (spesielt i de tidlige stadiene av utviklingen), er det kliniske bildet ekstremt sparsom. Forløpet av sykdommen er forlenget, den kan fortsette med periodisk veksling av tilbakefall og remisjoner, med en gradvis forverring av problemet.
I perioder med forverring føler pasientene seg verre, tegn på rus vises eller intensiveres: tretthet, appetitt forverres, litt økt temperatur, plager smerter i hodet. Samtidig vises magesmerter - verkende, med en tendens til å intensivere før eller under avføring.
Mange pasienter forbinder begynnelsen eller forverring av smertesyndrom med forbruk av mat: oftere skjer det omtrent 1,5 timer etter et måltid. Hvis det oppstår smerter umiddelbart etter å ha spist, skyldes det økt gass og oppblåsthet i magen. Utladning av gass eller avføringslivet fører til lindring av smerte eller forsvinning. Generelt kan smertesyndromet beskrives som verkende, ofte forårsaket av spising.
I tillegg til smertefulle sensasjoner, blir avføringsrytmen forstyrret, avføringskarakteren endres. Pasienter rapporterer oftere forstoppelse enn diaré. Avføring kan være fraværende i 1-3 dager, noe som noen ganger gjør det nødvendig å gi klyster eller ta avføringsmidler. Slim eller blod kan finnes i avføringen. Feces natur: den såkalte "sauen", eller komprimert fecalom. Noen ganger er det avføring ustabilitet, endring av forstoppelse med diaré.
Mange pasienter presenterer tegn på autonom dysfunksjon og nevrologiske lidelser: søvnløshet eller døsighet, irritabilitet, generell tretthet, hodepine, pulsinstabilitet.
Under ekstern undersøkelse blir symptomer på kronisk rus lagt merke til. Det er plakett på tungen. Abdominalområdet er oppblåst, noen ganger smertefullt ved palpasjon. Ved hyperkinesi dominerer tegn på spastisk kolitt, og ved hypokinesi - atonisk eller hypoton kolitt.
Generelt er løpet av tarmatrofi forlenget, bølget. Andre eksisterende sykdommer i fordøyelseskanalen har en uttalt innflytelse på symptomatologien, som bør være oppmerksom på under diagnosen.
Hvis atrofiske forandringer spredte seg til tarmen og magen, blir slike symptomer som forverring av matlyst, ubehagelig belching og kvalme lagt merke til. Mange pasienter rapporterer en følelse av tyngde og fylde i bukområdet, overdreven spytt, halsbrann og en ubehagelig ettersmak i munnhulen.
Etter hvert utvides det kliniske bildet, supplert med å rumle i magen, intoleranse mot meieriprodukter, avføring ustabilitet. Noen pasienter mister kroppsvekt, anemi utvikler seg, hypovitaminose, noe som resulterer i alvorlig svakhet og tretthet, pustevansker selv med litt fysisk aktivitet.
Problemer med fordøyelse av mat påvirker hudens tilstand. Huden blir tørr, flasser og flass vises. Samtidig forverres immuniteten og synet svekkes.
Første tegn
Det ledende symptomet på alle typer tarmatrofi er sløvt eller angreplignende smerter i bukområdet. Den nøyaktige lokaliseringen av smerter avhenger av hvilket tarmsegment som påvirkes. Dermed kan smerter bemerkes i navlen, i høyre iliac-region, venstre underkostalt område, eller "søl over" i hele abdominalsonen.
Det er ofte midlertidig lettelse etter gass eller en vellykket avføring. Etter en tid kommer smertene tilbake eller forverres. Å ta antispasmodics eller bruke en varmekilde kan også bidra til å lindre smertene.
Utseendet til smerte med fysisk aktivitet eller skyving kan indikere dypere tarmatrofi.
Andre første tegn inkluderer ofte:
- Avføringsforstyrrelser, forstoppelse vekslende med diaré, "sauer" avføring;
- Lyder av "rumling" i magen, oppblåsthet, med en tendens til å intensivere seg etter måltider;
- Unormale urenheter i avføringen (oftere - slim eller blod, streket);
- En følelse av trykk, tyngde i tarmområdet;
- Smertefull Tenesmus (falske trang til å defekere);
- Appetitt forverring og tilhørende glans;
- Subfebrilfeber, hodepine, alvorlig tretthet;
- Peling luft;
- Kvalme og oppkast (sjelden).
Det kliniske bildet av en slik patologisk tilstand som cøliaki har lignende tegn:
- Gauntness;
- Vekslende mellom forstoppelse og diaré;
- Kjedelig, trekker magesmerter;
- Leddsmerter;
- Vesikulære utslett på huden og slimhinnene;
- Konstant og alvorlig tretthet.
Symptomene på tarmatrofi kan sammenfalle med kronisk gastroenteritt. Forløpet av sykdommen - intermitterende, med vekslende perioder med forverringer og remisjoner. Slike endringer blir vanligvis provosert av ernæringsforstyrrelser, eller eksterne stressorer. Dessverre, når de første tegnene blir oppdaget, søker en ekstremt liten prosentandel av pasientene medisinsk hjelp. De fleste pasienter ignorerer problemet eller selvmedisineren, noe som over tid fører til forverring av patologi og utvikling av komplikasjoner.
Mage og tarmatrofi
Utviklingen av atrofiske prosesser i magen blir vanligvis provosert av forskjellige aggressive faktorer - spesielt bakterien Helicobacter pylori, saltsyre, duodenogastrisk refluks, pepsin, samt utilstrekkelig beskyttelse av mucosa (for eksempel et underskudd.
Atrofi begynner omtrent 2-3 år etter starten av den inflammatoriske prosessen. For eksempel finnes atrofiske tegn hos 43% av pasientene med kronisk gastroenterokolitis allerede 10 år etter manifestasjonen av patologi. Spesialister snakker ofte om atrofi som sluttfasen av inflammatorisk sykdom.
To hovedmekanismer er kjent for utvikling av slimhinnevev atrofi:
- Skade på grunn av direkte eksponering (spesielt bakteriell);
- En autoimmun reaksjon.
Helicobacter pylori-infeksjon er massivt utbredt. Det forårsaker skade og strukturelle endringer i celler, påvirker den beskyttende funksjonen til slimhinnen negativt og støtter den konstante forløpet av den inflammatoriske prosessen i vevet, som innebærer atrofi. [5]
På sin side er den autoimmune prosessen forårsaket av arvelige svikt i immunreaktiviteten i kroppen. Under "antigen-antistoff" -reaksjonen er det for tidlig dø-off og feil modning av nye cellulære strukturer. Dette innebærer en gradvis svekkelse av gastrisk surhet, endringer i slimhinnestrukturen, en reduksjon i produksjonen av saltsyre. I fordøyelsessystemet blir absorpsjonen av vitaminer og jern svekket, og anemi oppstår.
Helicobacter-assosiert gastritt kan provosere utviklingen av autoimmun aggresjon mot gastrisk epitelvev med videre utvikling av atrofiske og metaplastiske prosesser. Pasienter med påvist Helicobacter pylori er oftere funnet å ha kjertelatrofi, spesielt uttalt ved høye titere av autoantistoffer.
I sin utvikling passerer atrofi av magen og tarmen gjennom flere stadier:
- Superficial inflammatorisk prosess utvikler seg, saltsyreproduksjon lider ubetydelig, det er ingen tegn til patologi;
- Det er foci av atrofi;
- Diffuse endringer med uttalte lidelser av sekretorisk funksjon vises (slimhinnevev er tynning, foci av tynntarmsmetaplasi dannes).
Atrofi av mage og tarm regnes som en av de grunnleggende risikofaktorene for ondartet tumorutvikling. De viktigste symptomene på problemet: Endring i appetitt, kvalme, ubehagelig belk. De fleste pasienter har en følelse av tyngde og fylde i magen, spytt, halsbrann, ubehagelig smak i munnhulen. Gradvis tilsatt og andre symptomer som flatulens, ustabil avføring (forstoppelse erstattes av diaré). Med hyppig diaré er mulig glanshet, manifestasjoner av mineral- og vitaminmangel, anemi. Som et resultat av nedsatt evakuering av mat kan det bli plaget av magesmerter (kjedelig, pressing, med økt intensitet etter spising). Hvis ubehandlede, kan atrofiske prosesser forårsake utvikling av hypovitaminose og anemi, achlorhydria, ulcerative lesjoner og kreft.
Komplikasjoner og konsekvenser
I mangel av behandling og forsømmelse av medisinsk råd, økes risikoen for å utvikle de formidable komplikasjonene av tarmatrofi betydelig:
- Tykktarmskreft; [6]
- Perforering av den berørte tarmveggen;
- Fullstendig eller delvis tarmhindring;
- Cachexia;
- Massiv blødning;
- Septiske komplikasjoner.
Tarmatrofi kan bli så komplisert at pasienten krever akuttkirurgi.
Spesielt alvorlige komplikasjoner inkluderer:
- Giftig Megacolon - Overdreven utvidelse av tykktarmen, forårsaker markert forverring av pasientens velvære, feberfeber, forstoppelse, flatulens, andre utseende av rus.
- Massiv tarmblødning - oppstår når store kar som leverer blod til tarmveggen blir utsatt. Volumet av blodtap kan være opptil 500 ml per dag.
- Perforering av tykktarmen - dannet mot bakgrunnen for overdreven strekk og atrofisk tynning av veggen i det hule organet. Som et resultat utvikler innholdet innhold i bukhulen, peritonitt utvikler seg.
- Kolorektal kreft - er i stand til å utvikle seg med en langvarig eksisterende atrofisk prosess. Atrofi av tykktarmen og endetarmen er spesielt vanlig for malignisering.
Ondartet transformasjon er diagnostisert:
- Med et ti års kurs for atrofi - i 2% av tilfellene;
- Med et 20-årig kurs i 8% av tilfellene;
- Hvis tarmatrofi har vært til stede i mer enn 30 år - i 18% av tilfellene.
Diagnostikk Tarmatrofi
For å få det mest komplette bildet av den eksisterende sykdommen og deretter velge riktig behandlingstaktikk, foreskriver legen en omfattende diagnose, inkludert både laboratorie- og instrumentalstudier.
Blodprøver tas først. Dette er nødvendig for å identifisere den inflammatoriske eller allergiske prosessen, for å bestemme mulig anemi (som et resultat av blodtap), for å vurdere kvaliteten på metabolske prosesser (protein, vannelektrolytt) og sannsynligheten for involvering av leveren eller andre indre organer. Laboratoriediagnostikk utføres også for å vurdere effektiviteten av den foreskrevne behandlingen og overvåke dynamikken.
I tillegg til generelle og biokjemiske blodprøver, kan legen foreskrive en studie av indikatorene for perinukleære cytoplasmatiske antineutrofile antistoffer (Panca), Saccharomyces antistoffer (ASCA) og så videre.
Avføringanalyse inkluderer koprogram, Gregersen-reaksjon (bestemmer tilstedeværelsen av skjult blod). Samtidig oppdages mulige urenheter av slim, pus, avføring blod.
I nærvær av en smittsom prosess og behovet for å velge antibakterielle medisiner foreskriver bakteriologisk kultur og PCR.
Endoskopi er en av de viktigste instrumentelle prosedyrene for tarmatrofi. Metoden kan brukes både på poliklinisk og døgnbasis. På det første stadiet av endoskopisk undersøkelse forklarer legen pasienten hvordan han skal forberede seg på prosedyren på riktig måte. I nesten alle tilfeller krever preparat rensing av tarmhulen ved hjelp av spesielle avføringsmidler, rensende klyster eller begge deler i kombinasjon. På dagen for den planlagte endoskopiske undersøkelsen er forbudt å spise (frokost), har det lov til å drikke vann. Generelt innebærer teknikken introduksjonen av et endoskopisk rør gjennom anus, utstyrt med en lysende enhet og et videokamera. Således kan spesialisten visuelt undersøke tilstanden til slimhinnevevet og bestemme de karakteristiske tegnene på tarmatrofi. Om nødvendig tas en biopsi - en partikkel av tarmvev - samtidig og deretter sendt for histologisk undersøkelse.
Endoskopisk instrumental diagnose kan være representert ved slike prosedyrer:
- Rektoromanoskopi ved bruk av et stivt rektoromanoskop i området for endetarmen og sigmoid kolon;
- Fibroileocolonoscopy ved bruk av et fleksibelt endoskop i tykktarmen og ileum;
- Fibrosigmoidoskopi ved bruk av et fleksibelt endoskop i endetarmen og sigmoid kolon;
- Fibrokolonoskopi ved bruk av et fleksibelt endoskop i tykktarmen.
Varigheten av disse prosedyrene kan variere fra 20-30 minutter til halvannen time (f.eks. Hvis overfladisk anestesi brukes).
Radiografi bestilles bare når endoskopi ikke kan utføres av en eller annen grunn.
En annen vanlig metode, Irrigoskopi, involverer klysteringsadministrasjonen av en bariumsuspensjon - et radiografisk kontrastmiddel - til pasienten, hvoretter røntgenstråler i tarmen tas. Videre, etter tømming, blir luft introdusert i tarmhulen og tar igjen bilder. Som et resultat får spesialisten et bilde av innsnevring og utvidelse av tarmen, områder med betennelse eller overfladiske endringer i slimhinnen.
Gjennomgang av radiografi pålegges å utelukke utvikling av komplikasjoner - for eksempel perforering eller giftig utvidelse av tarmen.
Ultralyd i tarmatrofi brukes praktisk talt ikke på grunn av lav informativitet. [7]
Differensiell diagnose
Før legen går videre til en fullverdig diagnose, må legen utelukke tilstedeværelsen hos pasienten med mange sykdommer som kjører med et lignende klinisk og endoskopisk bilde. Blant slike patologier:
- Smittsom enterokolitis (parasittisk, bakteriell, viral etiologi);
- Crohns sykdom;
- Iskemisk form for enterokolitis (forårsaket av en mangel på blodtilførsel til tarmveggen);
- Divertikulitt;
- Enterokolitis forårsaket av å ta visse medisiner;
- Strålingsinterokolitis;
- En ondartet svulst i tykktarmen;
- Rektal ensom magesår;
- Endometriose hos kvinner osv.
Disse sykdommene kan vise symptomatologi som ligner på tarmatrofi. Behandlingen av disse patologiene er imidlertid grunnleggende annerledes. Det er grunnen til at pasienten skal se lege og ikke prøve å diagnostisere og behandle sykdommen på egenhånd.
Det er ofte vanskelig å skille mellom tarmatrofi og Crohns sykdom. Hvis det er tvil, foreskriver legen ytterligere diagnostikk:
- Immunologisk;
- Radiologisk;
- Endoskopisk.
Å stille riktig diagnose er ekstremt viktig, selv om mange av sykdommene som presenteres har lignende utviklingsmekanismer. Selv i disse situasjonene er behandlingen alltid annerledes. I sjeldne tilfeller stilles en diagnose av uklassifisert (udifferensiert) enterokolitis: når en presis diagnose av en eller annen grunn ikke kan etableres.
Diagnostisering av cøliaki er et eget problem. I motsetning til sykdommer assosiert med matallergier (inkludert glutenallergier), kan cøliaki ikke direkte knyttes til forbruket av glutenholdig mat. Involvering av gluten i skaden av tarmvev kan bare påvises i løpet av morfologisk analyse av slimhinnebiopsi. Atrofi av tynntarmenes villi er karakteristisk ikke bare av cøliaki, men også av akutt tarminfeksjoner eller immunoglobulinmangel.
Når det gjelder divertikulitt, er det en atrofi av tarmmusklene med utvidelsen i lavtliggende områder. Det er en kronisk patologi der veggene i tykktarmen danner sac-lignende bule gjennom muskulaturlaget. Diagnosen divertikulitt er ikke etablert før legen fullstendig utelukker tilstedeværelsen av kreft. Det er viktig å huske at pasienter ofte får diagnosen både divertikula og tykktarmskreft på samme tid. Noen ganger eksisterer kreft og divertikulose sammen i samme segment av tykktarmen.
Hvem skal kontakte?
Behandling Tarmatrofi
Umiddelbart etter diagnose er en pasient med tarmatrofi foreskrevet et spesielt kosthold, noe som er viktig å strengt observere. Spesialister lager en individualisert matplan, som beskriver alle anbefalinger om sammensetningen og reglene for matlaging, kostholdsregime.
Medisiner brukes avhengig av indikasjoner og diagnostiske resultater. Hvis en smittsom prosess blir oppdaget, kan antibiotikabehandling foreskrives. For å redusere smertesyndrom brukes antispasmodics. I de fleste tilfeller er det aktuelt å bruke medisiner som kan gjenopprette normal tarmmikroflora. Hvis det er angitt, kan avføringsmidler eller snerpemidler være nødvendig.
I perioder med inflammatorisk forverring utelukker krydder, stekt og fet mat, ildfast fett, røkt kjøtt og pølser, sauser, konserveringsmidler og marinader. Sopp og nøtter, ferske kaker og pannekaker, kaffe og kakao (inkludert sjokolade), brus og is, hurtigmat og snacks, rå frukt og grønnsaker, melk og tørket frukt er forbudt.
Anbefalte matvarer inkluderer meierifri grøt basert på ris, havregryn, bokhvete, semulegryn. Tillatt egg, frokostblandinger og grønnsakssupper (uten passivering), hvitt magert kjøtt og dampet havfisk, tørket lysbrød, galetter, rusker, vegetabilske potetmos (inkludert potet), bakt frukt uten hud (epler eller pærer), ikke-konsentrerte kompott og sur, ikke-akkidisk naturlig gelé. Maten er dampet, kokt, purert eller purert, bakt, servert varm.
I perioder med remisjon kan ikke mat slipes eller purées. Introduser til naturlige juice med en fortynning av vann 50/50, ikke-sur bær, syltetøy, syltetøy, marshmallows, fersk agurk.
Meieriprodukter introduseres i stabil remisjon. Preferanse gis til ikke-surt cottageost av middels fettinnhold (kan være i form av gryteretter eller dampede ostekaker), naturlig yoghurt og kefir. Hard ikke-skarp ost kan bare konsumeres hvis avstrømningens normale funksjon.
Hvis en pasient får diagnosen cøliaki, er den viktigste terapeutiske metoden en streng livslang overholdelse av et glutenfritt kosthold. Kostholdet er helt fri for hvete, rug, bygg, havre i alle manifestasjonene. Så under forbudet faller brød, pasta, havregryn, hvete eller semulegryn. Den positive effekten av å endre kostholdet blir merkbar i løpet av de første ukene.
Valget av typer konservativ og kirurgisk behandling bestemmes avhengig av alvorlighetsgraden og omfanget av den atrofiske prosessen, effektiviteten av tidligere gjennomført terapi, graden av risiko for komplikasjoner. [8]
Indikasjoner for kirurgisk inngrep inkluderer:
- Fravær av den nødvendige effekten fra konservativ behandling eller umulighet av dens fortsettelse;
- Utvikling av tarmkomplikasjoner;
- Prosess malignitet, eller dens økte risiko.
Forebygging
Dessverre tenker de fleste på sin egen helse for sent, når sykdommen allerede utvikler seg, er det uttalte symptomer. Mange, til og med å vite om tilstedeværelsen av problemet, fortsetter å forsømme rådene fra legen, ignorerer anbefalingene om sunn mat og aktiv livsstil, med tanke på det som et spørsmål om vanskeligheter og ineffektivt. I mellomtiden er den mest effektive forebyggingen av utviklingen av tarmatrofi bare enkel og effektiv. Den består av følgende anbefalinger:
- Spis regelmessig, omtrent samtidig;
- Konsumere en tilstrekkelig mengde romtemperaturvæske (beregning av det optimale væskevolumet - fra 30 til 40 ml per 1 kg kroppsvekt);
- Unngå søtsaker, mat med konserveringsmidler, røkt kjøtt, krydret krydder, animalsk fett;
- Inkluder gjærede melkeprodukter, fiber, vegetabilske oljer i det daglige kostholdet.
Det er obligatorisk å gi opp kjente dårlige vaner. Det er bevist at alkohol og nikotin bidrar til utvikling av inflammatoriske prosesser i GI-kanalen, onkologien, patologiene til leveren og bukspyttkjertelen, noe som skyldes negativ påvirkning av alkoholer, giftstoffer, kjemiske forbindelser. VIKTIG: Fordøyelsesproblemer, inkludert tarmatrofi, kan indirekte provosere ikke bare konvensjonelle sigaretter, men også Hookahs, IQOs og så videre.
Et annet viktig forebyggende tiltak er å ta en bevisst tilnærming til din egen helse. Selvmedisinering skal ikke praktiseres: Hvis mistenkelige symptomer vises, er det nødvendig å besøke familielegen din og gjennomgå diagnostikk. Uberettiget og feil bruk av medisiner kan føre til veldig uheldige konsekvenser. For eksempel kan tarmatrofi provoseres ved langvarig bruk av ikke-steroide antiinflammatoriske medisiner, langvarig antibiotikabehandling, analfabet bruk av kortikosteroidmedisiner. Ikke mindre farlig og alle slags folkeprosedyrer med uprovosert effektivitet: Denne kategorien inkluderer en rekke såkalte "rensing" av GI-kanalen, Tyubazhi, langvarig faste, etc. Noen av disse prosedyrene bør avtales på forhånd med en lege og utføres bare med hans tillatelse og under hans tilsyn.
For å forhindre sykdommer i magen og tarmen, anbefales det å normalisere den psyko-emosjonelle tilstanden, unngå overarbeid, stress, overdreven reaksjoner på mulige vanskelige livssituasjoner (oppsigelse, skilsmisse, etc.). I disse situasjonene kan hjelpe økter med meditasjon, rådgivningspsykolog, sportstrening, autotraining. I noen tilfeller kan spesielle beroligende midler tas etter legens insistering.
Forebygging inkluderer også kampen mot overvekt: den består av riktig ernæring og trening. Det er kjent at overdreven kroppsvekt provoserer utseendet til problemer med bukspyttkjertelen og leveren, bidrar til en reduksjon i tarmmotiliteten. For å bli kvitt ekstra kilo, må du nøye vurdere og lage et kosthold, hvis grunnlag skal være grønnsaker og frukt, korn, magert hvitt kjøtt og sjømat. Et sunt kosthold kompletteres nødvendigvis av kompetent og dosert fysisk aktivitet.
Disse tiltakene kan gradvis stabilisere metabolismen, styrke immuniteten, mette blodet med oksygen, forbedre psyko-emosjonell tilstand. Som et resultat - vil en person unngå utvikling av forskjellige sykdommer i fordøyelsessystemet, inkludert tarmatrofi, og bevare sin egen helse i lang tid.
Prognose
Tarmatrofi er en alvorlig patologisk endring i tarmstrukturen. Hvis behandlingen blir forsømt eller utidig terapeutiske tiltak, kan utvikle alvorlige komplikasjoner, indre blødninger, irreversible endringer i fordøyelsessystemet.
For å forbedre prognosen for sykdommen, unngå ytterligere morfologiske endringer og utvikling av tykktarmskreft, anbefales det:
- Kontakt legen din minst to ganger i året;
- Utfør rutinemessig endoskopi regelmessig (frekvens bestemmes av legen avhengig av intensiteten av morfologiske avvik i tarmen);
- Ta regelmessig blodprøver for rettidig påvisning av anemi og vurdering av dynamikken i behandlingen;
- Følg kostholdet som er foreskrevet av den behandlende legen;
- Følg alle medisiner som er foreskrevet av legen din;
- Koordinere med leger for å ta medisiner som kan påvirke tarmvevets tilstand negativt.
Tarmatrofi er en sykdom som er preget av tynning av tarmslimhinnen, som skyldes påvirkning av negative faktorer. Opprinnelig utvikler den inflammatoriske prosessen seg gradvis, slimhinnen blir ødelagt ned til den ligamentøse muskulære mekanismen til den berørte delen av mage-tarmkanalen. På grunn av den langvarige patologiske prosessen, er lumen til det hule orgelbryter, dens funksjon gradvis går tapt.
Tarmatrofi er ledsaget av en rekke ikke-spesifikke symptomer som forverrer pasientens livskvalitet betydelig. Og noen komplikasjoner kan utgjøre en trussel ikke bare for helse, men også for pasientens liv. Dessverre er det ofte vanskeligheter med rettidig etablering av riktig diagnose, siden symptomatologien for tarmatrofi ligner på andre sykdommer i dette organet. Likevel, hvis diagnosen stilles i tid og riktig, og den foreskrevne behandlingen er riktig, kan prognosen betraktes som betinget gunstig. Det er umulig å kurere sykdommen fullstendig, men det er ofte mulig å stoppe videreutviklingen.

