Medisinsk ekspert av artikkelen
Nye publikasjoner
Syntese, utskillelse og metabolisme av katekolaminer
Sist anmeldt: 06.07.2025

Alt iLive-innhold blir gjennomgått med medisin eller faktisk kontrollert for å sikre så mye faktuell nøyaktighet som mulig.
Vi har strenge retningslinjer for innkjøp og kun kobling til anerkjente medieområder, akademiske forskningsinstitusjoner og, når det er mulig, medisinsk peer-evaluerte studier. Merk at tallene i parenteser ([1], [2], etc.) er klikkbare koblinger til disse studiene.
Hvis du føler at noe av innholdet vårt er unøyaktig, utdatert eller ellers tvilsomt, velg det og trykk Ctrl + Enter.
Binyremargen produserer forbindelser med en struktur som er langt fra steroider. De inneholder en 3,4-dihydroksyfenyl (katekol)-kjerne og kalles katekolaminer. Disse inkluderer adrenalin, noradrenalin og dopamin beta-hydroksytyramin.
Rekkefølgen for katekolaminsyntese er ganske enkel: tyrosin → dihydroksyfenylalanin (DOPA) → dopamin → noradrenalin → adrenalin. Tyrosin kommer inn i kroppen med mat, men kan også dannes fra fenylalanin i leveren under påvirkning av fenylalaninhydroksylase. Sluttproduktene av tyrosinomdannelse i vev er forskjellige. I binyremargen går prosessen videre til stadiet med adrenalindannelse, i endene av de sympatiske nervene - noradrenalin, i noen nevroner i sentralnervesystemet avsluttes syntesen av katekolaminer med dannelsen av dopamin.
Omdannelsen av tyrosin til DOPA katalyseres av tyrosinhydroksylase, hvis kofaktorer er tetrahydrobiopterin og oksygen. Det antas at dette enzymet begrenser hastigheten på hele prosessen med katekolaminbiosyntese og hemmes av sluttproduktene fra prosessen. Tyrosinhydroksylase er hovedmålet for regulatoriske effekter på katekolaminbiosyntese.
Omdannelsen av DOPA til dopamin katalyseres av enzymet DOPA-dekarboksylase (kofaktor - pyridoksalfosfat), som er relativt uspesifikk og dekarboksylerer andre aromatiske L-aminosyrer. Det finnes imidlertid indikasjoner på muligheten for å modifisere syntesen av katekolaminer ved å endre aktiviteten til dette enzymet. Noen nevroner mangler enzymer for videre omdannelse av dopamin, og det er sluttproduktet. Andre vev inneholder dopamin beta-hydroksylase (kofaktorer - kobber, askorbinsyre og oksygen), som omdanner dopamin til noradrenalin. I binyremargen (men ikke i endene av de sympatiske nervene) er fenyletanolamin tilstede - en metyltransferase som danner adrenalin fra noradrenalin. I dette tilfellet fungerer S-adenosylmetionin som en donor av metylgrupper.
Det er viktig å huske at syntesen av fenyletanolamin-N-metyltransferase induseres av glukokortikoider som kommer inn i medulla fra cortex via portalvenesystemet. Dette kan forklare det faktum at to forskjellige endokrine kjertler er kombinert i ett organ. Betydningen av glukokortikoider for syntesen av adrenalin understrekes av det faktum at cellene i binyremargen som produserer noradrenalin er lokalisert rundt arteriekarene, mens de adrenalinproduserende cellene mottar blod hovedsakelig fra venøse bihuler som ligger i binyrebarken.
Nedbrytningen av katekolaminer skjer hovedsakelig under påvirkning av to enzymsystemer: katekol-O-metyltransferase (COMT) og monoaminoksidase (MAO). Hovedveiene for nedbrytning av adrenalin og noradrenalin er skjematisk vist i figur 54. Under påvirkning av COMT, i nærvær av metylgruppedonoren S-adrenosylmetionin, omdannes katekolaminer til normetanefrin og metanefrin (3-O-metylderivater av noradrenalin og adrenalin), som under påvirkning av MAO omdannes til aldehyder og deretter (i nærvær av aldehydoksidase) til vanillylmandelsyre (VMA), hovednedbrytningsproduktet av noradrenalin og adrenalin. I samme tilfelle, når katekolaminer først eksponeres for MAO i stedet for COMT, omdannes de til 3,4-dioksomandelaldehyd, og deretter, under påvirkning av aldehydoksidase og COMT, til 3,4-dioksomandelsyre og VMC. I nærvær av alkoholdehydrogenase kan 3-metoksy-4-oksyfenylglykol, som er hovedsluttproduktet av adrenalin- og noradrenalin-nedbrytning i sentralnervesystemet, dannes fra katekolaminer.
Nedbrytningen av dopamin er lik, bortsett fra at metabolittene mangler hydroksylgruppen ved beta-karbonatomet, og derfor dannes homovanillinsyre (HVA) eller 3-metoksy-4-hydroksyfenyleddiksyre i stedet for vanillylmandelsyre.
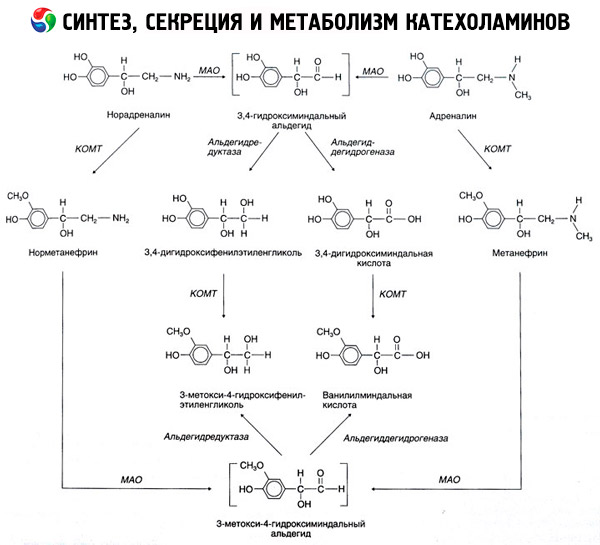
Eksistensen av en kinoid oksidasjonsvei for katekolaminmolekylet, som kan produsere mellomprodukter med uttalt biologisk aktivitet, postuleres også.
Noradrenalin og adrenalin, som dannes under påvirkning av cytosoliske enzymer i de sympatiske nerveendene og binyremargen, kommer inn i de sekretoriske granulene, som beskytter dem mot påvirkning av nedbrytningsenzymer. Oppfanging av katekolaminer av granuler krever energiforbruk. I kromaffingranulene i binyremargen er katekolaminer tett bundet til ATP (i forholdet 4:1) og spesifikke proteiner - kromograniner, som forhindrer diffusjon av hormoner fra granulene inn i cytoplasmaet.
Den direkte stimulansen for utskillelsen av katekolaminer er tilsynelatende penetrasjonen av kalsium inn i cellen, noe som stimulerer eksocytose (fusjon av granulamembranen med celleoverflaten og deres brudd med fullstendig frigjøring av løselig innhold - katekolaminer, dopamin beta-hydroksylase, ATP og kromograniner - i den ekstracellulære væsken).
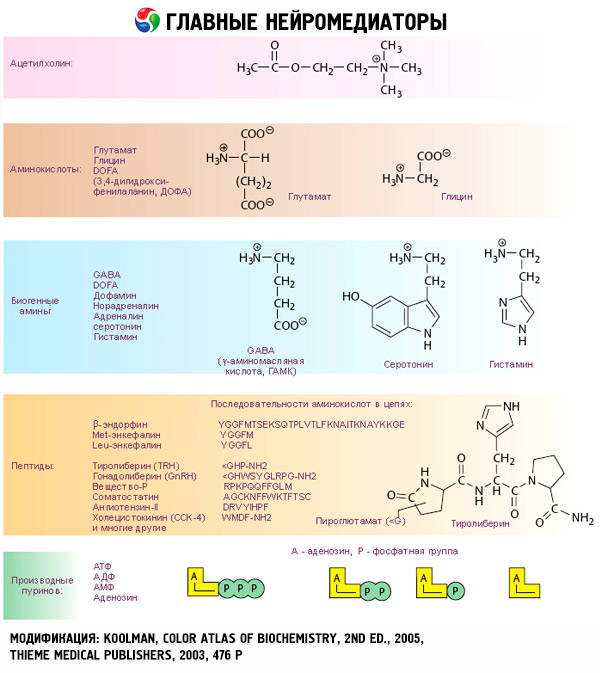
Fysiologiske effekter av katekolaminer og deres virkningsmekanisme
Effektene av katekolaminer begynner med interaksjon med spesifikke reseptorer i målcellene. Mens reseptorer for skjoldbruskkjertel- og steroidhormoner er lokalisert inne i cellene, er reseptorer for katekolaminer (samt acetylkolin- og peptidhormoner) tilstede på den ytre celleoverflaten.
Det har lenge vært fastslått at adrenalin eller noradrenalin er mer effektive enn det syntetiske katekolaminet isoproterenol i noen reaksjoner, mens effekten av isoproterenol er bedre enn virkningen av adrenalin eller noradrenalin i andre. På dette grunnlaget ble det utviklet et konsept om tilstedeværelsen av to typer adrenoreseptorer i vev: alfa og beta, og i noen av dem kan bare én av disse to typene være tilstede. Isoproterenol er den kraftigste agonisten av beta-adrenoreseptorer, mens den syntetiske forbindelsen fenylefrin er den kraftigste agonisten av alfa-adrenoreseptorer. Naturlige katekolaminer - adrenalin og noradrenalin - er i stand til å samhandle med reseptorer av begge typer, men adrenalin har en større affinitet for beta-, og noradrenalin - for alfa-reseptorer.
Katekolaminer aktiverer kardiale beta-adrenerge reseptorer sterkere enn glatte muskulatur-beta-reseptorer, noe som gjorde det mulig å dele beta-typen inn i undertyper: beta1-reseptorer (hjerte, fettceller) og beta2-reseptorer (bronkier, blodkar, etc.). Effekten av isoproterenol på beta1-reseptorer overstiger effekten av adrenalin og noradrenalin bare 10 ganger, mens den på beta2-reseptorer virker 100–1000 ganger sterkere enn naturlige katekolaminer.
Bruken av spesifikke antagonister (fentolamin og fenoksybenzamin for alfa- og propranolol for beta-reseptorer) bekreftet at klassifiseringen av adrenoreseptorer er tilstrekkelig. Dopamin er i stand til å interagere med både alfa- og beta-reseptorer, men forskjellige vev (hjerne, hypofyse, kar) har også sine egne dopaminerge reseptorer, hvis spesifikke blokker er haloperidol. Antallet beta-reseptorer varierer fra 1000 til 2000 per celle. De biologiske effektene av katekolaminer mediert av beta-reseptorer er vanligvis assosiert med aktivering av adenylatcyklase og en økning i det intracellulære innholdet av cAMP. Selv om reseptoren og enzymet er funksjonelt forbundet, er de forskjellige makromolekyler. Guanosintrifosfat (GTP) og andre purinnukleotider deltar i moduleringen av adenylatcyklaseaktivitet under påvirkning av hormonreseptorkomplekset. Ved å øke enzymaktiviteten ser de ut til å redusere affiniteten til beta-reseptorer for agonister.
Fenomenet med økt følsomhet i denerverte strukturer har lenge vært kjent. Tvert imot reduserer langvarig eksponering for agonister følsomheten til målvevet. Studiet av beta-reseptorer har gjort det mulig å forklare disse fenomenene. Det har blitt vist at langvarig eksponering for isoproterenol fører til tap av følsomhet for adenylatcyklase på grunn av en reduksjon i antall beta-reseptorer.
Desensibiliseringsprosessen krever ikke aktivering av proteinsyntese og skyldes sannsynligvis gradvis dannelse av irreversible hormon-reseptorkomplekser. Tvert imot er introduksjonen av 6-oksidopamin, som ødelegger sympatiske ender, ledsaget av en økning i antall reagerende beta-reseptorer i vev. Det er mulig at en økning i sympatisk nerveaktivitet også forårsaker aldersrelatert desensibilisering av blodkar og fettvev i forhold til katekolaminer.
Antallet adrenoreseptorer i forskjellige organer kan kontrolleres av andre hormoner. Dermed øker østradiol og progesteron reduserer antallet alfa-adrenoreseptorer i livmoren, noe som er ledsaget av en tilsvarende økning og reduksjon i dens kontraktile respons på katekolaminer. Hvis den intracellulære "andre budbringeren" som dannes ved virkningen av beta-reseptoragonister absolutt er cAMP, er situasjonen med hensyn til senderen av alfa-adrenerge effekter mer komplisert. Eksistensen av forskjellige mekanismer antas: en reduksjon i nivået av cAMP, en økning i innholdet av cAMP, modulering av cellulær kalsiumdynamikk, etc.
For å reprodusere ulike effekter i kroppen kreves det vanligvis doser adrenalin som er 5–10 ganger mindre enn noradrenalin. Selv om sistnevnte er mer effektivt i forhold til α- og beta1-adrenalinreseptorer, er det viktig å huske at begge endogene katekolaminer er i stand til å interagere med både alfa- og beta-reseptorer. Derfor avhenger den biologiske responsen til et gitt organ på adrenerg aktivering i stor grad av typen reseptorer som er tilstede i det. Dette betyr imidlertid ikke at selektiv aktivering av den nervøse eller humorale forbindelsen i det sympatiske binyresystemet er umulig. I de fleste tilfeller observeres økt aktivitet i de ulike forbindelsene. Dermed er det generelt akseptert at hypoglykemi refleksivt aktiverer binyremargen, mens en reduksjon i blodtrykk (postural hypotensjon) hovedsakelig ledsages av frigjøring av noradrenalin fra endene av de sympatiske nervene.
Adrenoreseptorer og effektene av deres aktivering i forskjellige vev
System, organ |
Adrenerg reseptortype |
Reaksjon |
Kardiovaskulært system: |
||
Hjerte |
Beta |
Økt hjertefrekvens, konduktivitet og kontraktilitet |
Arterioler: |
||
Hud og slimhinner |
Alfa |
Reduksjon |
Skjelettmuskler |
Beta |
Ekspansjonskontraksjon |
Mageorganer |
Alfa (mer) |
Reduksjon |
Beta |
Forlengelse |
|
Årer |
Alfa |
Reduksjon |
Åndedrettssystem: |
||
Musklene i bronkiene |
Beta |
Forlengelse |
Fordøyelsessystemet: |
||
Mage |
Beta |
Reduserte motoriske ferdigheter |
Tarmene |
Alfa |
Sammentrekning av sfinkterne |
Milt |
Alfa |
Reduksjon |
Beta |
Avslapning |
|
Eksokrin bukspyttkjertel |
Alfa |
Redusert sekresjon |
Urogenitalsystemet: |
Alfa |
Sfinkterkontraksjon |
Blære |
Beta |
Avslapning av ejektormuskelen |
Mannlige kjønnsorganer |
Alfa |
Ejakulasjon |
Øyne |
Alfa |
Pupillutvidelse |
Lær |
Alfa |
Økt svetting |
Spyttkjertler |
Alfa |
Utskillelse av kalium og vann |
Beta |
Amylase-sekresjon |
|
Endokrine kjertler: |
||
Øyer i bukspyttkjertelen |
||
Betaceller |
Alfa (mer) |
Redusert insulinsekresjon |
Beta |
Økt insulinsekresjon |
|
Alfaceller |
Beta |
Økt utskillelse av glukagon |
8-celler |
Beta |
Økt utskillelse av somatostatin |
Hypothalamus og hypofysen: |
||
Somatotrofer |
Alfa |
Økt sekresjon av STH |
Beta |
Redusert sekresjon av STH |
|
Laktotrofer |
Alfa |
Redusert utskillelse av prolaktin |
Tyrotrofer |
Alfa |
Redusert TSH-sekresjon |
Kortikotrofer |
Alfa |
Økt ACTH-sekresjon |
| beta | Redusert ACTH-sekresjon | |
Skjoldbruskkjertel: |
||
Follikulære celler |
Alfa |
Redusert utskillelse av tyroksin |
Beta |
Økt utskillelse av tyroksin |
|
Parafollikulære (K) celler |
Beta |
Økt utskillelse av kalsitonin |
Biskjoldkjertlene |
Beta |
Økt sekresjon av PTH |
Nyrer |
Beta |
Økt reninsekresjon |
Mage |
Beta |
Økt utskillelse av gastrin |
BX |
Beta |
Økt oksygenforbruk |
Lever |
? |
Økt glykogenolyse og glukoneogenese med frigjøring av glukose; økt ketogenese med frigjøring av ketonlegemer |
Fettvev |
Beta |
Økt lipolyse med frigjøring av frie fettsyrer og glyserol |
Skjelettmuskler |
Beta |
Økt glykolyse med frigjøring av pyruvat og laktat; redusert proteolyse med en reduksjon i frigjøring av alanin, glutamin |
Det er viktig å ta hensyn til at resultatene av intravenøs administrering av katekolaminer ikke alltid gjenspeiler effekten av endogene forbindelser på en tilstrekkelig måte. Dette gjelder hovedsakelig noradrenalin, siden det i kroppen hovedsakelig ikke frigjøres i blodet, men direkte i synapsekløftene. Derfor aktiverer endogent noradrenalin for eksempel ikke bare vaskulære alfa-reseptorer (økt blodtrykk), men også beta-reseptorer i hjertet (økt hjertefrekvens), mens tilførsel av noradrenalin utenfra hovedsakelig fører til aktivering av vaskulære alfa-reseptorer og en refleks (via vagus) senking av hjerterytmen.
Lave doser adrenalin aktiverer hovedsakelig beta-reseptorer i muskelkar og hjertet, noe som resulterer i en reduksjon i perifer vaskulær motstand og en økning i hjerteminuttvolum. I noen tilfeller kan den første effekten seire, og hypotensjon utvikles etter administrering av adrenalin. I høyere doser aktiverer adrenalin også alfa-reseptorer, noe som er ledsaget av en økning i perifer vaskulær motstand og, mot bakgrunn av en økning i hjerteminuttvolum, fører til en økning i arterielt trykk. Imidlertid er effekten på vaskulære beta-reseptorer også bevart. Som et resultat overstiger økningen i systolisk trykk den tilsvarende indikatoren for diastolisk trykk (økning i pulstrykk). Ved innføring av enda høyere doser begynner de alfa-mimetiske effektene av adrenalin å seire: systolisk og diastolisk trykk øker parallelt, som under påvirkning av noradrenalin.
Effekten av katekolaminer på metabolismen består av deres direkte og indirekte effekter. Førstnevnte realiseres hovedsakelig gjennom beta-reseptorer. Mer komplekse prosesser er assosiert med leveren. Selv om økt leverglykogenolyse tradisjonelt anses å være et resultat av beta-reseptoraktivering, finnes det også bevis for alfa-reseptorinvolvering. Indirekte effekter av katekolaminer er assosiert med modulering av utskillelsen av mange andre hormoner, som insulin. I effekten av adrenalin på utskillelsen dominerer den alfa-adrenerge komponenten tydelig, siden det har blitt vist at ethvert stress er ledsaget av hemming av insulinutskillelse.
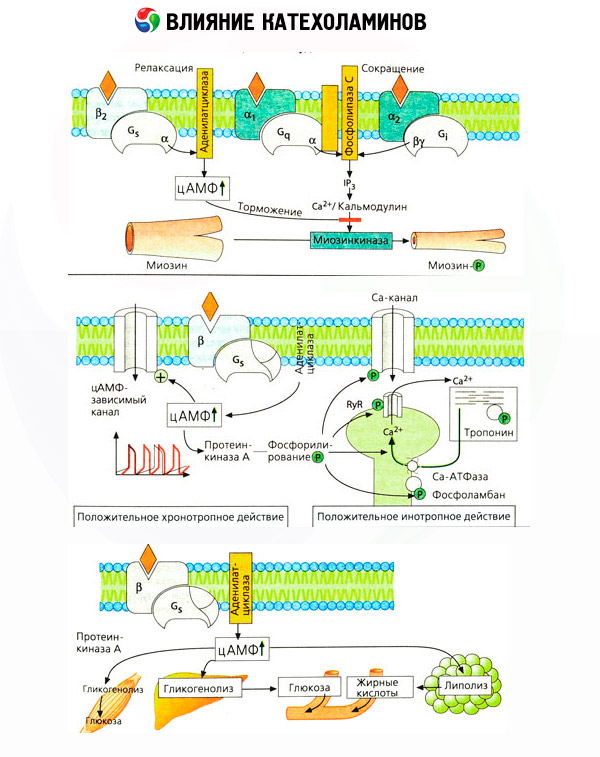
Kombinasjonen av direkte og indirekte effekter av katekolaminer forårsaker hyperglykemi, som ikke bare er forbundet med økt hepatisk glukoseproduksjon, men også med hemming av dens utnyttelse av perifert vev. Akselerasjon av lipolyse forårsaker hyperlipacidemi med økt tilførsel av fettsyrer til leveren og intensivering av ketonkroppsproduksjon. Økt glykolyse i muskler fører til en økning i frigjøring av laktat og pyruvat i blodet, som sammen med glyserol frigjort fra fettvev fungerer som forløpere for hepatisk glukoneogenese.
Regulering av katekolaminsekresjon. Likheten mellom produktene og reaksjonsmetodene i det sympatiske nervesystemet og binyremargen var grunnlaget for å kombinere disse strukturene til et enkelt sympatisk-binyresystem i kroppen med tildeling av dets nervøse og hormonelle forbindelser. Ulike afferente signaler er konsentrert i hypothalamus og sentrene i ryggmargen og medulla oblongata, hvorfra efferente meldinger kommer, og bytter til cellekroppene til preganglioniske nevroner som ligger i de laterale hornene i ryggmargen på nivå med VIII cervikale - II-III lumbale segmenter.
De preganglioniske aksonene i disse cellene forlater ryggmargen og danner synaptiske forbindelser med nevroner som ligger i gangliene i den sympatiske kjeden eller med celler i binyremargen. Disse preganglioniske fibrene er kolinerge. Den første grunnleggende forskjellen mellom sympatiske postganglioniske nevroner og kromaffinceller i binyremargen er at sistnevnte overfører det kolinerge signalet de mottar ikke via nerveledning (postganglioniske adrenerge nerver), men via den humorale banen, og frigjør adrenerge forbindelser i blodet. Den andre forskjellen er at postganglioniske nerver produserer noradrenalin, mens celler i binyremargen hovedsakelig produserer adrenalin. Disse to stoffene har ulik effekt på vev.

