Medisinsk ekspert av artikkelen
Nye publikasjoner
Diagnostisering av artrose: magnetisk resonanstomografi
Sist anmeldt: 04.07.2025

Alt iLive-innhold blir gjennomgått med medisin eller faktisk kontrollert for å sikre så mye faktuell nøyaktighet som mulig.
Vi har strenge retningslinjer for innkjøp og kun kobling til anerkjente medieområder, akademiske forskningsinstitusjoner og, når det er mulig, medisinsk peer-evaluerte studier. Merk at tallene i parenteser ([1], [2], etc.) er klikkbare koblinger til disse studiene.
Hvis du føler at noe av innholdet vårt er unøyaktig, utdatert eller ellers tvilsomt, velg det og trykk Ctrl + Enter.
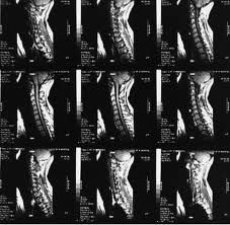
Magnetisk resonansavbildning (MR) har blitt en av de ledende metodene for ikke-invasiv diagnostikk av slitasjegikt de siste årene. Siden 1970-tallet, da prinsippene for magnetisk resonans (MR) først ble brukt til å studere menneskekroppen, har denne metoden for medisinsk avbildning endret seg dramatisk og fortsetter å utvikle seg raskt.
Teknisk utstyr og programvare forbedres, bildeopptaksmetoder utvikles, og MR-kontrastmidler utvikles. Dette gjør at man stadig kan finne nye bruksområder for MR. Hvis bruken først var begrenset til studier av sentralnervesystemet, brukes MR nå med suksess i nesten alle områder av medisin.
I 1946 oppdaget forskergrupper fra Stanford- og Harvard-universitetene uavhengig av hverandre et fenomen kalt kjernemagnetisk resonans (NMR). Essensen var at kjernene til noen atomer, som befinner seg i et magnetfelt, under påvirkning av et eksternt elektromagnetisk felt, er i stand til å absorbere energi og deretter sende den ut i form av et radiosignal. For denne oppdagelsen ble F. Bloch og E. Parmel tildelt Nobelprisen i 1952. Det nye fenomenet ble snart brukt til spektralanalyse av biologiske strukturer (NMR-spektroskopi). I 1973 demonstrerte Paul Rautenburg for første gang muligheten for å få et bilde ved hjelp av NMR-signaler. Slik dukket NMR-tomografi opp. De første NMR-tomogrammene av de indre organene til en levende person ble demonstrert i 1982 på den internasjonale radiologkongressen i Paris.
To presiseringer bør gis. Til tross for at metoden er basert på NMR-fenomenet, kalles den magnetisk resonans (MR), og ordet «kjerne» er utelatt. Dette gjøres slik at pasientene ikke skal ha tanker om radioaktivitet forbundet med nedbrytningen av atomkjerner. Og den andre omstendigheten: MR-tomografer er ikke ved et uhell «innstilt» på protoner, dvs. hydrogenkjerner. Det er mye av dette elementet i vev, og kjernene har det største magnetiske momentet blant alle atomkjerner, noe som bestemmer et ganske høyt nivå av MR-signal.
Hvis det i 1983 bare fantes noen få apparater som var egnet for klinisk forskning i verden, var det i begynnelsen av 1996 omtrent 10 000 tomografer i drift over hele verden. Hvert år introduseres 1000 nye apparater i praksis. Mer enn 90 % av parken med MR-tomografer er modeller med superledende magneter (0,5–1,5 T). Det er interessant å merke seg at hvis selskapene – produsentene av MR-tomografer – på midten av 80-tallet ble styrt av prinsippet «jo høyere felt, desto bedre», med fokus på modeller med et felt på 1,5 T og høyere, ble det på slutten av 80-tallet klart at de i de fleste bruksområder ikke har betydelige fordeler i forhold til modeller med gjennomsnittlig feltstyrke. Derfor vier de viktigste produsentene av MR-tomografer (General Electric, Siemens, Philips, Toshiba, Picker, Bruker, etc.) for tiden stor oppmerksomhet til produksjon av modeller med middels og til og med lave felt, som skiller seg fra høyfeltssystemer i sin kompakthet og økonomi med tilfredsstillende bildekvalitet og betydelig lavere kostnader. Høyfeltssystemer brukes primært i forskningssentre for MR-spektroskopi.
Prinsippet for MR-metoden
Hovedkomponentene i en MR-skanner er: en supersterk magnet, en radiosender, en mottakende radiofrekvensspole, en datamaskin og et kontrollpanel. De fleste enheter har et magnetfelt med et magnetisk moment parallelt med menneskekroppens lengdeakse. Magnetisk feltstyrke måles i tesla (T). For klinisk MR brukes felt med en styrke på 0,2–1,5 T.
Når en pasient plasseres i et sterkt magnetfelt, dreier alle protoner, som er magnetiske dipoler, seg i retning av det ytre feltet (som en kompassnål orientert mot jordens magnetfelt). I tillegg begynner de magnetiske aksene til hvert proton å rotere rundt retningen til det ytre magnetfeltet. Denne spesifikke rotasjonsbevegelsen kalles prosesjon, og frekvensen kalles resonansfrekvens. Når korte elektromagnetiske radiofrekvenspulser sendes gjennom pasientens kropp, fører radiobølgenes magnetfelt til at de magnetiske momentene til alle protoner roterer rundt det magnetiske momentet til det ytre feltet. For at dette skal skje, må frekvensen til radiobølgene være lik protonenes resonansfrekvens. Dette fenomenet kalles magnetisk resonans. For å endre retningen til de magnetiske protonene, må protonenes og radiobølgenes magnetfelt resonerer, dvs. ha samme frekvens.
Et netto magnetisk moment skapes i pasientens vev: vevene magnetiseres, og magnetismen deres er orientert strengt parallelt med det eksterne magnetfeltet. Magnetismen er proporsjonal med antall protoner per volumenhet vev. Det enorme antallet protoner (hydrogenkjerner) som finnes i de fleste vev, betyr at det netto magnetiske momentet er stort nok til å indusere en elektrisk strøm i en mottakerspiral som er plassert utenfor pasienten. Disse induserte MR-signalene brukes til å rekonstruere MR-bildet.
Prosessen med overgangen av elektronene i kjernen fra eksitert tilstand til likevektstilstand kalles spin-gitter-relaksasjonsprosessen eller longitudinell relaksasjon. Den er karakterisert ved T1 - spin-gitter-relaksasjonstiden - tiden som kreves for å overføre 63 % av kjernene til likevektstilstand etter eksitasjon med en 90°-puls. T2 - spin-spinn-relaksasjonstiden skilles også ut.
Det finnes flere metoder for å ta MR-tomogrammer. De varierer i rekkefølgen og arten av generering av radiofrekvenspulser og metoder for MR-signalanalyse. De to mest brukte metodene er spin-lattice og spin-ekko. Spin-lattice analyserer hovedsakelig T1-relaksasjonstiden. Ulike vev (grå og hvit substans i hjernen, cerebrospinalvæske, tumorvev, brusk, muskler, etc.) inneholder protoner med forskjellige T1-relaksasjonstider. Intensiteten til MR-signalet er relatert til varigheten av T1: jo kortere T1, desto mer intenst er MR-signalet og desto lysere vises det gitte området av bildet på TV-skjermen. Fettvev er hvitt på MR-tomogrammer, etterfulgt av hjerne og ryggmarg, tette indre organer, karvegger og muskler i synkende rekkefølge etter MR-signalintensitet. Luft, bein og forkalkninger produserer praktisk talt ikke et MR-signal og vises derfor i svart. Disse T1-relaksasjonstidsforholdene skaper forutsetningene for å visualisere normalt og endret vev på MR-skanninger.
I en annen MR-metode, kalt spin-ekko, rettes en serie radiofrekvenspulser mot pasienten, og roterer de presesserende protonene 90°. Etter at pulsene stopper, registreres MR-responssignalene. Intensiteten til responssignalet er imidlertid relatert annerledes til varigheten av T2: jo kortere T2, desto svakere signal og følgelig desto lavere lysstyrke på gløden på TV-skjermen. Dermed er det endelige MR-bildet ved bruk av T2-metoden det motsatte av det ved bruk av T1-metoden (ettersom et negativt bilde er det motsatte av et positivt bilde).
MR-tomografi viser bløtvev bedre enn CT-skanninger: muskler, fettlag, brusk og blodårer. Noen enheter kan produsere bilder av blodårer uten å injisere kontrastmiddel (MR-angiografi). På grunn av det lave vanninnholdet i beinvevet skaper ikke sistnevnte en skjermingseffekt, slik som ved røntgen-CT-skanning, dvs. at det ikke forstyrrer bildet av for eksempel ryggmargen, mellomvirvelskivene osv. Hydrogenkjerner finnes selvfølgelig ikke bare i vann, men i beinvevet er de fiksert i svært store molekyler og tette strukturer og forstyrrer ikke MR.
Fordeler og ulemper med MR
De viktigste fordelene med MR inkluderer ikke-invasivitet, ufarlighet (ingen strålingseksponering), tredimensjonal bildeopptak, naturlig kontrast fra blod i bevegelse, ingen artefakter fra beinvev, høy differensiering av bløtvev, muligheten til å utføre MP-spektroskopi for in vivo-studier av vevsmetabolisme. MR tillater å ta bilder av tynne lag av menneskekroppen i enhver seksjon - i frontal-, sagittal-, aksial- og skråplan. Det er mulig å rekonstruere volumetriske bilder av organer, synkronisere tomogrammer med elektrokardiogrammets tenner.
De største ulempene inkluderer vanligvis den relativt lange tiden det tar å ta bilder (vanligvis minutter), noe som fører til at det oppstår artefakter fra respirasjonsbevegelser (dette reduserer spesielt effektiviteten av lungeundersøkelse), arytmier (ved hjerteundersøkelse), manglende evne til pålitelig å oppdage steiner, forkalkninger, noen typer beinpatologi, høye kostnader for utstyr og drift, spesielle krav til lokalene der enhetene er plassert (skjerming mot interferens), manglende evne til å undersøke pasienter med klaustrofobi, kunstige pacemakere, store metallimplantater laget av ikke-medisinske metaller.
 [ 8 ], [ 9 ], [ 10 ], [ 11 ], [ 12 ], [ 13 ], [ 14 ], [ 15 ]
[ 8 ], [ 9 ], [ 10 ], [ 11 ], [ 12 ], [ 13 ], [ 14 ], [ 15 ]
Kontrastmidler for MR
I begynnelsen av MR-bruk trodde man at den naturlige kontrasten mellom ulike vev eliminerte behovet for kontrastmidler. Det ble snart oppdaget at forskjellen i signaler mellom ulike vev, dvs. kontrasten i MR-bildet, kunne forbedres betydelig med kontrastmidler. Da det første MR-kontrastmidlet (som inneholdt paramagnetiske gadoliniumioner) ble kommersielt tilgjengelig, økte det diagnostiske informasjonsinnholdet i MR betydelig. Essensen av å bruke MR-kontrastmidler er å endre de magnetiske parametrene til vevs- og organprotoner, dvs. å endre relaksasjonstiden (TR) til T1- og T2-protoner. I dag finnes det flere klassifiseringer av MR-kontrastmidler (eller rettere sagt kontrastmidler - CA).
I henhold til den dominerende effekten på avslapningstiden er MR-KA delt inn i:
- T1-CA, som forkorter T1 og dermed øker intensiteten til vevs-MP-signalet. De kalles også positiv CA.
- T2-CA-er som forkorter T2, og reduserer intensiteten til MR-signalet. Dette er negative CA-er.
Avhengig av deres magnetiske egenskaper er MR-CA delt inn i paramagnetiske og superparamagnetiske:
 [ 16 ], [ 17 ], [ 18 ], [ 19 ], [ 20 ]
[ 16 ], [ 17 ], [ 18 ], [ 19 ], [ 20 ]
Paramagnetiske kontrastmidler
Paramagnetiske egenskaper har atomer med ett eller flere uparede elektroner. Disse er magnetiske ioner av gadolinium (Gd), krom, nikkel, jern og mangan. Gadoliniumforbindelser har fått den bredeste kliniske anvendelsen. Kontrasteffekten til gadolinium skyldes forkortelsen av relaksasjonstiden T1 og T2. I lave doser dominerer effekten på T1, noe som øker signalintensiteten. I høye doser dominerer effekten på T2, noe som reduserer signalintensiteten. Paramagneter er nå mest brukt i klinisk diagnostisk praksis.
Superparamagnetiske kontrastmidler
Den dominerende effekten av superparamagnetisk jernoksid er forkortingen av T2-relaksasjon. Med økende dose er det en reduksjon i signalintensitet. Ferromagnetiske CA-er, som inkluderer ferromagnetiske jernoksider som strukturelt sett ligner magnetittferritt (Fe2 +OFe23+ O3 ), kan også inkluderes i denne gruppen av CA-er.
Følgende klassifisering er basert på farmakokinetikken til CA (Sergeev PV et al., 1995):
- ekstracellulær (vevs-uspesifikk);
- mage-tarmkanalen;
- organotropisk (vevsspesifikk);
- makromolekylære, som brukes til å bestemme det vaskulære rommet.
I Ukraina er fire MR-CA kjent, som er ekstracellulær vannløselig paramagnetisk CA, hvorav gadodiamid og gadopentetinsyre er mye brukt. De resterende gruppene av CA (2-4) gjennomgår kliniske studier i utlandet.
Ekstracellulær vannløselig MR-CA
Internasjonalt navn |
Kjemisk formel |
Struktur |
Gadopentetisk syre |
Gadoliniumdimeglumin-dietylentriaminpentaacetat ((NMG)2Gd-DTPA) |
Lineær, ionisk |
Gadotersyre |
(NMG)Gd-DOTA |
Syklisk, ionisk |
Gadodiamid |
Gadoliniumdietylentriaminpentaacetat-bis-metylamid (Gd-DTPA-BMA) |
Lineær, ikke-ionisk |
Gadoteridol |
Gd-HP-D03A |
Syklisk, ikke-ionisk |
Ekstracellulær CA administreres intravenøst, 98 % av dem skilles ut av nyrene, trenger ikke inn i blod-hjerne-barrieren, har lav toksisitet og tilhører gruppen paramagnetiske stoffer.
Kontraindikasjoner for MR
Absolutte kontraindikasjoner inkluderer tilstander der undersøkelsen utgjør en trussel mot pasientens liv. For eksempel tilstedeværelsen av implantater som aktiveres elektronisk, magnetisk eller mekanisk – dette er primært kunstige pacemakere. Eksponering for radiofrekvensstråling fra en MR-skanner kan forstyrre funksjonen til en pacemaker som opererer i styringssystemet, siden endringer i magnetfelt kan imitere hjerteaktivitet. Magnetisk tiltrekning kan også føre til at pacemakeren forskyver seg i soklen og beveger elektrodene. I tillegg skaper magnetfeltet hindringer for driften av ferromagnetiske eller elektroniske mellomøreimplantater. Tilstedeværelsen av kunstige hjerteklaffer er farlig og er en absolutt kontraindikasjon kun ved undersøkelse på MR-skannere med høye felt, og hvis det er klinisk mistanke om skade på klaffen. Absolutte kontraindikasjoner for undersøkelsen inkluderer også tilstedeværelsen av små kirurgiske metallimplantater (hemostatiske klips) i sentralnervesystemet, siden deres forskyvning på grunn av magnetisk tiltrekning truer blødning. Deres tilstedeværelse i andre deler av kroppen utgjør en mindre trussel, siden fibrose og innkapsling av klemmene etter behandling bidrar til å holde dem stabile. I tillegg til den potensielle faren forårsaker imidlertid tilstedeværelsen av metalliske implantater med magnetiske egenskaper uansett artefakter som skaper vanskeligheter med å tolke resultatene av studien.
Kontraindikasjoner for MR
Absolutt: |
Slektning: |
Pacemakere |
Andre sentralstimulerende midler (insulinpumper, nervestimulatorer) |
Ferromagnetiske eller elektroniske mellomøreimplantater |
Ikke-ferromagnetiske implantater i det indre øret, hjerteklaffproteser (i høye felt, ved mistanke om dysfunksjon) |
Hemostatiske klemmer av hjernekar |
Hemostatiske klemmer på andre steder, dekompensert hjertesvikt, graviditet, klaustrofobi, behov for fysiologisk overvåking |
Relative kontraindikasjoner, i tillegg til de som er nevnt ovenfor, inkluderer dekompensert hjertesvikt og behovet for fysiologisk overvåking (mekanisk ventilasjon, elektriske infusjonspumper). Klaustrofobi er et hinder for studien i 1–4 % av tilfellene. Det kan overvinnes ved å bruke apparater med åpne magneter, og ved en detaljert forklaring av apparatet og undersøkelsesforløpet. Det finnes ingen bevis for en skadelig effekt av MR på embryoet eller fosteret, men det anbefales å unngå MR i første trimester av svangerskapet. Bruk av MR under graviditet er indisert i tilfeller der andre ikke-ioniserende diagnostiske avbildningsmetoder ikke gir tilfredsstillende informasjon. MR-undersøkelse krever mer pasientmedvirkning enn computertomografi, siden pasientbevegelser under undersøkelsen har en mye større effekt på bildekvaliteten, så undersøkelse av pasienter med akutt patologi, nedsatt bevissthet, spastiske tilstander, demens, samt barn er ofte vanskelig.

