Medisinsk ekspert av artikkelen
Nye publikasjoner
Diagnostisering av stadier av prostatakreftforløpet
Sist anmeldt: 04.07.2025

Alt iLive-innhold blir gjennomgått med medisin eller faktisk kontrollert for å sikre så mye faktuell nøyaktighet som mulig.
Vi har strenge retningslinjer for innkjøp og kun kobling til anerkjente medieområder, akademiske forskningsinstitusjoner og, når det er mulig, medisinsk peer-evaluerte studier. Merk at tallene i parenteser ([1], [2], etc.) er klikkbare koblinger til disse studiene.
Hvis du føler at noe av innholdet vårt er unøyaktig, utdatert eller ellers tvilsomt, velg det og trykk Ctrl + Enter.
Klinisk skilles det mellom lokalisert (T1-2 , N0 , M0 ), lokalt avansert (T3-4 , N0-1 , M0 ) og generalisert kreft (T1-4 , N0-1 , M1 ).
Pasienter med klinisk lokaliserte og lokalt avanserte stadier klassifiseres etter risikograd (D'Amico A V. et al., 2003):
- lav: stadium T 1a-c; PSA-nivå mindre enn 10 ig/ml: Gleason-gradering - 2-5; i biopsi - ensidig lesjon mindre enn 50 %:
- moderat: stadium T 2a; PSA-nivå mindre enn 10 ng/ml; Gleason-score - 3 + 4 = 7; i biopsi - bilateral lesjon mindre enn 50 %;
- høyt stadium T2b , T3a -b; PSA-nivå - 10–20 ng/ml; Gleason-gradering - mer enn 4 + 3–7; i biopsi - skade mer enn 50 %, perinevral invasjon;
- svært høyt: stadium T 4; PSA-nivå over 20 ng/ml; Gleason-score over 8; biopsi viser lymfovaskulær invasjon.
Etter at diagnosen er avklart og omfanget av prosessen er fastslått (lokalisert, lokalt avansert eller generalisert), står legen og pasienten overfor et valg av behandlingsmetode. I det moderne samfunnet legges det stor vekt på pasientenes livskvalitet etter behandlingsstart. Livskvaliteten uten behandling tilsvarer forløpet av den underliggende sykdommen og avhenger av progresjonen av den onkologiske prosessen. Endringer i livskvaliteten skjer hovedsakelig etter behandlingsstart og bruk av en av de terapeutiske eller kirurgiske metodene. Å tydelig fastslå prosessens stadium gjør det ikke bare mulig å velge den optimale behandlingsmetoden, men også å forutsi sykdommens videre forløp.
Bestemmelse av PSA-nivået i kombinasjon med det kliniske bildet av prostatakreft og svulstens gradering i henhold til Gleason-skalaen øker informasjonsinnholdet i hver av de listede indikatorene betydelig når det gjelder å fastslå det patologiske stadiet av kreft. AV Partin et al. (1997) foreslo prognostiske tabeller som gjør det mulig å forutsi videre spredning av svulsten, valg av behandlingsmetode, graden av radikalitet og prognosen for behandlingens effektivitet.
For å vurdere spredningen av svulsten er de vanligste metodene DRE, TRUS, bestemmelse av PSA-nivå og beinscintigrafi. Om nødvendig foreskrives computertomografi (CT) eller magnetisk resonansavbildning (MR) og røntgen av thorax.
Enhver av avbildningsmetodene er utformet for å bestemme stadiet og vurdere effektiviteten av behandlingen. Etter å ha bekreftet diagnosen, må urologen avklare volumet av den primære svulsten, dens grenser, svulstens invasive eller metastatiske potensial. Alle disse indikatorene er av stor betydning for sykdomsprognosen og valg av behandlingsmetode.
Primærsvulst (T)
Først og fremst er det nødvendig å avgjøre om svulsten er begrenset til prostata (T 1-2 ) eller strekker seg utover kapselen (T 3-4 ). Digital undersøkelse tillater ofte ikke å vurdere svulstens spredning. Ifølge noen data samsvarer resultatene av DRE med resultatene av histologisk undersøkelse hos mindre enn 50 % av pasientene. Imidlertid er en mer detaljert undersøkelse kun indisert når man bestemmer seg for radikal behandling.
PSA-nivået kan gjenspeile svulstens omfang, men tillater ikke en nøyaktig bestemmelse av det morfologiske stadiet. Kombinasjonen av PSA-nivå, Gleason-indeks og palpasjonsdata gir en bedre prediksjon av det morfologiske stadiet enn hver av disse parameterne separat. Verdien av fritt PSA er kontroversiell: i én studie bidro bestemmelse av fritt PSA-innhold til å avklare stadiet i lokaliserte svulster, men andre studier bekreftet ikke dette. Kun grundige studier vil bidra til å løse dette problemet.
Transrektal ultralyd brukes oftest til å undersøke tilstanden til prostata. Denne metoden kan bare oppdage 60 % av svulstene og viser ikke alltid kapselinvasjon. Nesten 60 % av pasientene har stadium T3 . Ultralyd indikerer en mindre vanlig prosess. Ultralydtegn på kapselinvasjon er utbuling, ujevnheter og ruptur av kjertelens kontur. Invasjon av tumorceller i sædblærene er et dårlig prognostisk tegn, men informasjon om det er ekstremt viktig for valg av behandlingsmetode. Ved utførelse av TRUS bør man være oppmerksom på ekkostrukturen til blærene (hyperekogenisitet), deres asymmetri, deformasjon og ekspansjon. Skade på sædblærene indikeres også av tap av rundhet og kompaktering ved kjertelens base. Disse tegnene er ganske subjektive, så det er upassende å stole utelukkende på ultralyddata. Invasjon av sædblærene indikerer høy risiko for lokalt tilbakefall og metastaser, og biopsi av disse er indisert for avklaring (før kirurgi). Undersøkelsen bør ikke startes med denne prosedyren, men hvis risikoen for invasjon er høy og valg av behandling avhenger av biopsiresultatet, er implementeringen av den berettiget. Et negativt resultat utelukker ikke mikroskopisk invasjon. Som regel utføres en biopsi av sædblærene i klinisk stadium T 2b og høyere, og PSA-innholdet er mer enn 10 ng/ml. Resultatet anses som positivt hvis minst én biopsi fra prostatabasen inneholder tumorceller. Ikke bare ytterligere studier, men også en grundig analyse av resultatene av den primære biopsien gjør det mulig å øke nøyaktigheten av den kliniske bestemmelsen av stadiet (antall og omfang av tumorfokus, kapselinvasjon spiller en rolle). Graden av differensiering er også viktig: med en Gleason-indeks på mindre enn 6 er svulsten lokalisert i 70 % av tilfellene.
Blodstrømmen i prostata ved kreft er høyere enn i en normal kjertel eller ved hyperplasi. Etter kastrering reduseres intensiteten av blodstrømmen i kjertelen. Utviklingen av ekkodopplerografiske kart for diagnose og overvåking av prostatakreft er lovende, men for øyeblikket finnes det ingen pålitelige data om bruk av ekkodopplerografi for å bestemme stadiet i den lokale prosessen. Det er mulig å bruke denne metoden til å innhente ytterligere materiale under målrettet biopsi fra fokus på patologisk vaskularisering.
Resultatene av visualisering av prostatakreft er direkte avhengige av klinikkens tekniske utstyr og spesialistens erfaring. Derfor spiller alle moderne visualiseringsmetoder ikke en avgjørende, men en avklarende rolle, og valget av behandlingsmetode er basert på en kombinasjon av kliniske undersøkelsesdata og instrumentelle studier.
MR har de beste egenskapene for å visualisere strukturen til prostata. Den moderne standarden for undersøkelse av bekkenorganene ved hjelp av MR-metoden er bruk av en endorektal sensor, som gjør det mulig å få et bilde med høyest mulig romlig oppløsning på 0,5–1 mm. Å presse luft inn i den endorektale sensoren gir tydelig visualisering av prostatakapselen, rektoprostatiske vinkler og Denonvilliers' rektoprostatiske fascia. Bruken av en endorektal sensor i MR begrenser ikke visualiseringen av regionale lymfeknuter (opp til nivået av bifurkasjonen av abdominalaorta). Prostatakreft er karakterisert ved lav signalintensitet på T-vektede bilder mot bakgrunnen av et høyintensitetssignal fra en uendret perifer sone av kjertelen. Uregelmessig form, diffus spredning med masseeffekt, uklare og ujevne konturer er morfologiske kjennetegn ved foci med lav signalintensitet i den perifere sonen av prostata, noe som tyder på en neoplastisk natur av lesjonen. Ved dynamisk kontrastering akkumuleres kontrastmiddelet raskt i arteriefasen i kreftfokusene og fjernes raskt, noe som gjenspeiler graden av angiogenese og dermed graden av svulstmalignitet. Lav signalintensitet er også karakteristisk for blødninger etter biopsi, prostatitt, benign stromal hyperplasi i kjertelens nøytrale sone, fibrøse-arrforandringer, fibromuskulær hyperplasi og konsekvenser av hormonell eller strålebehandling. MR uten dynamisk kontrast tillater ikke pålitelig differensiering av de fleste av de listede endringene og sykdommene.
Som nevnt ovenfor, er en av hovedoppgavene til enhver avbildningsmetode for prostatakreft å bestemme volumet av kjertellesjonen og spredningen av svulsten utover kapselen. Å bestemme tumorvolumet er viktig for prognosen. Et tumorvolum på mindre enn 4 cm3 indikerer fjerne metastaser, og 12 cm3 indikerer en ekstremt høy sannsynlighet for metastaser. Ifølge forskning varierer nøyaktigheten til MR i å oppdage foci av neoplastiske lesjoner i prostata fra 50 til 90 %. Sensitiviteten til MR for å bestemme lokaliseringen av prostatakreft er omtrent 70–80 %, mens mikroskopiske foci av kreft (foci) ikke kan oppdages ved hjelp av MR.
Den viktigste fordelen med endorektal MR er evnen til å lokalisere neoplastiske lesjoner i områder som ikke er tilgjengelige for andre diagnostiske metoder, og å avklare arten og retningen på tumorvekst. For eksempel tillater MR å oppdage neoplastiske lesjoner i de fremre delene av den perifere sonen av prostata, som ikke er tilgjengelige med transrektal biopsi. Generelt sett utfyller MR dataene fra DRE og TRUS om tumorlokalisering betydelig.
Endorektal MR muliggjør visualisering av kjertelkapselen, vaskulære nervebunter, sædblærer, kjertelspiss, periprostatisk venøs pleksus og bestemmelse av lokal forekomst av kjerteltumor. Det bør understrekes at kapselpenetrasjon regnes som et mikroskopisk tegn, og selv moderne MR-enheter (endorektal coil) er ikke i stand til å gi slik informasjon. Det er bare mulig å innhente data om vekst utover kjertelkapselen.
Diagnostiske kriterier for ekstrakapsulær ekstensjon ved bruk av MR:
- tilstedeværelsen av en ekstrakapsulær svulst;
- ujevn kontur av kjertelen (deformasjon, vinkelformethet);
- asymmetri av nevrovaskulære bunter;
- utslettelse av de rektoprostatiske vinklene;
- bred kontakt mellom svulsten og kapselen.
Den høyeste spesifisiteten (opptil 95–98 %) og nøyaktigheten av MR-resultater oppnås ved undersøkelse av pasienter med middels eller høy risiko for ekstrakapsulær invasjon. Det antas at ekstrakapsulær invasjon (ifølge MR-data) indikerer upassende kirurgisk behandling og en ugunstig prognose for sykdommen. Hormonell eller strålebehandling påvirker ikke nøyaktigheten av å oppdage ekstrakapsulær spredning av prostatasvulst. Hovedvanskeligheten med å oppdage kreftfokus og ekstrakapsulær spredning av svulst er den høye variasjonen i tolkningen av tomogrammer av forskjellige spesialister. Hovedoppgaven til en spesialist i strålediagnostikk er å oppnå høy diagnostisk spesifisitet (selv på bekostning av sensitivitet) for ikke å frata operable pasienter muligheten for radikal behandling.
Likheten i tettheten av kreft-, hyperplastisk og normalt prostatavev i CT gjør denne metoden lite nyttig for å vurdere lokal spredning av svulsten. Invasjon i sædblærene er viktigere enn invasjon i kapslene, men selv i dette tilfellet gir CT informasjon bare i avanserte tilfeller. Denne metoden brukes imidlertid aktivt for å markere treffområdet før strålebehandling.
Den langsomme utviklingen av strålediagnostikk i landet vårt har ført til sen diagnose av prostatakreft og dermed til utilstrekkelig utbredelse av radikale metoder for behandling av prostatakreft (for eksempel prostatektomi), lav tilgjengelighet av moderne tomografier og mangel på passende opplæringsprogrammer for spesialister i strålediagnostikk og urologer. Til tross for at CT og MR nå er utbredt, er utstyrsnivået på kontorene og utdanningen til spesialister i strålediagnostikk utilstrekkelig til at informasjonen som innhentes er avgjørende for valg av behandlingsmetode for pasienter med prostatakreft.
Regionale lymfeknuter (N)
Regionale lymfeknuter bør kun vurderes når dette direkte påvirker behandlingsstrategien (vanligvis ved planlegging av radikal behandling). Høye PSA-nivåer, T2c -T3a- svulster, dårlig differensiering og perinevral invasjon er assosiert med høy risiko for lymfeknutemetastase. Vurdering av lymfeknutestatus basert på PSA-nivåer anses som utilstrekkelig.
Kun lymfadenektomi (åpen eller laparoskopisk) gir nødvendig informasjon. Nyere studier av utvidet lymfadenektomi har vist at prostatakreft ikke alltid påvirker obturatorlymfeknutene. Ved asymptomatiske svulster og PSA-nivåer under 20 kg/ml bekrefter CT forstørrede lymfeknuter bare i 1 % av tilfellene. Bruk av MR eller CT er berettiget i tilfeller med høy risiko for metastase, siden spesifisiteten til disse metodene når 93–96 %. Imidlertid kan selv et positivt resultat ved bruk av dem være falskt, og bare en punktering av en mistenkelig lymfeknute tillater en å nekte lymfadenektomi. I følge retrospektiv analyse indikerer ikke størrelsen på lymfeknuten alltid tilstedeværelsen av metastaser i den; asymmetri av de berørte lymfeknutene anses som et mer informativt tegn. For tiden får bare 2–3 % av pasientene som har gjennomgått radikal prostatektomi for lokalisert prostatakreft diagnosen metastase til lymfeknutene basert på postoperativ histologisk undersøkelse.
Positronemisjonstomografi (PET) og scintigrafi med merkede antistoffer anbefales som metoder for å påvise metastaser til lymfeknuter, men bruken av dem er fortsatt begrenset på grunn av utilstrekkelig sensitivitet.
Partins nomogrammer (2001) kan brukes til å vurdere risikoen for regional lymfeknuteinvolvering. Nomogrammer er matematiske algoritmer som brukes for en spesifikk pasient eller en gruppe pasienter. Disse tabellene lar en bestemme sannsynligheten for lokal tumorspredning (til kapselen, sædblærene) og lymfeknuteinvolvering basert på klinisk stadium, PSA-nivå og Gleason-indeks. Spesielt gjør de det mulig å identifisere en gruppe pasienter med lav (mindre enn 10 %) sannsynlighet for lymfeknutemetastase (med et PSA-nivå over 20 ng/md, stadium T 1-2a og Gleason-indeks 2-6); i denne gruppen kan tilstanden til lymfeknutene ikke spesifiseres før radikal behandling. Risikoen for lymfeknutemetastase kan også vurderes ved å oppdage tumorområder med uttalt anaplasi (4-5 poeng): hvis slike områder finnes i fire eller flere biopsier eller de dominerer i minst én biopsi, når risikoen 20-45 %. Hos andre pasienter overstiger den ikke 2,5 %. Ytterligere undersøkelse er ikke nødvendig i slike tilfeller.
Fjernmetastaser (M)
Hos 85 % av pasientene som dør av prostatakreft, oppdages lesjoner i aksialskjelettet. Benmetastaser oppstår på grunn av at kreftceller penetrerer benmargen med blodet, noe som fører til tumorvekst og lysis av beinstrukturer. Forekomsten av benmetastaser påvirker prognosen, og tidlig oppdagelse av dem advarer legen om mulige komplikasjoner. I 70 % av tilfellene er metastase kombinert med en økning i aktiviteten til benisoenzymet alkalisk fosfatase (ALP). Bestemmelse av ALP-aktiviteten og PSA-nivået lar oss i de aller fleste tilfeller oppdage benmetastaser. I følge multivariat analyse påvirkes disse indikatorene kun av antall benmetastaser. Det er viktig at aktiviteten til benisoenzymet ALP gjenspeiler graden av beinskade mer nøyaktig enn PSA-nivået.
Scintigrafi regnes som den mest sensitive metoden for å oppdage beinmetastaser (den er bedre enn radiografi og bestemmelse av alkalisk og sur fosfataseaktivitet). Technetiumdifosfonater er bedre brukt som radiofarmasøytisk legemiddel, siden akkumuleringen i bein er mye mer aktiv enn i bløtvev. Det er vist en korrelasjon mellom en semi-kvantitativ vurdering av beinskade og overlevelse. Påvisning av fjerne metastaser er mulig i ethvert organ. De forekommer oftest i ikke-regionale lymfeknuter, lunger, lever, hjerne og hud. Ved tilsvarende plager og symptomer brukes røntgen av brystkassen, ultralyd, CT og MR for å oppdage dem. Taktikken for mistanke om beinmetastaser er presentert i diagrammet.
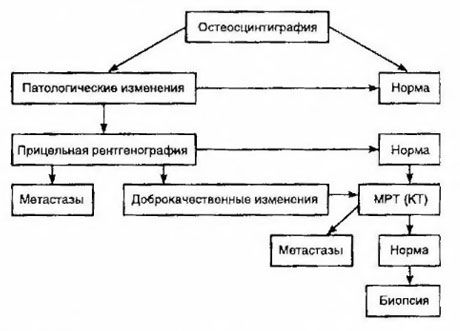
Den mest pålitelige laboratorieindikatoren som bidrar til å bestemme graden av metastase er PSA-nivået. Det har blitt vist at en økning over 100 ng/ml er den eneste parameteren som pålitelig indikerer fjernmetastaser. Bestemmelse av PSA-nivået reduserer antallet pasienter som trenger beinscintigrafi. Sannsynligheten for å oppdage beinmetastaser med en reduksjon i PSA-nivået er svært lav. Ved fravær av plager og et initialt PSA-innhold på mindre enn 20 ng/ml, kan deteksjon av høyt og moderat differensierte svulster, unngås, og scintigrafi kan utføres. Samtidig, ved dårlig differensierte svulster og kapselinvasjon, er scintigrafi indisert (uavhengig av PSA-nivå).


 [
[