Medisinsk ekspert av artikkelen
Nye publikasjoner
Blod-hjerne-barrieren
Last reviewed: 07.07.2025

Alt iLive-innhold blir gjennomgått med medisin eller faktisk kontrollert for å sikre så mye faktuell nøyaktighet som mulig.
Vi har strenge retningslinjer for innkjøp og kun kobling til anerkjente medieområder, akademiske forskningsinstitusjoner og, når det er mulig, medisinsk peer-evaluerte studier. Merk at tallene i parenteser ([1], [2], etc.) er klikkbare koblinger til disse studiene.
Hvis du føler at noe av innholdet vårt er unøyaktig, utdatert eller ellers tvilsomt, velg det og trykk Ctrl + Enter.
Blod-hjerne-barrieren er ekstremt viktig for å sikre homeostase i hjernen, men mange spørsmål angående dens dannelse er ennå ikke fullt avklart. Men det er allerede klart at BBB er den mest differensierte, komplekse og tette histohematiske barrieren. Dens viktigste strukturelle og funksjonelle enhet er endotelcellene i hjernekapillærene.
Hjernens metabolisme er, som ingen andre organer, avhengig av stoffer som kommer inn i blodet. Tallrike blodkar som sikrer nervesystemets funksjon, utmerker seg ved at prosessen med å penetrere stoffer gjennom veggene deres er selektiv. Endotelceller i hjernens kapillærer er forbundet med hverandre med kontinuerlige tette kontakter, slik at stoffer bare kan passere gjennom selve cellene, men ikke mellom dem. Gliaceller, den andre komponenten i blod-hjerne-barrieren, ligger inntil den ytre overflaten av kapillærene. I de vaskulære pleksene i hjernens ventrikler er den anatomiske basisen for barrieren epitelceller, også tett forbundet med hverandre. For tiden anses blod-hjerne-barrieren ikke som en anatomisk og morfologisk, men som en funksjonell formasjon som er i stand til selektivt å passere, og i noen tilfeller levere forskjellige molekyler til nerveceller ved hjelp av aktive transportmekanismer. Dermed utfører barrieren regulerende og beskyttende funksjoner.
Det finnes strukturer i hjernen der blod-hjerne-barrieren er svekket. Dette er først og fremst hypothalamus, samt en rekke strukturer nederst i 3. og 4. ventrikkel – det bakerste feltet (area postrema), de subforniske og subkommissurale organene, og pineallegemet. Integriteten til blod-hjerne-barrieren er forstyrret ved iskemiske og inflammatoriske hjerneskader.
Blod-hjerne-barrieren anses å være fullstendig dannet når egenskapene til disse cellene tilfredsstiller to betingelser. For det første må hastigheten på væskefaseendocytose (pinocytose) i dem være ekstremt lav. For det andre må det dannes spesifikke tette forbindelser mellom cellene, som kjennetegnes av svært høy elektrisk motstand. Den når verdier på 1000–3000 Ohm/cm2 for kapillærer i pia mater og fra 2000 til 8000 m/cm2 for intraparenkymale cerebrale kapillærer. Til sammenligning: gjennomsnittsverdien for transendotelial elektrisk motstand i skjelettmuskelkapillærer er bare 20 Ohm/cm2.
Permeabiliteten til blod-hjerne-barrieren for de fleste stoffer bestemmes i stor grad av deres egenskaper, samt nevroners evne til å syntetisere disse stoffene uavhengig. Stoffer som kan overvinne denne barrieren inkluderer først og fremst oksygen og karbondioksid, samt forskjellige metallioner, glukose, essensielle aminosyrer og fettsyrer som er nødvendige for normal hjernefunksjon. Glukose og vitaminer transporteres ved hjelp av bærere. Samtidig har D- og L-glukose forskjellige penetrasjonshastigheter gjennom barrieren - førstnevnte er mer enn 100 ganger høyere. Glukose spiller en viktig rolle både i hjernens energimetabolisme og i syntesen av en rekke aminosyrer og proteiner.
Den viktigste faktoren som bestemmer funksjonen til blod-hjerne-barrieren er nivået av metabolismen til nerveceller.
Forsyning av nevroner med nødvendige stoffer skjer ikke bare ved hjelp av blodkapillærer som nærmer seg dem, men også takket være prosessene i de myke og araknoide membranene, gjennom hvilke cerebrospinalvæsken sirkulerer. Cerebrospinalvæsken befinner seg i kraniehulen, i hjernens ventrikler og i mellomrommene mellom hjernemembranene. Hos mennesker er volumet omtrent 100–150 ml. Takket være cerebrospinalvæsken opprettholdes den osmotiske balansen i nervecellene, og metabolske produkter som er giftige for nervevevet fjernes.
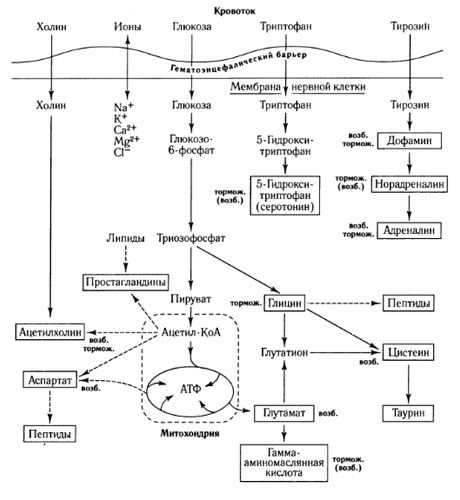
Veier for mediatorutveksling og blod-hjerne-barrierens rolle i metabolismen (ifølge: Shepherd, 1987)
Stoffers passasje gjennom blod-hjerne-barrieren avhenger ikke bare av karveggens permeabilitet for dem (molekylvekt, ladning og lipofilisitet av stoffet), men også av tilstedeværelsen eller fraværet av et aktivt transportsystem.
Den stereospesifikke insulinuavhengige glukosetransportøren (GLUT-1), som sikrer overføringen av dette stoffet over blod-hjerne-barrieren, finnes i rikelig mengde i endotelceller i hjernekapillærene. Aktiviteten til denne transportøren kan sikre tilførsel av glukose i en mengde som er 2–3 ganger større enn det hjernen trenger under normale forhold.
Kjennetegn ved transportsystemene i blod-hjerne-barrieren (ifølge: Pardridge, Oldendorf, 1977)
Transportable |
Foretrukket substrat |
Km, mm |
Vmaks |
Heksoser |
Glukose |
9 |
1600 |
Monokarboksylsyrer |
Laktat |
1.9 |
120 |
Nøytrale |
Fenylalanin |
0,12 |
30 |
Essensielle |
Lysin |
0,10 |
6 |
Aminer |
Kolin |
0,22 |
6 |
Puriner |
Adenin |
0,027 |
1 |
Nukleosider |
Adenosin |
0,018 |
0,7 |
Barn med nedsatt funksjon av denne transportøren opplever en betydelig reduksjon i glukosenivået i cerebrospinalvæsken og forstyrrelser i hjernens utvikling og funksjon.
Monokarboksylsyrer (L-laktat, acetat, pyruvat) og ketonlegemer transporteres av separate stereospesifikke systemer. Selv om transportintensiteten deres er lavere enn glukoses, er de et viktig metabolsk substrat hos nyfødte og under sult.
Kolintransport inn i sentralnervesystemet medieres også av transportøren og kan reguleres av hastigheten på acetylkolinsyntesen i nervesystemet.
Vitaminer syntetiseres ikke av hjernen og tilføres fra blodet ved hjelp av spesielle transportsystemer. Til tross for at disse systemene har en relativt lav transportaktivitet, kan de under normale forhold sikre transport av mengden vitaminer som er nødvendig for hjernen, men mangel på dem i mat kan føre til nevrologiske lidelser. Noen plasmaproteiner kan også trenge inn i blod-hjerne-barrieren. En av måtene de kan penetrere på er reseptormediert transcytose. Slik trenger insulin, transferrin, vasopressin og insulinlignende vekstfaktor inn i barrieren. Endotelceller i hjernekapillærene har spesifikke reseptorer for disse proteinene og er i stand til å endocytere protein-reseptorkomplekset. Det er viktig at komplekset som et resultat av påfølgende hendelser disintegrerer, det intakte proteinet kan frigjøres på motsatt side av cellen, og reseptoren kan igjen integreres i membranen. For polykationiske proteiner og lektiner er transcytose også en måte å trenge inn i blod-hjerne-barrieren på, men den er ikke assosiert med arbeidet til spesifikke reseptorer.
Mange nevrotransmittere i blodet klarer ikke å trenge inn i BBB. Dermed har ikke dopamin denne evnen, mens L-DOPA trenger inn i BBB ved hjelp av det nøytrale aminosyretransportsystemet. I tillegg inneholder kapillærceller enzymer som metaboliserer nevrotransmittere (kolinesterase, GABA-transaminase, aminopeptidaser, etc.), legemidler og giftstoffer, noe som sikrer beskyttelse av hjernen ikke bare mot nevrotransmittere som sirkulerer i blodet, men også mot giftstoffer.
Arbeidet til BBB involverer også bærerproteiner som transporterer stoffer fra endotelcellene i hjernekapillærene til blodet, for eksempel b-glykoprotein.
Under ontogenesen endres transporthastigheten for ulike stoffer gjennom BBB betydelig. Dermed er transporthastigheten for b-hydroksybutyrat, tryptofan, adenin, kolin og glukose hos nyfødte betydelig høyere enn hos voksne. Dette gjenspeiler det relativt høyere behovet for energi og makromolekylære substrater hos den utviklende hjernen.


 [
[