Medisinsk ekspert av artikkelen
Nye publikasjoner
Vanemessig spontanabort - årsaker
Last reviewed: 04.07.2025

Alt iLive-innhold blir gjennomgått med medisin eller faktisk kontrollert for å sikre så mye faktuell nøyaktighet som mulig.
Vi har strenge retningslinjer for innkjøp og kun kobling til anerkjente medieområder, akademiske forskningsinstitusjoner og, når det er mulig, medisinsk peer-evaluerte studier. Merk at tallene i parenteser ([1], [2], etc.) er klikkbare koblinger til disse studiene.
Hvis du føler at noe av innholdet vårt er unøyaktig, utdatert eller ellers tvilsomt, velg det og trykk Ctrl + Enter.
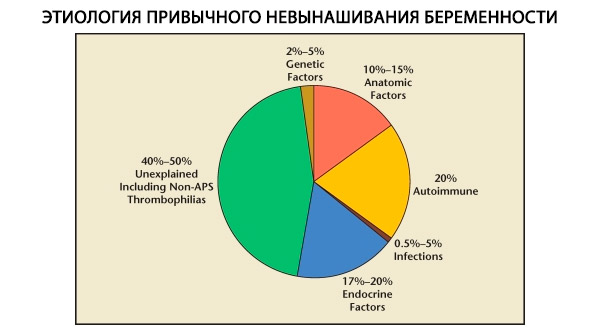
I strukturen av vanemessige svangerskapstap skilles genetiske, anatomiske, endokrine, immunologiske og infeksiøse faktorer. Når alle de ovennevnte årsakene utelukkes, gjenstår en gruppe pasienter der opprinnelsen til vanemessig spontanabort er uklar (idiopatiske spontanaborter). Ifølge C. Coulam et al. (1996) er 80 % av idiopatiske spontanaborter basert på uoppdagede immunforstyrrelser.
Det finnes ingen overbevisende bevis for at endometriose forårsaker tilbakevendende spontanabort, eller at medisinsk eller kirurgisk behandling av endometriose reduserer forekomsten av tilbakevendende spontanabort.
I følge nåværende konsepter, i tillegg til genetiske og delvis infeksiøse årsaker som fører til dannelsen av et unormalt embryo, består implementeringen av den skadelige effekten av andre faktorer (anatomiske, endokrine, immunologiske) i å skape en ugunstig bakgrunn for utviklingen av et genetisk komplett befruktet egg, noe som fører til uttømming av chorions reservekapasitet og opphør av utvikling (embryogenese). Kritiske perioder i første trimester av svangerskapet er anerkjent som 6-8 uker (embryodød) og 10-12 uker (utstøting av det befruktede egget).
 [ 1 ]
[ 1 ]
Genetiske årsaker til vanemessig spontanabort
Genetiske faktorer står for 3–6 % av årsakene til habeutvikling. Ved sporadisk abort i første trimester har omtrent 50 % av abortene kromosomavvik. De fleste av disse (95 %) er endringer i antall kromosomer – monosomi (tap av ett kromosom), trisomi (tilstedeværelsen av et ekstra kromosom), som er et resultat av feil i meiosen, samt polyploidi (en økning i kromosomsammensetningen med et fullt haploidt sett), som oppstår når et egg befruktes av to eller flere sædceller. Ved sporadiske spontanaborter forekommer trisomi oftest – 60 % av alle mutasjoner (oftest på kromosom 16, samt 13, 18, 21, 22), på andreplass i hyppighet er Shereshevsky-Turners syndrom (kromosom 45 X0) – 20 %, de resterende 15 % skyldes polyploidi (spesielt triploidi).
Ved endring i antall kromosomer ved en abort avslører undersøkelsen av foreldrenes karyotype oftest ingen patologi, og sannsynligheten for kromosomsykdom hos fosteret under et påfølgende svangerskap er 1 %. I motsetning til dette observeres strukturelle endringer i kromosomene (intra- og interkromosomale) i 3–6 % av tilfellene ved undersøkelse av aborter hos par med habituell spontanabort. Ved undersøkelse av foreldrenes karyotype finner man balanserte kromosomale omorganiseringer i 7 % av tilfellene. Oftest er dette resiproke translokasjoner, der et segment av ett kromosom er plassert på stedet for et annet segment av et ikke-homologt kromosom, samt mosaikk av kjønnskromosomer, inversjon og deteksjon av kromosomer i form av en ring. Ved tilstedeværelse av slike omorganiseringer hos en av ektefellene hindres prosessene for paring og separasjon av kromosomer under meiose, noe som resulterer i tap (delesjon) eller dobling (duplisering) av kromosomseksjoner i kjønnscellene. Dette resulterer i såkalte ubalanserte kromosomale omorganiseringer, der embryoet enten er ikke-levedyktig eller fungerer som bærer av en alvorlig kromosompatologi. Sannsynligheten for å få et barn med ubalanserte kromosomavvik ved nærvær av balanserte kromosomale omorganiseringer i karyotypen til en av foreldrene er 1–15 %. Forskjeller i data er knyttet til omorganiseringenes art, størrelsen på de involverte segmentene, bærerens kjønn og familiehistorie.
Diagnostikk
Anamnese
- Arvelige sykdommer hos familiemedlemmer.
- Tilstedeværelse av medfødte anomalier i familien.
- Fødsel av barn med psykisk utviklingshemming.
- Tilstedeværelsen av infertilitet og/eller spontanabort av ukjent opprinnelse hos et ektepar eller hos slektninger.
- Tilstedeværelse av uklare tilfeller av perinatal dødelighet.
Spesielle forskningsmetoder
- En studie av foreldrenes karyotype er spesielt indisert for ektepar ved fødselen av en nyfødt med utviklingsdefekter i tillegg til en historie med spontanabort, samt i tilfeller av habituell spontanabort i de tidlige stadiene av svangerskapet.
- Cytogenetisk analyse av abort i tilfeller av dødfødsel eller nyfødtdødelighet.
Indikasjoner for konsultasjon med andre spesialister
Hvis det oppdages endringer i karyotypen hos foreldrene, er det nødvendig med en konsultasjon med en genetiker for å vurdere graden av risiko for å få et barn med en patologi, eller om nødvendig for å avgjøre spørsmålet om å donere et egg eller en sædcelle.
Videre behandling av pasienten
Hvis et ektepar har en patologisk karyotype, selv hos en av foreldrene, anbefales det å utføre prenatal diagnostikk under graviditet - korionbiopsi eller fostervannsprøve - på grunn av den høye risikoen for utviklingsforstyrrelser hos fosteret.
Anatomiske årsaker til vanemessig spontanabort
Anatomiske årsaker til vanemessig spontanabort inkluderer:
- medfødte anomalier i livmorens utvikling (fullstendig dobling av livmoren; bihornet, salformet, enhjørningsformet livmor; delvis eller fullstendig intrauterin septum);
- ervervede anatomiske defekter;
- intrauterine adhesjoner (Ashermans syndrom);
- submukøse livmorfibroider;
- istmisk-cervikal insuffisiens.
Hyppigheten av anatomiske avvik hos pasienter med habituell spontanabort varierer fra 10 til 16 %. Hyppigheten av forekomst av livmormisdannelser som kan føre til spontanabort (men ikke infertilitet) i forhold til alle livmormisdannelser er som følger: bihornet livmor - 37 %, salformet livmor - 15 %, intrauterin septum - 22 %, fullstendig dobling av livmoren - 11 %, enhjørningsformet livmor - 4,4 %.
Diagnose av habituell spontanabort
Anamnese
Ved anatomisk patologi i livmoren observeres sene avslutninger av graviditet og for tidlig fødsel oftere, men ved implantasjon på det intrauterine septum eller nær den myomatiske knuten er tidlig avslutning av graviditet også mulig.
Ved istmisk-cervikal insuffisiens er det patognomoniske tegnet spontan avbrytelse av svangerskapet i andre trimester eller tidlig for tidlig fødsel, som skjer relativt raskt og med lite smerte.
Ved misdannelser i livmoren er det nødvendig å være oppmerksom på anamnestiske indikasjoner på patologi i urinveiene (ofte ledsagende medfødte anomalier i livmoren) og arten av utviklingen av menstruasjonsfunksjonen (indikasjoner på hematometra med et fungerende rudimentært horn i livmoren).
Spesielle undersøkelsesmetoder
- For tiden utføres hysterosalpingografi for å stille en diagnose som gjør det mulig å studere formen på livmorhulen, identifisere tilstedeværelsen av submukøse fibroider, adhesjoner, skillevegger og bestemme eggledernes åpenhet. For å diagnostisere livmorpatologi er det rasjonelt å utføre hysterosalpingografi i perioden mellom menstruasjon og eggløsning, dvs. i den første fasen av menstruasjonssyklusen etter at den blodige utfloden har opphørt (7.-9. dag i syklusen). For å diagnostisere istmisk-cervikal insuffisiens utføres undersøkelsen i den andre fasen av menstruasjonssyklusen (18.-20. dag) for å bestemme tilstanden til livmorhalsens indre os. Før hysterosalpingografi utføres, er det nødvendig å utelukke inflammatoriske sykdommer i bekkenorganene eller behandle dem.
- Hysteroskopi har blitt utbredt de siste årene og har blitt gullstandarden for diagnostisering av intrauterin patologi. På grunn av den høyere kostnaden sammenlignet med hysterosalpingografi, brukes metoden imidlertid hos kvinner med indikasjon på intrauterin patologi basert på foreløpige ultralyddata. Hysteroskopi kan brukes til å undersøke livmorhulen, bestemme arten av den intrauterine patologien, og, hvis nødvendig utstyr (resektoskop) er tilgjengelig, utføre minimalt invasiv kirurgisk behandling - fjerning av adhesjoner, submukøse myomknuter og endometriepolypper. Ved fjerning av en intrauterin septum foretrekkes hysteroresektoskopi med laparoskopisk kontroll, som forhindrer muligheten for perforasjon av livmorveggen.
- Ultralyd utføres i den første fasen av menstruasjonssyklusen, noe som muliggjør en presumptiv diagnose av submukøse livmormyomer, intrauterine adhesjoner, og i den andre fasen av syklusen - for å identifisere en intrauterin septum og en bicornuate livmor. Denne metoden er spesielt viktig i de tidlige stadiene av svangerskapet, når sensitiviteten i diagnostisering av disse tilstandene er 100 %, og spesifisiteten er 80 %. Utenom graviditet krever diagnosen ytterligere bekreftelse med andre metoder.
- Utenlandske forfattere peker på fordelen med sonohysterografi (ultralyd med en transvaginal sensor med forutgående introduksjon av 0,9 % natriumkloridløsning i livmorhulen) fremfor hysterosalpingografi, ettersom det muliggjør differensialdiagnostikk mellom det intrauterine septum og den bihornede livmoren. Med sonohysterografi er det ikke bare mulig å studere formen på livmorhulen, men også å bestemme konfigurasjonen av livmorfundus. I vårt land har denne metoden ikke blitt utbredt.
- I noen komplekse tilfeller brukes MR av bekkenorganene for å bekrefte diagnosen. Metoden gjør det mulig å innhente verdifull informasjon ved utviklingsanomalier i livmoren ledsaget av atypisk organarrangement i bekkenet. MR er viktig ved rudimentære livmorhorn for å avgjøre om det er tilrådelig å fjerne det. Behovet for å fjerne det rudimentære livmorhornet oppstår hvis det er i forbindelse med egglederen og eggstokken for å forhindre dannelse og utvikling av det befruktede egget i det. Avbrudd av svangerskap ved anatomiske anomalier i livmoren kan være assosiert med mislykket implantasjon av det befruktede egget (på den intrauterine septum, nær den submukøse myomknuten), utilstrekkelig utviklet vaskularisering og mottak av endometriet, tette romlige forhold i livmorhulen (for eksempel ved deformasjon av hulrommet av en myomknute), ofte ledsaget av ICI, og hormonelle forstyrrelser.
Behandling av vanemessig spontanabort
Kirurgisk behandling
Ved tilstedeværelse av en intrauterin septum, submukøse myomknuter og adhesjoner er den mest effektive kirurgiske behandlingen hysteroresektoskopi. Hyppigheten av påfølgende spontanaborter i denne gruppen kvinner etter behandling er 10 % sammenlignet med 90 % før operasjonen. Ved sammenligning av resultatene av metroplastikk utført ved laparotomi og transcervikal hysteroresektoskopi, oppnådde P. Heinonen (1997) resultater som indikerer mindre traumer og større effektivitet av hysteroresektoskopi; andelen graviditeter som resulterte i fødsel av levedyktige barn var henholdsvis 68 og 86 %.
Kirurgisk fjerning av intrauterin septum, adhesjoner og submukøse myomknuter eliminerer spontanabort i 70–80 % av tilfellene. Det er imidlertid ineffektivt hos kvinner med livmormisdannelser som har hatt normale fødsler med påfølgende tilbakevendende spontanaborter. Det er sannsynlig at i slike tilfeller er den anatomiske faktoren ikke den viktigste årsaken, og det er nødvendig å se etter andre årsaker til spontanabort.
Det er bevist at abdominal metroplastikk er forbundet med en betydelig risiko for postoperativ infertilitet og ikke forbedrer prognosen for senere graviditeter. Derfor er det bedre å foretrekke hysteroskopi og laparoskopiske operasjoner.
Medikamentell behandling
Effektiviteten av innføring av spiral, høye doser østrogene legemidler, innføring av et Foley-kateter i livmorhulen etter operasjoner for å fjerne sammenvoksninger, intrauterin septum er ikke bevist. Det anbefales å planlegge graviditet tidligst 3 måneder etter operasjonen. For å forbedre veksten av endometriet utføres syklisk hormonbehandling i 3 menstruasjonssykluser [14]. I 3 måneder i løpet av de første 14 dagene av syklusen anbefales det å ta et legemiddel som inneholder 2 mg 17-beta-østradiol, i løpet av de neste 14 dagene - 2 mg 17-beta-østradiol og 20 mg dydrogesteron (10 mg dydrogesteron som en del av et kombinasjonslegemiddel pluss 10 mg dydrogesteron i en separat tablettform).
Videre behandling av pasienten
Funksjoner ved svangerskapsforløpet med en bicornuate livmor eller dobling av livmoren (når det er 2 livmorhulrom):
- I de tidlige stadiene av svangerskapet oppstår det ofte blødning fra det "tomme" hornet eller livmorhulen på grunn av en uttalt decidualreaksjon; taktikken i dette tilfellet bør være konservativ og bestå av bruk av antispasmodiske og hemostatiske midler;
- trussel om svangerskapsavbrudd på ulike stadier;
- utvikling av istmisk-cervikal insuffisiens;
- intrauterin vekstretardasjon på grunn av placentainsuffisiens.
I de tidlige stadiene av svangerskapet, ved blødning, anbefales sengeleie og delvis sengeleie, samt administrering av hemostatiske, krampestillende og beroligende legemidler, og behandling med gestagener (dydrogesteron i en daglig dose på 20 til 40 mg) opptil 16–18 ukers svangerskap.
Endokrine årsaker til vanemessig spontanabort
Ifølge diverse forfattere står endokrine årsaker til spontanabort for 8 til 20 %. De viktigste av disse er lutealfasesvikt (LPD), hypersekresjon av LH, skjoldbruskdysfunksjon og diabetes mellitus.
Alvorlig skjoldbruskkjertelsykdom eller diabetes mellitus kan føre til gjentatte spontanaborter. Ved kompensert diabetes mellitus er imidlertid ikke risikoen for vanemessige spontanaborter forskjellig fra den i den generelle befolkningen.
Samtidig krever den høye forekomsten av hypotyreose i befolkningen screening med måling av TSH-nivåer. Hos pasienter med habituell spontanabort observeres lutealfaseinsuffisiens i 20–60 % av tilfellene, og ultralydtegn på polycystiske eggstokker - i 44–56 %. I følge litteraturen er påvirkningen av individuelle hormonforstyrrelser på dannelsen av symptomkomplekset ved habituell spontanabort fortsatt kontroversiell. Studiene til M. Ogasawara et al. (1997) avdekket ikke pålitelige forskjeller i hyppigheten av svangerskapsavbrudd med og uten LPI hos pasienter med to eller flere tidligere spontanaborter i anamnesen, unntatt autoimmune, anatomiske og infeksiøse årsaker.
Utilstrekkelig funksjon av corpus luteum kan være et resultat av en rekke ugunstige faktorer:
- forstyrrelser i utskillelsen av FSH og LH i den første fasen av menstruasjonssyklusen;
- tidlig eller omvendt for sen topp av LH-frigjøring;
- hypoøstrogenisme som følge av utilstrekkelig follikulogenese. Alle disse tilstandene kan ikke korrigeres ved substitusjonsterapi med gestagenlegemidler i den postovulatoriske perioden. Prospektive studier utført av L. Regan et al. viste en signifikant økning i hyppigheten av spontanaborter hos pasienter med LH-hypersekresjon på den 8. dagen i menstruasjonssyklusen sammenlignet med kvinner med normale LH-nivåer i blodet (henholdsvis 65 % og 12 % av spontanabortene). Den skadelige effekten av en for tidlig økning i LH er assosiert med for tidlig gjenopptakelse av den andre meiotiske delingen og eggløsning av et umodent egg, samt med induksjon av androgenproduksjon av thecaceller sammen med nedsatt endometrieopptak under påvirkning av gestageninsuffisiens. Imidlertid gir ikke en foreløpig reduksjon av preovulatoriske LH-nivåer med gonadotropinfrigjørende hormonagonister uten ytterligere tiltak som tar sikte på å forlenge påfølgende graviditet den forventede reduksjonen i hyppigheten av spontanaborter.
Gullstandarden for diagnostisering av NLF er histologisk undersøkelse av materiale hentet fra endometriebiopsi i den andre fasen av syklusen over 2 menstruasjonssykluser.
Diagnostisering av andre årsaker til eggløsningsdysfunksjon, som hyperprolaktinemi, hypotyreose, funksjonelt overskudd av androgener (eggstokk eller binyre), må ledsages av foreskrivelse av passende behandling.
Diagnostikk
Historie og fysisk undersøkelse
- Anamnese. Faktorer å vurdere: sen menarche, uregelmessig menstruasjonssyklus (oligomenoré, amenoré, plutselig vektøkning, vekttap, infertilitet, vanemessige tidlige spontanaborter).
- Undersøkelse: kroppstype, høyde, kroppsvekt, hirsutisme, alvorlighetsgrad av sekundære seksuelle karakteristika, tilstedeværelse av striae, undersøkelse av melkekjertler for galaktoré.
- Funksjonelle diagnostiske tester: måling av endetarmstemperatur i løpet av 3 menstruasjonssykluser.
Spesielle forskningsmetoder
- Hormonell studie:
- i den første fasen av menstruasjonssyklusen (7.–8. dag) – bestemmelse av innholdet av FSH, LH, prolaktin, TSH, testosteron, 17-hydroksyprogesteron (17-OP), DHEAS;
- i den andre fasen av menstruasjonssyklusen (21–22 dager) – bestemmelse av progesteroninnhold (normative indikatorer for progesteronnivåer er svært variable, metoden kan ikke brukes uten å ta hensyn til andre faktorer).
- Ultralyd:
- i den første fasen av menstruasjonssyklusen (5.–7. dag) – diagnose av endometriepatologi, polycystiske eggstokker;
- i den andre fasen av menstruasjonssyklusen (20–21 dager) – måling av tykkelsen på endometriet (normal 10–11 mm, korrelerer med innholdet av progesteron).
- En endometriebiopsi for å bekrefte endometriumsvulst (NLF) utføres 2 dager før forventet menstruasjon (på den 26. dagen med en 28-dagers syklus). Denne metoden brukes i tilfeller der diagnosen er uklar. For å studere endringer i endometriet i den såkalte «implantasjonsvinduet»-perioden, utføres en biopsi på den 6. dagen etter eggløsning.
Behandling
Ved diagnostisering av NLF (ifølge rektaltemperaturdiagrammer er varigheten av 2. fase mindre enn 11 dager, en trinnvis økning i temperatur observeres, utilstrekkelig sekretorisk transformasjon av endometrium i henhold til endometriebiopsidata, lave nivåer av progesteron i blodserumet), er det nødvendig å identifisere årsaken til slike lidelser.
Hvis NLF er ledsaget av hyperprolaktinemi, utføres MR av hjernen. En alternativ metode er røntgen av hodeskallen (sella turcica-regionen).
Det første stadiet ved hyperprolaktinemi er å utelukke hypofyseadenom, som krever kirurgisk behandling. Ved fravær av signifikante endringer anses hyperprolaktinemi som funksjonell, og bromokriptinbehandling foreskrives for å normalisere prolaktinnivåene. Startdosen bromokriptin er 1,25 mg/dag i 2 uker, og etter overvåking av prolaktinnivåene, hvis indikatorene ikke normaliseres, økes dosen til 2,5 mg/dag. Ved en signifikant økning i prolaktinnivåene er startdosen 2,5 mg/dag. Hvis graviditet oppstår, bør bromokriptin seponeres.
Hvis hypotyreose oppdages, bestemmes arten av skjoldbruskkjertelpatologien sammen med en endokrinolog. Uansett er daglig natriumlevothyroksinbehandling indisert, dosen velges individuelt inntil TSH-nivået er normalisert. Hvis graviditet oppstår, bør behandlingen med natriumlevothyroksin fortsette. Spørsmålet om hvorvidt det er tilrådelig å øke dosen i første trimester av svangerskapet avgjøres sammen med en endokrinolog etter å ha mottatt resultatene av en hormonundersøkelse (TSH-nivå, fritt tyroksin).
Korrigering av NLF utføres på en av to måter. Den første måten er eggløsningsstimulering, den andre måten er erstatningsterapi med progesteronpreparater.
Det første behandlingsalternativet er eggløsningsstimulering med klomifensitrat. Denne behandlingsmetoden er basert på det faktum at de fleste lutealfaseforstyrrelser oppstår i follikulærfasen av syklusen. Konstant reduserte progesteronnivåer i 2. fase er en konsekvens av nedsatt follikulogenese i 1. fase av syklusen. Denne lidelsen vil bli korrigert med større suksess ved lave doser klomifensitrat i tidlig follikulærfase enn ved å foreskrive progesteron i 2. fase av syklusen.
I den første syklusen er dosen klomifensitrat 50 mg/dag fra den femte til den niende dagen i menstruasjonssyklusen. Effektiviteten overvåkes ved hjelp av rektal temperaturmåling, progesteronnivåmålinger i den andre fasen av syklusen eller dynamisk ultralyd. Hvis det ikke er tilstrekkelig effekt i den andre syklusen med eggløsningsstimulering, bør dosen klomifensitrat økes til 100 mg/dag fra den femte til den niende dagen i syklusen. Maksimal mulig dose i den tredje syklusen med eggløsningsstimulering er 150 mg/dag. En slik doseøkning er kun mulig hvis legemidlet tolereres godt (ingen intense smerter i nedre del av magen og korsryggen og ingen andre tegn på ovariell hyperstimulering).
Det andre behandlingsalternativet: erstatningsterapi med progesteronpreparater, som fremmer full sekretorisk transformasjon av endometriet, noe som gir den nødvendige effekten hos pasienter med habituell spontanabort med bevart eggløsning. I tillegg har det de siste årene blitt fastslått at administrering av progesteronpreparater ikke bare har en hormonell, men også en immunmodulerende effekt, som undertrykker avstøtningsreaksjoner fra immunkompetente celler i endometriet. Spesielt er en lignende effekt beskrevet for dihydrogesteron i en dose på 20 mg/dag. For erstatningsterapi brukes dydrogesteron i en dose på 20 mg/dag oralt eller mikronisert progesteron vaginalt i en dose på 200 mg/dag. Behandlingen utføres den andre dagen etter eggløsning (dagen etter økningen i rektal temperatur) og fortsetter i 10 dager. Hvis graviditet oppstår, bør behandlingen med progesteronpreparater fortsettes.
Moderne forskning har ikke bekreftet effektiviteten av humant koriongonadotropin i behandlingen av tilbakevendende spontanabort.
Ved hyperandrogenisme (ovariell eller binyrebarkgenere) hos pasienter med habituell spontanabort er medikamentell behandling indisert på grunn av androgeners effekt på fullstendig eggløsning og endometriets tilstand. Ved brudd på biosyntesen av binyreandrogener er deres viriliserende effekt på det kvinnelige fosteret mulig, derfor utføres steroidbehandling i fosterets interesse.
Hyperandrogenisme av eggstokkgenese (polycystiske eggstokker)
Anamnese, fysisk undersøkelse og resultater av spesielle undersøkelser
- Sykehistorie: sen menarche, menstruasjonsforstyrrelser som oligomenoré (vanligvis primær, sjeldnere sekundær). Svangerskap er sjeldne, vanligvis spontant avbrutt i første trimester, med lange perioder med infertilitet mellom svangerskapene.
- Undersøkelse: hirsutisme, kviser, strekkmerker, høy kroppsmasseindeks (valgfritt).
- Rektale temperaturdiagrammer: anovulatoriske sykluser veksler med sykluser med eggløsning og ikke-leveransen av fettlever.
- Hormonundersøkelse: høye testosteronnivåer, FSH- og LH-nivåer kan være forhøyede, LH/FSH-forholdet er større enn 3. Ultralyd: polycystiske eggstokker.
Behandling
Ikke-medikamentell behandling
Vekttap - kostholdsterapi, fysisk aktivitet.
Medikamentell behandling
- Orlistat i en dose på 120 mg til hvert hovedmåltid. Varigheten av kuren bestemmes under hensyntagen til effekt og toleranse.
- Foreløpig testosteronreduksjon med preparater som inneholder cyproteronacetat (2 mg) og EE (35 mcg) i 3 menstruasjonssykluser.
- Seponering av prevensjon, hormonell støtte i den andre fasen av syklusen (gestagenbehandling) - dydrogesteron i en dose på 20 mg/dag fra den 16. til den 25. dagen i menstruasjonssyklusen. Hvis det ikke er spontan eggløsning, gå videre til neste trinn.
- Stimulering av eggløsning med klomifensitrat med en startdose på 50 mg/dag fra 5. til 9. dag i menstruasjonssyklusen, samtidig behandling med gestagener (dydrogesteron med en dose på 20 mg/dag fra 16. til 25. dag i syklusen) og deksametason (0,5 mg).
- Ved fravær av graviditet økes dosen av klomifensitrat til 100–150 mg/dag ved administrering av gestagener i den andre fasen av syklusen og deksametason (0,5 mg). Det er fastslått at selv om deksametason bare reduserer nivået av binyrebarkandrogener, forekommer eggløsning og unnfangelse betydelig oftere ved behandling med klomifensitrat og deksametason enn ved bruk av klomifensitrat alene [12].
- Tre sykluser med eggløsningsstimulering utføres, hvoretter det anbefales en pause i tre menstruasjonssykluser med gestagenisk støtte og en beslutning om kirurgisk behandling ved bruk av laparoskopisk tilgang (kilereseksjon av eggstokkene, laserfordampning).
Videre behandling av pasienten
Graviditetshåndtering bør ledsages av gestagenisk støtte inntil 16 uker med svangerskap (dydrogesteron i en dose på 20 mg/dag eller mikronisert progesteron i en dose på 200 mg/dag). Deksametason foreskrives kun i første trimester av svangerskapet. Overvåking er obligatorisk for rettidig diagnose av istmisk-cervikal insuffisiens og om nødvendig kirurgisk korrigering.
Adrenal hyperandrogenisme (pubertal og postpubertal adrenogenital syndrom)
Adrenogenital syndrom (AGS) er en arvelig sykdom assosiert med en forstyrrelse i syntesen av hormoner i binyrebarken på grunn av skade på gener som er ansvarlige for syntesen av en rekke enzymsystemer. Sykdommen arves autosomalt recessivt med overføring av mutante gener fra begge foreldre, som er friske bærere.
I 90 % av tilfellene er adrenogenital syndrom forårsaket av mutasjoner i CYP21B-genet, noe som fører til en forstyrrelse i syntesen av 21-hydroksylase.
Anamnese, fysisk undersøkelse og resultater av spesielle undersøkelser
- Anamnese: sen menarche, noe forlenget menstruasjonssyklus, mulig oligomenoré, spontanaborter i første trimester, mulig infertilitet.
- Undersøkelse: kviser, hirsutisme, android kroppstype (brede skuldre, smalt bekken), klitorishypertrofi.
- Rektale temperaturdiagrammer: anovulatoriske sykluser veksler med sykluser med eggløsning og ikke-leveransen av fettlever.
- Hormonell test: høye nivåer av 17-OP, DHEAS.
- Ultralyd: eggstokkene er uendret.
Et patognomonisk tegn utenfor graviditet er en økning i konsentrasjonen av 17-OP i blodplasmaet.
For tiden brukes en test med ACTH til å diagnostisere den latente, ikke-klassiske formen for adrenal hyperandrogenisme. Synacthen brukes til denne testen - et syntetisk polypeptid som har egenskapene til endogen ACTH, dvs. det stimulerer de innledende fasene av syntesen av steroidhormoner fra kolesterol i binyrene.
Synacthen-test (en ACTH-analog): 1 ml (0,5 mg) synacthen injiseres subkutant i skulderen. Det opprinnelige innholdet av 17-OP og kortisol bestemmes først i en 9-timers blodplasmaprøve om morgenen. En kontrollblodprøve tas 9 timer etter injeksjonen for å bestemme nivået av 17-OP og kortisol. Bestemmelsesindeksen (D) beregnes deretter ved hjelp av formelen:
D = 0,052 × 17-OP + 0,005 × Kortisol/17-OP - 0,018 × Kortisol/17-OP
Hvis D-koeffisienten er mindre enn eller lik 0,069, indikerer dette fravær av binyrehyperandrogenisme. Hvis D-koeffisienten er mer enn 0,069, bør det vurderes at hyperandrogenisme er forårsaket av en dysfunksjon i binyrene.
Medikamentell behandling
Hovedbehandlingen for hyperandrogenisme på grunn av 21-hydroksylase-mangel er glukokortikoider, som brukes til å undertrykke overflødig androgensekresjon.
Videre behandling av pasienten
På grunn av den viriliserende effekten av mors androgener på fosteret, med en etablert diagnose av adrenal hyperandrogenisme, foreskrives behandling med deksametason med en initial dose på 0,25 mg før graviditet og fortsettes med en individuelt valgt dose (fra 0,5 til 1 mg) gjennom hele graviditeten. Hos en kvinne med habituell spontanabort som lider av adrenal hyperandrogenisme, er det upassende å avbryte behandlingen, siden hyppigheten av spontanaborter uten behandling når 14 %, med fortsettelse - 9 %.
Med tanke på at pasienter med adrenogenitalt syndrom kan overføre dette genet til fosteret, er det nødvendig å utføre prenatal diagnostikk: i uke 17–18 av svangerskapet foreskrives en blodprøve for å bestemme innholdet av 17-OP hos moren. Hvis nivået av hormonet i blodet økes, bestemmes konsentrasjonen i fostervannet. Hvis innholdet av 17-OP i fostervannet økes, diagnostiseres adrenogenitalt syndrom hos fosteret. Dessverre er det umulig å bestemme alvorlighetsgraden av adrenogenitalt syndrom (mild eller alvorlig saltsløsende form) ut fra nivået av 17-OP i fostervannet. Spørsmålet om å opprettholde svangerskapet i denne situasjonen avgjøres av foreldrene.
Hvis barnets far er bærer av genet for adrenogenitalt syndrom, og det har vært tilfeller av barn født med dette syndromet i familien, får pasienten, selv uten adrenal hyperandrogenisme, deksametason av hensyn til fosteret (for å forhindre virilisering av det kvinnelige fosteret) i en dose på 20 mcg/kg kroppsvekt, maksimalt 1,5 mg/dag fordelt på 2–3 doser etter måltider. Ved 17–18 uker, etter å ha bestemt fosterets kjønn og uttrykket av genet for adrenogenitalt syndrom (basert på resultatene av fostervannsprøve), fortsettes behandlingen til slutten av svangerskapet hvis fosteret er en jente med adrenogenitalt syndrom. Hvis fosteret er en gutt eller en jente som ikke er bærer av genet for adrenogenitalt syndrom, kan deksametason seponeres.
Hvis en kvinne med habituell spontanabort lider av binyrehyperandrogenisme, utføres deksametasonbehandling gjennom hele svangerskapet og avsluttes først etter fødselen. På den tredje dagen etter fødselen reduseres deksametasondosen gradvis (med 0,125 mg hver tredje dag) inntil fullstendig seponering i postpartumperioden.
Hyperandrogenisme av blandet genese (eggstokk og binyre)
Anamnese, fysisk undersøkelse og resultater av spesielle undersøkelser
- Anamnese: sen menarche, menstruasjonsforstyrrelser som oligomenoré (vanligvis primær, sjeldnere sekundær), amenoré, mulige skader, hjernerystelse. Svangerskap er sjeldne, vanligvis spontant avbrutt i første trimester, lange perioder med infertilitet mellom svangerskapene.
- Fysisk undersøkelse: hirsutisme, akne, striae, acanthosis nigricans, høy kroppsmasseindeks, hypertensjon.
- Rektale temperaturdiagrammer: anovulatoriske sykluser veksler med sykluser med eggløsning og ikke-leveransen av fettlever.
- Hormonundersøkelse: høye testosteronnivåer, FSH- og LH-nivåer kan være forhøyede, LH/FSH-forhold større enn 3, høye DHEAS- og 17-OP-nivåer, hyperprolaktinemi kan være tilstede.
- Ultralyd: polycystiske eggstokker.
- Elektroencefalografi: endringer i hjernens bioelektriske aktivitet.
- Hyperinsulinemi, forstyrrelser i lipidmetabolismen (høyt kolesterol, lipoproteiner med lav tetthet og lipoproteiner med svært lav tetthet), redusert glukosetoleranse eller forhøyede blodsukkernivåer.
Behandling
Ikke-medikamentell behandling
Vekttap (lavkaloridiett, fysisk aktivitet).
Medikamentell behandling
Det første stadiet - i nærvær av insulinresistens, anbefales det å foreskrive metformin i en daglig dose på 1000-1500 mg for å øke insulinfølsomheten.
Den andre fasen - ved alvorlige menstruasjonsforstyrrelser og høye testosteronnivåer, anbefales det å foreskrive legemidler med antiandrogen effekt som inneholder cyproteronacetat (2 mg) og etinyløstradiol (35 mcg) i 3 måneder.
Det tredje stadiet er stimulering av eggløsning etterfulgt av gestagenisk støtte (skjemaet er beskrevet ovenfor) og inntak av deksametason i en daglig dose på 0,25–0,5 mg.
Ved hyperprolaktinemi og hypotyreose bør passende medikamentkorrigering utføres i eggløsningsstimuleringssykluser. Hvis graviditet oppstår, bør bromokriptin seponeres og levotyroksin fortsettes.
Hvis eggløsningsstimulering er ineffektiv, bør spørsmålet om forskrivning av direkte eggløsningsindusere, og om kirurgisk behandling av polycystiske eggstokker eller in vitro-fertilisering er tilrådelig, avgjøres.
Videre behandling av pasienten
Hos pasienter med metabolsk syndrom er graviditet ofte komplisert av arteriell hypertensjon, nefropati, hyperkoagulasjon, og i den forbindelse er det nødvendig å overvåke blodtrykket, ta hemostasiogram fra de tidlige stadiene av svangerskapet og korrigere oppståtte lidelser (om nødvendig) med antihypertensive legemidler, platehemmere og antikoagulantia. Gestageniske legemidler foreskrives inntil 16 ukers svangerskap - didrogesteron i en dose på 20 mg/dag eller mikronisert progesteron i en dose på 200 mg/dag i 2 doser.
Alle kvinner med hyperandrogenisme representerer en risikogruppe for utvikling av istmisk-cervikal insuffisiens. Overvåking av livmorhalsens tilstand bør utføres fra 16. svangerskapsuke, om nødvendig - kirurgisk korreksjon av istmisk-cervikal insuffisiens.
Immunologiske årsaker til habituell spontanabort
Det er for tiden kjent at omtrent 80 % av alle tidligere uforklarlige tilfeller av gjentatte aborter (etter å ha utelukket genetiske, anatomiske og hormonelle årsaker) er assosiert med immunforstyrrelser. Man skille mellom autoimmune og alloimmune lidelser, som fører til habetentlig spontanabort.
I autoimmune prosesser blir immunsystemets eget vev gjenstand for aggresjon, dvs. immunresponsen rettes mot dets egne antigener. I denne situasjonen lider fosteret sekundært som følge av skade på morens vev.
Ved alloimmune lidelser er en kvinnes immunrespons rettet mot embryonale/føtale antigener mottatt fra faren og som potensielt er fremmede for morens kropp.
Autoimmune lidelser som oftest forekommer hos pasienter med habituell spontanabort inkluderer tilstedeværelsen av antifosfolipid-, antityreoidea- og antinukleære autoantistoffer i serum. Det er derfor fastslått at 31 % av kvinner med habituell spontanabort utenfor graviditet har autoantistoffer mot tyreoglobulin og tyreoideaperoksidase (tyreoideamikrosomale [tyreoideaperoksidase] autoantistoffer). I disse tilfellene øker risikoen for spontanabort i første trimester av svangerskapet til 20 %. Ved habituell spontanabort indikerer tilstedeværelsen av antinukleære og antityreoidea-antistoffer behov for ytterligere undersøkelse for å identifisere den autoimmune prosessen og bekrefte diagnosen.
Antifosfolipidsyndrom (APS) er fortsatt en generelt anerkjent autoimmun tilstand som fører til embryo-/fosterdød.
Alloimmune lidelser
For tiden inkluderer alloimmune prosesser som fører til fosteravstøtning tilstedeværelsen av et økt (mer enn 3) antall vanlige antigener i det store histokompatibilitetskomplekssystemet hos ektefeller (ofte observert i blodsekteskap); lave nivåer av blokkerende faktorer i mors serum; økte nivåer av naturlige dreperceller (NK-celler CD56, CD16) i endometrium og perifert blod hos mor både utenfor og under graviditet; høye konsentrasjonsnivåer av en rekke cytokiner i endometrium og blodserum, spesielt γ-interferon, tumornekrosefaktor a, interleukiner-1 og 2.
For tiden studeres alloimmune faktorer som fører til tidlige svangerskapstap og måter å korrigere disse tilstandene på. Det er ingen enighet om behandlingsmetodene. Ifølge noen forskere gir ikke aktiv immunisering med donorlymfocytter en signifikant effekt, mens andre forfattere beskriver en signifikant positiv effekt med slik immunisering og behandling med immunglobuliner.
For tiden er progesteron et av de immunmodulerende midlene tidlig i svangerskapet. Spesielt har studier vist rollen til dydrogesteron i en daglig dose på 20 mg hos kvinner med habituell spontanabort i første trimester av svangerskapet med et økt nivå av CD56-celler i endometriet.
 [ 11 ], [ 12 ], [ 13 ], [ 14 ], [ 15 ], [ 16 ]
[ 11 ], [ 12 ], [ 13 ], [ 14 ], [ 15 ], [ 16 ]
Genetisk bestemte trombofilier
Følgende former for genetisk bestemte trombofilier anses å være trombofile tilstander under graviditet som fører til habituell spontanabort.
- Antitrombin III-mangel.
- Faktor V-mutasjon (Leiden-mutasjon).
- Protein C-mangel.
- Protein S-mangel.
- Protrombin-genmutasjon G20210A.
- Hyperhomocysteinemi.
Undersøkelse for å identifisere sjeldne årsaker til trombofili er nødvendig i tilfeller der det var:
- familiehistorie - tromboembolisme før fylte 40 år hos slektninger;
- pålitelige episoder med venøs og/eller arteriell trombose før fylte 40 år;
- tilbakevendende trombose hos pasienten og nærmeste slektninger;
- tromboemboliske komplikasjoner under graviditet og etter fødsel ved bruk av hormonell prevensjon;
- gjentatte graviditetstap, dødfødsler, intrauterin veksthemming, morkakeløsning;
- tidlig debuterende preeklampsi, HELLP-syndrom.
Smittsomme årsaker til vanemessig spontanabort
Infeksjonsfaktorens rolle som årsak til habituell spontanabort er for tiden mye omdiskutert. Det er kjent at primærinfeksjon i de tidlige stadiene av svangerskapet kan forårsake skade på embryoet som er uforenlig med liv, noe som fører til sporadisk spontanabort. Sannsynligheten for reaktivering av infeksjonen samtidig med gjentatte graviditetstab er imidlertid ubetydelig. I tillegg er det for tiden ikke funnet mikroorganismer som fremkaller habituell spontanabort. Studier de siste årene har vist at de fleste kvinner med habituell spontanabort og kronisk endometritt har en forekomst av 2–3 eller flere typer obligate anaerobe mikroorganismer og virus i endometriet.
Ifølge VM Sidelnikova et al. ble diagnosen kronisk endometritt utenfor graviditet histologisk bekreftet hos kvinner som led av habituell spontanabort i 73,1 % av tilfellene, og i 86,7 % ble det observert persistens av opportunistiske mikroorganismer i endometriet, noe som absolutt kan være årsaken til aktivering av immunopatologiske prosesser. Blandet persisterende virusinfeksjon (herpes simplex-virus, Coxsackie A, Coxsackie B, enterovirus 68–71, cytomegalovirus) finnes hos pasienter med habituell spontanabort betydelig oftere enn hos kvinner med normal obstetrisk historie. K. Kohut et al. (1997) viste at prosentandelen av inflammatoriske forandringer i endometriet og decidualvevet hos pasienter med primær tilbakevendende spontanabort er betydelig høyere enn hos kvinner etter spontanabort med en historie med minst én fullbåren fødsel.
Bakteriell og viral kolonisering av endometriet skyldes vanligvis immunsystemets og kroppens uspesifikke beskyttende krefter (komplementsystemet, fagocytose) manglende evne til å eliminere smittestoffet fullstendig, og samtidig er spredningen begrenset av aktivering av T-lymfocytter (T-hjelpere, naturlige drepere) og makrofager. I alle de ovennevnte tilfellene oppstår det en persistens av mikroorganismer, karakterisert ved at mononukleære fagocytter, naturlige drepere, T-hjelpere, som syntetiserer forskjellige cytokiner, til stedet for kronisk betennelse tiltrekkes. Tilsynelatende forhindrer en slik tilstand av endometriet dannelsen av lokal immunsuppresjon i preimplantasjonsperioden, noe som er nødvendig for å danne en beskyttende barriere og forhindre avstøting av et halvfremmed foster.
I denne forbindelse bør kvinner med habituell spontanabort diagnostiseres med kronisk endometritt før graviditet. For å etablere eller utelukke denne diagnosen utføres en endometriebiopsi på 7.-8. dag i menstruasjonssyklusen med histologisk undersøkelse, PCR og bakteriologisk undersøkelse av materialet fra livmorhulen. Ved bekreftelse av diagnosen behandles kronisk endometritt i henhold til standarder for behandling av inflammatoriske sykdommer i bekkenorganene.

