Medisinsk ekspert av artikkelen
Nye publikasjoner
Ikke-tuberkuløse mykobakterier
Sist anmeldt: 04.07.2025

Alt iLive-innhold blir gjennomgått med medisin eller faktisk kontrollert for å sikre så mye faktuell nøyaktighet som mulig.
Vi har strenge retningslinjer for innkjøp og kun kobling til anerkjente medieområder, akademiske forskningsinstitusjoner og, når det er mulig, medisinsk peer-evaluerte studier. Merk at tallene i parenteser ([1], [2], etc.) er klikkbare koblinger til disse studiene.
Hvis du føler at noe av innholdet vårt er unøyaktig, utdatert eller ellers tvilsomt, velg det og trykk Ctrl + Enter.
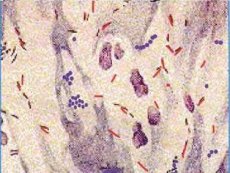
Ikke-tuberkuløse mykobakterier er uavhengige arter, utbredt i miljøet som saprofytter, som i noen tilfeller kan forårsake alvorlige sykdommer - mykobakteriose. De kalles også miljømykobakterier, forårsakende agenser for mykobakteriose, opportunistiske og atypiske mykobakterier. En betydelig forskjell mellom ikke-tuberkuløse mykobakterier og Mycobacterium tuberculosis-komplekset er at de praktisk talt ikke overføres fra person til person.
Ikke-tuberkuløse mykobakterier er delt inn i fire grupper basert på et begrenset antall egenskaper: veksthastighet, pigmentdannelse, kolonimorfologi og biokjemiske egenskaper.
1. gruppe - saktevoksende fotokromogene (M. kansasii, etc.). Hovedtrekket ved representanter for denne gruppen er utseendet av pigment i lyset. De danner kolonier fra S- til RS-former, inneholder karotenkrystaller som farger dem gule. Veksthastigheten er fra 7 til 20 dager ved 25, 37 og 40 °C, katadasepositive.
M. kansasii er gule basiller som lever i vann og jord og som oftest påvirker lungene. Disse bakteriene kan identifiseres ved sin store størrelse og korsformede arrangement. En viktig manifestasjon av infeksjoner forårsaket av M. kansasii er utviklingen av spredt sykdom. Hud- og bløtvevsskader, utvikling av tenosynovitt, osteomyelitt, lymfadenitt, perikarditt og urogenitale infeksjoner er også mulige.
2. gruppe - saktevoksende skotokromogene (M. scrofulaceum, M. matmoense, M. gordonae, etc.). Mikroorganismer danner gule kolonier i mørket og oransje eller rødlige kolonier i lyset, vanligvis S-formede kolonier, vokser ved 37 °C. Dette er den mest tallrike gruppen av ikke-tuberkuløse mykobakterier. De er isolert fra forurensede vannforekomster og jord og har lav patogenitet for mennesker og dyr.
M. scrofulaceum (fra engelsk scrofula - scrofula) er en av hovedårsakene til cervikal lymfadenitt hos barn under 5 år. Ved alvorlige samtidige sykdommer kan de forårsake skade på lunger, bein og bløtvev. I tillegg til vann og jord har mikrober blitt isolert fra rå melk og andre meieriprodukter.
M. maimoense er mikroaerofiler som danner gråhvite, glatte, skinnende, ugjennomsiktige, kuppelformede, runde kolonier.
Primære isolater vokser svært sakte ved 22–37 °C. Eksponering for lys forårsaker ikke pigmentproduksjon. Om nødvendig kan eksponeringen fortsette i opptil 12 uker. Hos mennesker forårsaker de kronisk lungesykdom.
M. gordonae er de vanligste anerkjente saprofyttene, skotokromogenene i vann fra springen, og forårsaker mykobakteriose ekstremt sjelden. I tillegg til vann (kjent som M. aquae), isoleres de ofte fra jord, mageskylling, bronkiale sekresjoner eller annet materiale fra pasienter, men i de fleste tilfeller er de ikke-patogene for mennesker. Samtidig er det rapportert om tilfeller av hjernehinnebetennelse, peritonitt og hudlesjoner forårsaket av denne typen mykobakterier.
Gruppe 3 - saktevoksende ikke-kromogene mykobakterier (M. avium-kompleks, M. gaslri M. terrae-kompleks, etc.). De danner fargeløse S- eller SR- og R-former av kolonier, som kan ha lysegule og kremfargede nyanser. De isoleres fra syke dyr, vann og jord.
M. avium - M. inlracellulare er kombinert til ett M. avium-kompleks, siden deres interartsdifferensiering byr på visse vanskeligheter. Mikroorganismer vokser ved 25–45 °C, er patogene for fugler, mindre patogene for storfe, griser, sauer og hunder, og er ikke patogene for marsvin. Oftest forårsaker disse mikroorganismene lungelesjoner hos mennesker. Lesjoner i hud, muskelvev og skjelettsystem, samt spredte former for sykdommer, er beskrevet. De er blant de årsakende agensene til opportunistiske infeksjoner som kompliserer ervervet immunsviktsyndrom (AIDS). M. avium-underarten paratuberkulose er årsaken til Jones sykdom hos storfe og muligens Crohns sykdom (en kronisk inflammatorisk sykdom i mage-tarmkanalen) hos mennesker. Mikroben finnes i kjøtt, melk og avføring fra infiserte kyr, og finnes også i vann og jord. Standard vannrensemetoder inaktiverer ikke denne mikroben.
M. xenopi forårsaker lungeskader hos mennesker og spredte former for sykdom assosiert med AIDS. De er isolert fra frosker av slekten Xenopus. Bakteriene danner små, glatte, skinnende, ikke-pigmenterte kolonier som deretter blir knallgule. Termofile vokser ikke ved 22 °C og vokser godt ved 37 og 45 °C. Ved bakterioskopi ser de ut som veldig tynne stenger, avsmalnende i den ene enden og arrangert parallelt med hverandre (som et stakittgjerde). De er ofte isolert fra kaldt og varmt vann fra springen, inkludert drikkevann lagret i sykehusreservoarer (nosokomiale utbrudd). I motsetning til andre opportunistiske mykobakterier er de følsomme for de fleste antituberkulosemedisiner.
M. ukerans er det etiologiske agens for mykobakteriell kutan N (Buruli-sår), vokser bare ved 30–33 °C, og kolonivekst observeres først etter 7 uker. Patogenet frigjøres også når mus blir infisert i pulpa på poten. Denne sykdommen er vanlig i Australia og Afrika. Kilden til infeksjon er det tropiske miljøet og BCG-vaksinasjon mot denne mykobakteriosen.
Gruppe 4 - hurtigvoksende mykobakterier (M. fortuitum-kompleks, M. phlei, M. xmegmatis, etc.). Veksten deres observeres i form av R- eller S-formkolonier i 1-2 til 7 dager. De finnes i vann, jord, kloakk og er representanter for den normale mikrofloraen i menneskekroppen. Bakterier i denne gruppen isoleres sjelden fra patologisk materiale fra pasienter, men noen av dem har klinisk betydning.
M. fortuitum-komplekset omfatter M. fortuitum og M. chcionae, som består av underarter. De forårsaker disseminerte prosesser, hud- og postoperative infeksjoner, samt lungesykdommer. Mikrober i dette komplekset er svært resistente mot antituberkulosemedisiner.
M. smegmatis er en representant for normal mikroflora, isolert fra smegma hos menn. Den vokser godt ved 45 °C. Som årsak til menneskelige sykdommer er den nummer to blant hurtigvoksende mykobakterier etter M. fortuitum-komplekset. Den påvirker hud og bløtvev. Tuberkulosepatogener må differensieres fra M. smegmatis ved undersøkelse av urin.
Mykobakteriose er oftest forårsaket av representanter for gruppe 3 og 1.
Epidemiologi av mykobakteriose
De forårsakende agensene for mykobakteriose er utbredt i naturen. De kan finnes i jord, støv, torv, gjørme, elvevann, dammer og svømmebassenger. De finnes i flått og fisk, forårsaker sykdommer hos fugler, ville og husdyr, og er representanter for den normale mikrofloraen i slimhinnene i øvre luftveier og urogenitaltrakt hos mennesker. Infeksjon med ikke-tuberkuløse mykobakterier skjer fra miljøet gjennom luftbåren overføring, kontakt med hudskader, samt gjennom mat og vann. Overføring av mikroorganismer fra person til person er uvanlig. Disse er opportunistiske bakterier, så en reduksjon i makroorganismens resistens og dens genetiske predisposisjon er av stor betydning i utviklingen av sykdommen. Granulomer dannes i de berørte områdene. I alvorlige tilfeller er fagocytosen ufullstendig, bakteriemien er uttalt, og makrofager fylt med ikke-tuberkuløse mykobakterier og som ligner spedalskhetsceller oppdages i organene.
Symptomer på mykobakteriose
Symptomene på mykobakteriose er varierte. Luftveiene er oftest påvirket. Symptomene på lungepatologi ligner på de ved tuberkulose. Det er imidlertid hyppige tilfeller av ekstrapulmonal lokalisering av prosessen som involverer hud og subkutant vev, såroverflater, lymfeknuter, urogenitale organer, bein og ledd, samt hjernehinnene. Organlesjoner kan begynne både akutt og latent, men fortsetter nesten alltid alvorlig,
Utvikling av en blandet infeksjon er også mulig; i noen tilfeller kan de være årsaken til utviklingen av en sekundær endogen infeksjon.
Mikrobiologisk diagnostikk av mykobakteriose
Hovedmetoden for å diagnostisere mykobakteriose er bakteriologisk. Materialet for studien tas basert på patogenesen og kliniske manifestasjoner av sykdommen. Først avgjøres spørsmålet om den isolerte renkulturen tilhører de forårsakende agensene for tuberkulose eller ikke-tuberkuløse mykobakterier. Deretter brukes en serie studier for å fastslå typen mykobakterier, graden av virulens og Runyon-gruppen. Primær identifikasjon er basert på egenskaper som veksthastighet, evne til å danne pigment, kolonimorfologi og evne til å vokse ved forskjellige temperaturer. For å identifisere disse egenskapene er det ikke nødvendig med ekstra utstyr eller reagenser, så de kan brukes i grunnleggende laboratorier ved tuberkuloseapotek. Endelig identifikasjon (referanseidentifikasjon) ved hjelp av komplekse biokjemiske studier utføres i spesialiserte moratorier ved vitenskapelige institusjoner. I de fleste tilfeller foretrekkes identifikasjon av dem basert på biokjemiske fakta, da moderne molekylærgenetiske metoder er arbeidskrevende, har mange forberedende stadier, krever spesialutstyr og er dyre. Bestemmelse av følsomhet for antibiotika er av stor betydning for behandlingen. Kriteriet for samtidig forekomst av kliniske, radiologiske og laboratoriedata og isolering av renkultur av ikke-tuberkuløse mykobakterier, samt gjennomføring av flere dynamiske studier er av avgjørende betydning for diagnosen mykobakteriose.
Av tilleggsvikt i diagnostikk er bestemmelse av antiteser ved bruk av RNGA, RP, immunelektroforese, RNIF og ELISA, samt utførelse av hudallergitester med sensitiner.
Behandling og spesifikk forebygging av mykobakteriose
Alle typer ikke-tuberkuløse mykobakterier, med unntak av M. xenopi, er resistente mot isoniazid, streptomycin og tiosemikarbazoner. Behandling av mykobakteriose med antituberkulose- og antibakterielle legemidler bør være langvarig (12–13 måneder) og kombinert. Det er vanligvis ineffektivt ved MAC-infeksjoner og sykdommer forårsaket av hurtigvoksende mykobakterier. I noen tilfeller brukes kirurgisk behandling. Legemidler for spesifikk forebygging av mykobakteriose er ikke utviklet.


 [
[