Medisinsk ekspert av artikkelen
Nye publikasjoner
Fibroelastose
Sist anmeldt: 05.07.2025

Alt iLive-innhold blir gjennomgått med medisin eller faktisk kontrollert for å sikre så mye faktuell nøyaktighet som mulig.
Vi har strenge retningslinjer for innkjøp og kun kobling til anerkjente medieområder, akademiske forskningsinstitusjoner og, når det er mulig, medisinsk peer-evaluerte studier. Merk at tallene i parenteser ([1], [2], etc.) er klikkbare koblinger til disse studiene.
Hvis du føler at noe av innholdet vårt er unøyaktig, utdatert eller ellers tvilsomt, velg det og trykk Ctrl + Enter.
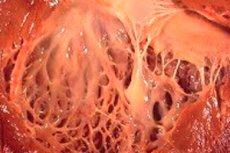
I medisin refererer begrepet «fibroelastose» til endringer i kroppens bindevev som dekker overflaten av indre organer og blodårer, forårsaket av en forstyrrelse i veksten av elastiske fibre. Samtidig observeres fortykkelse av organveggene og deres strukturer, noe som nødvendigvis påvirker funksjonen til vitale systemer i kroppen, spesielt det kardiovaskulære og respiratoriske systemet. Dette fører igjen til en forverring av pasientens velvære, spesielt under fysisk anstrengelse, noe som påvirker livskvaliteten og -varigheten.
Epidemiologi
Generelt kan sykdommer ledsaget av endringer i bindevevet, som resulterer i fortykkelse av membraner og skillevegger i indre organer, deles inn i to grupper: hjertefibroelastose og pulmonal fibroelastose. Hjertepatologi kan være både medfødt og ervervet; i pulmonalformen av sykdommen snakker vi om en ervervet sykdom.
Pulmonal fibroelastose begynner å utvikle seg i middelalderen (nærmere 55–57 år), selv om sykdommens opprinnelse i halvparten av tilfellene må søkes i barndommen. En "lett" periode er karakteristisk, når symptomene på sykdommen er fraværende. Samtidig har sykdommen ingen kjønnspreferanser og kan ramme både kvinner og menn i like stor grad. Denne ganske sjeldne patologien er preget av endringer i vevet i pleura og parenkymet (funksjonelle celler) i lungen, hovedsakelig i den øvre lungelappen. Siden etiologien og patogenesen til sykdommen fortsatt er uklar, klassifiseres sykdommen som en idiopatisk patologi. I følge medisinsk terminologi kalles den "pleeuroparenkymatøs fibroelastose". [ 1 ]
Hjertefibroelastose er et generalisert navn for en patologi i hjertemembranene, karakterisert ved fortykkelse og redusert funksjonalitet. Medfødte former av patologien er karakterisert ved diffus (utbredt) fortykkelse av hjertets indre membran. Dette er et tynt bindevev som kler hjertets hulrom (dets seksjoner) og danner klaffene.
Hos voksne pasienter diagnostiseres vanligvis en fokal form av sykdommen, når hjertets indre overflate ser ut til å være dekket av flekker av sterkere og tykkere vev (det kan inkludere ikke bare overgrodde fibre, men også trombotiske masser).
I halvparten av tilfellene av hjertefibroelastose blir ikke bare organveggen tykkere, men også klaffene (bikuspidal mitral mellom atrium og ventrikkel med samme navn, trikuspidal aorta mellom venstre ventrikkel og aorta, pulmonal mellom høyre ventrikkel og lungearterien). Dette kan igjen forstyrre klaffenes funksjon og forårsake innsnevring av arterieåpningen, som allerede er liten sammenlignet med andre hjertehulrom.
I medisinsk terminologi kalles endokardiell fibroelastose endokardiell fibroelastose (prenatal fibroelastose, endokardiell sklerose, føtal endokarditt, osv.). Men ganske ofte kan også det midterste muskellaget i hjertemembranen være involvert i prosessen. [ 2 ]
Anomalier i myokardstrukturen (hjertets muskellag, bestående av kardiomyocytter), genmutasjoner og alvorlige infeksjonsprosesser kan forårsake en vanlig form for fibroelastose, når ikke bare endokardiet, men også myokardiet er involvert i prosessen. Vanligvis forekommer dysplastiske prosesser i endokardiet, forårsaket av forskjellige årsaker, ved grensen for kontakt med muskelmembranen, noe som forstyrrer kontraktiliteten til dette laget. I noen tilfeller er det til og med innvekst av det indre laget i myokardiet, erstatning av kardiomyocytter med fibroblaster og fibre, noe som påvirker konduktiviteten til nerveimpulser og hjertets rytmiske arbeid.
Kompresjon av blodårene i tykkelsen av hjertemembranen av det fortykkede myokardiet forstyrrer ernæringen til myokardiet (myokardiskemi), som igjen kan føre til nekrose av vevet i hjertemuskelen.
Endokardiell fibroelastose med skade på hjertets myokard kalles subendokardiell eller endomyokardial fibroelastose.
I følge statistikk diagnostiseres fibroelastose i venstre hjertekammer i de fleste tilfeller av denne sjeldne sykdommen (bare 0,007 % av det totale antallet nyfødte), selv om prosessen i noen tilfeller også sprer seg til høyre hjertekammer og atrier, inkludert klaffene som skiller dem.
Hjertefibroelastose er ofte ledsaget av skade på store koronarkar, også dekket av bindevev. I voksen alder forekommer det ofte mot bakgrunn av progressiv vaskulær aterosklerose.
Sykdommen er oftere registrert i tropiske afrikanske land blant befolkninger med lav levestandard, noe som forenkles av dårlig ernæring, hyppige infeksjoner og visse matvarer og planter som konsumeres som mat.
Endokardiell fortykkelse observeres også i det siste stadiet av Löfflers fibroplastiske endokarditt, som hovedsakelig rammer middelaldrende menn. Patogenesen til denne sykdommen er også assosiert med smittsomme agenser som forårsaker utviklingen av alvorlig eosinofili, som er mer typisk for interne parasittinfeksjoner. I dette tilfellet begynner kroppens vev (primært hjertemuskelen og hjernen) å oppleve oksygenmangel (hypoksi). Til tross for likheten mellom symptomene på hjertefibroelastose og Löfflers fibrøse endokarditt, anser leger dem for å være helt forskjellige sykdommer.
Fører til fibroelastose
Fibroelastose refererer til endringer i bindevevet i vitale organer: hjertet og lungene, som er ledsaget av forstyrrelser i organfunksjonen og gjenspeiles i pasientens utseende og tilstand. Leger har visst om sykdommen i flere tiår. Fibroelastose i hjertets indre slimhinne (endokardiet) ble beskrevet tilbake på begynnelsen av 1700-tallet, og lignende endringer i lungene begynte å bli diskutert to og et halvt århundre senere. Legene har imidlertid ennå ikke kommet til en endelig enighet om årsakene til den patologiske proliferasjonen av bindevev.
Det er fortsatt uklart hva som egentlig forårsaker forstyrrelsen i vekst og utvikling av bindefibre. Men forskere identifiserer visse risikofaktorer for slike endringer, og anser dem som mulige (men ikke endelige) årsaker til sykdommen.
I patogenesen av pulmonal fibroelastose, som regnes som en sykdom hos modne mennesker, gis det derfor en spesiell rolle til tilbakevendende infeksiøse organlesjoner, som finnes hos halvparten av pasientene. Infeksjoner fremkaller betennelse i lungevevvet og pleura, og langvarig betennelse disponerer for fibrøs transformasjon.
Noen pasienter har fibroelastose i familien, noe som tyder på en arvelig predisposisjon. Uspesifikke autoantistoffer er funnet i kroppen deres, noe som fremkaller langvarige inflammatoriske prosesser med usikker etiologi.
Det finnes en oppfatning om at fibrøse forandringer i lungevevet kan være forårsaket av gastroøsofageal reflukssykdom. Selv om denne sammenhengen mest sannsynlig er indirekte, antas det også at risikoen for fibroelastose er høyere hos de som lider av hjerte- og karsykdommer eller lungetrombose.
Pulmonal fibroelastose hos ung og ungdom kan dukke opp under graviditet. Vanligvis er sykdommen skjult i omtrent 10 år eller mer, men den kan manifestere seg tidligere, muligens på grunn av økt belastning på den vordende morens kropp og hormonelle forandringer, men det finnes ingen eksakt forklaring ennå. Likevel ble et lignende bilde av sykdomsutviklingen observert hos 30 % av de undersøkte pasientene i reproduktiv alder.
Graviditet i seg selv kan ikke forårsake sykdommen, men det kan akselerere utviklingen av hendelser, noe som er veldig trist, fordi dødeligheten av sykdommen er svært høy, og forventet levealder med fibroelastose er kort.
I de fleste tilfeller kan hjertefibroelastose tilskrives barnesykdommer. Medfødt patologi oppdages i prenatalperioden hos et 4-7 måneder gammelt foster, men diagnosen kan først bekreftes etter at barnet er født. Flere mulige negative faktorer vurderes i patogenesen av denne sykdomsformen: smittsomme og inflammatoriske sykdommer hos moren som overføres til fosteret, abnormaliteter i utviklingen av hjertemembranene, nedsatt blodtilførsel til hjertevevet, genetiske mutasjoner, oksygenmangel.
Det antas at blant infeksjoner utgjør virus det største patogenetiske bidraget til utviklingen av hjertefibroelastose, fordi de er innebygd i kroppens celler, ødelegger dem og endrer vevets egenskaper. Fosterets udannede immunsystem kan ikke gi det beskyttelse mot disse patogenene, i motsetning til den vordende morens immunitet. Sistnevnte opplever kanskje ikke konsekvensene av en virusinfeksjon, mens hos fosteret kan en intrauterin infeksjon provosere frem forekomsten av ulike anomalier.
Noen forskere mener at den avgjørende rollen i patogenesen av den infeksiøse formen for fibroelastose spilles av en infeksjon som påvirker fosteret opptil 7 måneders alder. Senere kan den bare forårsake inflammatoriske hjertesykdommer (myokarditt, endokarditt).
Anomalier i utviklingen av hjertets membraner og ventiler kan provoseres av både den inflammatoriske prosessen og utilstrekkelige autoimmune reaksjoner, som et resultat av at cellene i immunsystemet begynner å angripe kroppens egne celler.
Genmutasjoner forårsaker unormal utvikling av bindevev, fordi gener inneholder informasjon om strukturen og oppførselen til proteinstrukturer (spesielt kollagen- og elastinproteiner).
Hypoksi og iskemi i hjertevevet kan være en konsekvens av unormal hjerteutvikling. I dette tilfellet snakker vi om sekundær fibroelastose, provosert av medfødte hjertefeil (CHD). Disse inkluderer slike anomalier som forårsaker obstruksjon (nedsatt åpenhet i hjertet og dets kar):
- stenose eller innsnevring av aorta nær ventilen,
- koarktasjon eller segmental innsnevring av aorta ved krysset mellom dens bue og nedadgående seksjon,
- atresi eller mangel på naturlig åpning i aorta,
- underutvikling av hjertevev (oftest venstre ventrikkel, sjeldnere høyre ventrikkel og atrier), noe som påvirker hjertets pumpefunksjon.
Det er en oppfatning at toksikose under graviditet også kan fungere som en predisponerende faktor for fibroelastose hos fosteret.
I den barselsperioden kan utviklingen av hjertefibroelastose fremmes av infeksjons- og inflammatoriske sykdommer i organmembranene, hemodynamiske forstyrrelser som følge av skader, vaskulær tromboembolisme, hjerteinfarktblødning, metabolske forstyrrelser (økt fibrindannelse, forstyrrelser i protein- og jernmetabolismen: amyloidose, hemokromatose). De samme årsakene forårsaker utviklingen av sykdommen hos voksne.
Patogenesen
Bindevev er et spesielt vev i menneskekroppen som er en del av nesten alle organer, men som ikke aktivt deltar i deres funksjoner. Bindevev tilskrives støttende og beskyttende funksjoner. Ved å danne et slags skjelett (rammeverk, stroma) og begrense organets funksjonelle celler, sikrer det dets endelige form og størrelse. Med tilstrekkelig styrke beskytter bindevevet også organcellene mot ødeleggelse og skade, forhindrer penetrering av patogener, og absorberer ved hjelp av spesielle makrofagceller foreldede strukturer: døde vevsceller, fremmede proteiner, avfallsblodkomponenter, etc.
Dette vevet kan kalles hjelpevev, fordi det ikke inneholder cellulære elementer som sikrer funksjonaliteten til ett eller annet organ. Likevel er dets rolle i kroppens liv ganske stor. Som en del av membranene i blodårene sikrer bindevevet sikkerheten og funksjonaliteten til disse strukturene, på grunn av hvilken ernæring og respirasjon (trofisme) av det omkringliggende vevet i kroppens indre miljø utføres.
Det finnes flere typer bindevev. Membranen som dekker de indre organene kalles løst bindevev. Det er en halvflytende, fargeløs substans som inneholder bølgete kollagenfibre og rette elastinfibre, mellom hvilke ulike typer celler er tilfeldig spredt. Noen av disse cellene (fibroblaster) er ansvarlige for dannelsen av fiberstrukturer, andre (endoteliocytter og mastceller) danner en gjennomskinnelig matrise av bindevev og produserer spesielle stoffer (heparin, histamin), andre (makrofager) sørger for fagocytose, etc.
Den andre typen fibervev er tett bindevev, som ikke inneholder et stort antall individuelle celler, som igjen er delt inn i hvitt og gult. Hvitt vev består av tettpakkede kollagenfibre (leddbånd, sener, periosteum), og gult vev består av kaotisk sammenflettede elastinfibre med inneslutninger av fibroblaster (del av leddbånd, membraner i blodårer, lunger).
Bindevev omfatter også: blod, fett, bein og brusk, men vi er ikke interessert i dem ennå, siden vi når vi snakker om fibroelastose, mener endringer i fiberstrukturer. Og elastiske og spenstige fibre finnes bare i løst og tett bindevev.
Syntesen av fibroblaster og dannelsen av bindevevsfibre fra dem reguleres på hjernenivå. Dette sikrer konstansen av dens egenskaper (styrke, elastisitet, tykkelse). Hvis syntesen og utviklingen av hjelpevev forstyrres på grunn av patologiske årsaker (antall fibroblaster øker, deres "oppførsel" endres), skjer det en spredning av sterke kollagenfibre eller en endring i veksten av elastiske (de forblir korte, vridde), noe som fører til en endring i egenskapene til organmembranen og noen indre strukturer dekket av bindevev. De får en større tykkelse enn nødvendig, blir tettere, sterkere og uelastiske, og ligner fibervev i leddbånd og sener, noe som krever stor innsats for å strekke.
Slikt vev strekker seg ikke godt, noe som begrenser organets bevegelser (automatiske rytmiske bevegelser av hjertet og blodårene, endringer i lungenes størrelse under innånding og utånding), derav forstyrrelser i blodtilførselen og luftveiene, noe som fører til oksygenmangel.
Faktum er at kroppens blodtilførsel skjer takket være hjertet, som fungerer som en pumpe, og to sirkulasjonskretser. Lungesirkulasjonen er ansvarlig for blodtilførsel og gassutveksling i lungene, hvorfra oksygen tilføres hjertet med blodstrømmen, og derfra til den systemiske sirkulasjonen og fordeles gjennom hele kroppen, noe som gir respirasjon til organer og vev.
Den elastiske membranen, som begrenser hjertemuskelens sammentrekning, reduserer hjertets funksjonalitet, som ikke pumper blod like aktivt, og med det oksygen. Ved fibroelastose i lungene svekkes ventilasjonen (osigenering), og det er tydelig at mindre oksygen begynner å komme inn i blodet, noe som selv med normal hjertefunksjon vil bidra til oksygenmangel (hypoksi) i vev og organer. [ 3 ]
Symptomer fibroelastose
Hjerte- og pulmonal fibroelastose er to typer sykdommer som er karakterisert av en forstyrrelse i fibersyntesen i bindevevet. De har ulik lokalisering, men begge er potensielt livstruende, ettersom de er assosiert med progressiv eller alvorlig hjerte- og respirasjonssvikt.
Pulmonal fibroelastose er en sjelden type interstitiell sykdom i dette viktige organet i luftveiene. Disse inkluderer kroniske patologier i lungeparenkymet med skade på alveolveggene (betennelse, forstyrrelse av strukturen og strukturen), det indre slimhinnen i lungekapillærene, etc. Fibroelastose regnes ofte som en spesiell sjelden form for progressiv lungebetennelse med en tendens til fibrøse forandringer i lunge- og pleuravevet.
Det er nesten umulig å oppdage sykdommen helt i begynnelsen, fordi den kanskje ikke minner om seg selv før om 10 år. Denne perioden kalles det klare intervallet. Utbruddet av patologiske forandringer som ennå ikke påvirker lungevolumet og gassutvekslingen, kan oppdages ved en tilfeldighet under en detaljert undersøkelse av lungene i forbindelse med en annen sykdom i luftveiene eller skade.
Sykdommen kjennetegnes av en langsom progresjon av symptomer, slik at de første manifestasjonene av sykdommen kan bli betydelig forsinket i tid fra dens debut. Symptomene intensiveres gradvis.
De første tegnene på sykdommen som det er verdt å være oppmerksom på er hoste og økende kortpustethet. Slike symptomer blir ofte en konsekvens av en tidligere luftveissykdom, slik at de kan være forbundet med forkjølelse og dens konsekvenser over lengre tid. Kortpustethet oppfattes ofte som en hjertesykdom eller aldersrelaterte forandringer. Tross alt diagnostiseres sykdommen hos personer som nærmer seg alderdom.
Både pasienter og leger som undersøker dem kan gjøre feil, noe som fører til sen oppdagelse av en farlig sykdom. Det er verdt å være oppmerksom på hosten, som er uproduktiv ved fibroelastose, men ikke stimuleres av mukolytika og slimløsende midler, men stoppes av hostestillende midler. En langvarig hoste av denne typen er et karakteristisk symptom på pulmonal fibroelastose.
Dyspné er forårsaket av progressiv respirasjonssvikt på grunn av fortykkelse av alveolveggene og pleura, en reduksjon i volum og antall alveolære hulrom i lungen (organets parenkym er synlig på røntgenbildet som en bikake). Symptomet intensiveres under påvirkning av fysisk anstrengelse, først betydelig, og deretter til og med liten. Etter hvert som sykdommen utvikler seg, forverres den, noe som forårsaker uførhet og død hos pasienten.
Progresjonen av fibroelastose er ledsaget av en forverring av den generelle tilstanden: hypoksi fører til svakhet og svimmelhet, kroppsvekten synker (anoreksi utvikler seg), neglefalangene endres til typen trommestikker, huden blir blek og får et sykelig utseende.
Halvparten av pasientene utvikler uspesifikke symptomer som pustevansker og brystsmerter, karakteristisk for pneumothorax (opphopning av gasser i pleurahulen). Denne anomalien kan også oppstå som følge av skader, primære og sekundære lungesykdommer, feil behandling, slik at den ikke kan diagnostiseres.
Hjertefibroelastose, samt patologien til bindevevsvekst i lungene, kjennetegnes av: blek hud, vekttap, svakhet, som ofte er paroksysmal, kortpustethet. Vedvarende subfebril temperatur uten tegn på forkjølelse eller infeksjon kan også observeres.
Mange pasienter opplever endringer i leverstørrelsen. Den øker i størrelse uten symptomer på dysfunksjon. Hevelse i ben, ansikt, armer og korsbeinsområdet er også mulig.
En karakteristisk manifestasjon av sykdommen anses å være økende sirkulasjonssvikt assosiert med hjerteforstyrrelser. I dette tilfellet diagnostiseres takykardi (økt hjertefrekvens, ofte kombinert med arytmi), kortpustethet (også i fravær av fysisk aktivitet), vevscyanose (blåaktig farging forårsaket av akkumulering av karboksyhemoglobin i blodet, dvs. en forbindelse av hemoglobin med karbondioksid på grunn av forstyrret blodstrøm og dermed gassutveksling).
I dette tilfellet kan symptomene oppstå enten umiddelbart etter fødselen av et barn med denne patologien, eller over en periode. Når eldre barn og voksne er rammet, oppstår tegn på alvorlig hjertesvikt vanligvis mot bakgrunn av en luftveisinfeksjon, som fungerer som en utløsende faktor. [ 4 ]
Fibroelastose hos barn
Hvis pulmonal fibroelastose er en sykdom hos voksne, ofte med opprinnelse i barndommen, men som ikke gjør seg kjent på lenge, oppstår ofte en lignende patologi i hjertets endokardium allerede før fødselen av barnet og påvirker livet hans fra de første øyeblikkene etter fødselen. Denne sjeldne, men alvorlige patologien er årsaken til utviklingen av vanskelig korrigert hjertesvikt hos spedbarn, hvorav mange dør innen 2 år. [ 5 ]
Endokardiell fibroelastose hos nyfødte er i de fleste tilfeller et resultat av patologiske prosesser som oppstår i babyens kropp i prenatal alder. Infeksjoner mottatt fra moren, genetiske mutasjoner, abnormaliteter i utviklingen av det kardiovaskulære systemet, arvelige metabolske sykdommer - alt dette, ifølge forskere, kan føre til endringer i bindevevet i hjertets membraner. Spesielt hvis et 4-7 måneder gammelt foster utsettes for to eller flere faktorer samtidig.
For eksempel gir en kombinasjon av abnormiteter i utviklingen av hjertet og koronarkarene (stenose, atresi, aortakoarktasjon, unormal utvikling av myokardceller, endokardsvakhet osv.), som bidrar til vevsiskemi, kombinert med en inflammatorisk prosess på grunn av infeksjon, barnet praktisk talt ingen sjanse for å overleve. Selv om organutviklingsdefekter fortsatt kan korrigeres raskt, kan progressiv fibroelastose bare bremses, men ikke kureres.
Vanligvis oppdages hjertefibroelastose hos fosteret allerede under graviditeten under ultralyddiagnostikk i andre eller tredje trimester. Ultralyd og ekkokardiografi i uke 20 til 38 viste hyperekogenisitet, noe som indikerer fortykkelse og kompaktering av endokardiet (vanligvis diffust, sjeldnere fokalt), en endring i hjertets størrelse og form (organet forstørres og tar form av en kule eller kule, de indre strukturene glattes gradvis ut). [ 6 ]
I 30–35 % av tilfellene ble fibroelastose oppdaget før 26 ukers svangerskap, i 65–70 % i den påfølgende perioden. Hos mer enn 80 % av nyfødte er fibroelastose kombinert med obstruktiv hjertefeil, dvs. at den er sekundær, til tross for tidlige stadier av oppdagelsen. Venstre ventrikkelhyperplasi ble oppdaget hos halvparten av de berørte barna, noe som forklarer den høye forekomsten av fibroelastose i denne spesielle hjertestrukturen. Patologier i aorta og dens klaff, oppdaget hos en tredjedel av barn med endokardiell proliferasjon, fører også til en økning (utvidelse) av venstre ventrikkelkammer og en forstyrrelse av dets funksjonalitet.
Ved instrumentelt bekreftet hjertefibroelastose anbefaler leger å avbryte svangerskapet. Hos nesten alle barn født av mødre som nektet medisinsk abort, ble tegnene på sykdommen bekreftet. Symptomer på hjertesvikt, karakteristiske for fibroelastose, oppstår innen et år (sjelden i 2.-3. leveår). Hos barn med en kombinert form av sykdommen oppdages tegn på hjertesvikt fra de første levedagene.
Medfødte former for primær og kombinert fibroelastose hos barn har oftest et raskt forløp med utvikling av alvorlig hjertesvikt. Lav aktivitet, sløvhet hos barnet, nektelse av amming på grunn av rask tretthet, dårlig appetitt, økt svetting indikerer dårlig helse. Alt dette fører til at barnet ikke går opp i vekt godt. Babyens hud er smertefullt blek, hos noen med et blålig skjær, oftest i nasolabialtrekanten.
Det er tegn på dårlig immunitet, så slike barn får ofte og raskt luftveisinfeksjoner, noe som kompliserer situasjonen. Noen ganger i løpet av de første dagene og månedene av livet viser ikke barnet noen sirkulasjonsforstyrrelser, men hyppige infeksjoner og lungesykdommer blir en utløser for utvikling av hjertesvikt.
Ytterligere helseundersøkelser av nyfødte og små barn med mistanke om fibroelastose eller tidligere diagnostiserte symptomer viste lavt blodtrykk (hypotensjon), forstørret hjerte (kardiomegali), dempede toner ved lytting til hjertet, noen ganger systolisk bilyd karakteristisk for mitralklaffinsuffisiens, takykardi, dyspné. Lytting til lungene viser tilstedeværelse av piping i pusten, noe som indikerer tetthet.
Endokardskade på venstre ventrikkel fører ofte til svekkelse av hjertets muskellag (myokard). Den normale hjerterytmen består av to rytmisk alternerende toner. Ved fibroelastose kan en tredje (og noen ganger en fjerde) tone oppstå. En slik patologisk rytme er tydelig hørbar og ligner en tretaktsgangart hos en hest (galopp) i lyden, og det er derfor den kalles galopprytmen.
Et annet symptom på fibroelastose hos små barn er forekomsten av en hjertepukkel. Faktum er at barnets ribbein i den tidlige barselperioden forblir ikke-forbenet og er representert av brusk. Økningen i hjertets størrelse fører til at det begynner å presse på de "myke" ribbeina, noe som resulterer i at de bøyer seg og tar en permanent fremoverbøyd form (hjertepukkel). Ved fibroelastose hos voksne dannes det ikke en hjertepukkel på grunn av styrken og stivheten i ribbeinas beinvev, selv ved en økning i alle hjertets strukturer.
Dannelsen av en hjertepukkel i seg selv indikerer bare en medfødt hjertefeil uten å spesifisere dens natur. Men uansett er det forbundet med en økning i størrelsen på hjertet og dets ventrikler.
Ødemsyndrom ved fibroelastose hos barn diagnostiseres sjelden, men mange barn opplever en forstørret lever, som begynner å stikke ut med gjennomsnittlig 3 cm fra under kanten av ribbebuen.
Hvis fibroelastose erverves (for eksempel, det er en konsekvens av betennelsessykdommer i hjertemembranene), er det kliniske bildet oftest sakte progressivt. I en periode kan symptomene være helt fraværende, deretter oppstår svake tegn på hjertedysfunksjon i form av kortpustethet under fysisk anstrengelse, økt hjertefrekvens, rask tretthet og lav fysisk utholdenhet. Litt senere begynner leveren å forstørres, ødem og svimmelhet oppstår.
Alle symptomer på ervervet fibroelastose er uspesifikke, noe som kompliserer diagnosen av sykdommen og ligner på kardiomyopati, lever- og nyresykdom. Sykdommen diagnostiseres oftest i stadiet med alvorlig hjertesvikt, noe som påvirker resultatene av behandlingen negativt.
Komplikasjoner og konsekvenser
Det skal sies at fibroelastose i hjertet og lungene er alvorlige patologier, hvis forløp avhenger av ulike omstendigheter. Medfødte hjertefeil kompliserer situasjonen betydelig, som kan elimineres kirurgisk i ung alder, men samtidig er det fortsatt en ganske høy risiko for død (omtrent 10 %).
Det antas at jo tidligere sykdommen utvikler seg, desto mer alvorlige vil konsekvensene være. Dette bekreftes av det faktum at medfødt fibroelastose i de fleste tilfeller har et fulminant eller akutt forløp med rask progresjon av hjertesvikt. Utvikling av akutt hjertesvikt hos et barn under 6 måneder regnes som et dårlig prognostisk tegn.
Behandlingen garanterer imidlertid ikke full gjenoppretting av hjertefunksjonen, men bremser bare utviklingen av symptomer på hjertesvikt. På den annen side fører fravær av slik støttende behandling til død i løpet av de to første leveårene.
Hvis hjertesvikt oppdages i løpet av de første dagene og månedene av et spedbarns liv, vil barnet mest sannsynlig ikke overleve en uke. Responsen på behandlingen varierer mellom barn. Uten terapeutisk effekt er det praktisk talt ikke noe håp. Men med den hjelpen som gis, er forventet levealder for et sykt barn kort (fra flere måneder til flere år).
Kirurgi og korrigering av medfødte hjertefeil som forårsaket fibroelastose forbedrer vanligvis pasientens tilstand. Ved vellykket kirurgisk behandling av venstre ventrikkelhyperplasi og overholdelse av legens krav, kan sykdommen få et godartet forløp: hjertesvikt vil ha et kronisk forløp uten tegn til progresjon. Selv om håpet om et slikt resultat er lite.
Når det gjelder den ervervede formen for hjertefibroelastose, blir den raskt kronisk og utvikler seg gradvis. Medisinering kan bremse prosessen, men ikke stoppe den.
Pulmonal fibroelastose, uavhengig av tidspunktet for endringer i parenkymet og membranene i organet etter den lette perioden, begynner å utvikle seg raskt og dreper faktisk en person i løpet av et par år, noe som forårsaker alvorlig respirasjonssvikt. Det triste er at effektive metoder for å behandle sykdommen ennå ikke er utviklet. [ 7 ]
Diagnostikk fibroelastose
Endomyokardial fibroelastose, hvis symptomer i de fleste tilfeller oppdages i tidlig alder, er en medfødt sykdom. Hvis vi utelukker de sjeldne tilfellene der sykdommen begynte å utvikle seg i sen barndom og voksen alder som en komplikasjon av skader og somatiske sykdommer, er det mulig å identifisere patologien i prenatalperioden, dvs. før barnets fødsel.
Leger mener at patologiske forandringer i endokardvevet, endringer i formen på fosterhjertet og noen trekk ved dets funksjon, karakteristiske for fibroelastose, kan bestemmes så tidlig som i den 14. svangerskapsuke. Men dette er fortsatt en ganske kort periode, og det kan ikke utelukkes at sykdommen kan manifestere seg noe senere, nærmere tredje trimester av svangerskapet, og noen ganger et par måneder før fødselen. Derfor anbefales det å utføre klinisk ultralydundersøkelse av fosterhjertet med flere ukers mellomrom når man overvåker gravide.
Hvilke tegn kan leger mistenke sykdommen ved neste ultralyd? Mye avhenger av sykdomsformen. Oftest diagnostiseres fibroelastose i venstre ventrikkel, men denne strukturen er ikke alltid forstørret. Den utvidede formen av sykdommen med forstørret venstre ventrikkel bestemmes lett under en ultralydundersøkelse ved hjertets sfæriske form, hvis toppunkt er representert av venstre ventrikkel, den generelle økningen i organstørrelsen og utbulingen av interventrikulærseptum mot høyre ventrikkel. Men hovedtegnet på fibroelastose er fortykkelse av endokardiet, samt hjerteseptum med en karakteristisk økning i ekogenisiteten til disse strukturene, som bestemmes av en spesifikk ultralydundersøkelse.
Studien utføres ved hjelp av spesielt ultralydutstyr med kardiologiprogrammer. Fosterekkokardiografi skader ikke moren eller det ufødte barnet, men lar ikke bare identifisere anatomiske endringer i hjertet, men også bestemme tilstanden til koronarkarene, tilstedeværelsen av blodpropper i dem og endringer i tykkelsen på hjertemembranene.
Fosterekkokardiografi er foreskrevet ikke bare i tilfelle avvik under dekoding av ultralydresultater, men også i tilfelle mors infeksjon (spesielt viral), bruk av potente medisiner, arvelig predisposisjon, tilstedeværelse av metabolske forstyrrelser, samt medfødte hjertesykdommer hos eldre barn.
Fosterekkokardiografi kan også oppdage andre medfødte former for fibroelastose. For eksempel fibroelastose i høyre ventrikkel, en utbredt prosess med samtidig skade på venstre ventrikkel og tilstøtende strukturer: høyre ventrikkel, hjerteklaffer, atrier, kombinerte former for fibroelastose, endomyokardial fibroelastose med fortykkelse av den indre slimhinnen i ventriklene og involvering av deler av myokardiet i den patologiske prosessen (vanligvis kombinert med trombose i veggen).
Endokardiell fibroelastose oppdaget i prenatal alder har en svært dårlig prognose, så leger anbefaler å avbryte svangerskapet i dette tilfellet. Muligheten for en feilaktig diagnose utelukkes ved en gjentatt ultralyd av fosterhjertet, som utføres 4 uker etter den første undersøkelsen som avdekket patologien. Det er tydelig at den endelige avgjørelsen om å avbryte eller opprettholde svangerskapet forblir hos foreldrene, men de må være klar over hva slags liv de dømmer barnet til.
Endokardiell fibroelastose oppdages ikke alltid under graviditet, spesielt med tanke på at ikke alle vordende mødre registrerer seg på en kvinnehelseklinikk og gjennomgår forebyggende ultralyddiagnostikk. Barnets sykdom i livmoren har praktisk talt ingen effekt på den gravide kvinnens tilstand, så fødselen av en syk baby blir ofte en ubehagelig overraskelse.
I noen tilfeller får både foreldre og leger vite om babyens sykdom flere måneder etter fødselen. I dette tilfellet kan det hende at laboratorieblodprøver ikke viser noe annet enn en økning i natriumkonsentrasjonen (hypernatremi). Men resultatene vil være nyttige for å utføre differensialdiagnostikk for å utelukke inflammatoriske sykdommer.
Det er fortsatt håp for instrumentell diagnostikk. En standard hjerteundersøkelse (EKG) er ikke spesielt indikativ ved fibroelastose. Den bidrar til å identifisere forstyrrelser i hjertet og hjertemuskelens elektriske ledningsevne, men spesifiserer ikke årsakene til slike lidelser. Dermed indikerer en endring i EKG-spenningen (i yngre alder er den vanligvis undervurdert, i eldre alder - tvert imot, for høy) kardiomyopati, som kan være assosiert ikke bare med hjertesykdommer, men også med metabolske forstyrrelser. Takykardi er et symptom på hjertesykdommer. Og hvis begge hjertets ventrikler er påvirket, kan kardiogrammet generelt virke normalt. [ 8 ]
Computertomografi (CT) er et utmerket ikke-invasivt verktøy for å oppdage kardiovaskulær forkalkning og utelukke perikarditt.[ 9 ]
Magnetisk resonansavbildning (MR) kan være nyttig for å oppdage fibroelastose fordi biopsi er invasiv. En hypointens kant på en myokardperfusjonssekvens og en hyperintens kant på en forsinket forsterkningssekvens tyder på fibroelastose.[ 10 ]
Men dette betyr ikke at studien bør forlates, fordi den bidrar til å bestemme arten av hjertets arbeid og graden av utvikling av hjertesvikt.
Når symptomer på hjertesvikt oppstår og pasienten oppsøker lege om dette, foreskrives også: røntgen av brystet, computertomografi eller magnetisk resonansavbildning av hjertet, ekkokardiografi (ECCG). I tvilstilfeller er det nødvendig å ty til en biopsi av hjertevev med påfølgende histologisk undersøkelse. Diagnosen er svært alvorlig, derfor krever den samme tilnærming til diagnose, selv om behandlingen ikke er mye forskjellig fra symptomatisk behandling for koronar hjertesykdom og hjertesvikt.
Men selv en slik grundig undersøkelse vil ikke være nyttig hvis resultatene ikke brukes i differensialdiagnostikk. EKG-resultater kan brukes til å differensiere akutt fibroelastose fra idiopatisk myokarditt, eksudativ perikarditt, aortastenose. Samtidig vil laboratorietester ikke vise tegn på betennelse (leukocytose, økt ESR, etc.), og temperaturmålinger vil ikke vise hypertermi.
Analyse av hjertelyder og bilyd, endringer i atrienes størrelse og en studie av anamnesen bidrar til å skille endokardiell fibroelastose fra isolert mitralklaffinsuffisiens og mitralklaffedefekt.
Analyse av anamnestiske data er nyttig for å skille mellom fibroelastose og hjerte- og aortastenose. Ved aortastenose er det også verdt å være oppmerksom på å bevare sinusrytmen og fraværet av tromboembolisme. Hjerterytmeforstyrrelser og trombeavsetning observeres heller ikke ved ekssudativ perikarditt, men sykdommen manifesterer seg med økt temperatur og feber.
Den største vanskeligheten er å skille endokardiell fibroelastose og kongestiv kardiomyopati. I dette tilfellet har fibroelastose, selv om den i de fleste tilfeller ikke er ledsaget av uttalte hjerteledningsforstyrrelser, en mindre gunstig behandlingsprognose.
Ved kombinerte patologier er det nødvendig å være oppmerksom på eventuelle avvik som avdekkes under tomografi eller ultralyd av hjertet, fordi medfødte defekter kompliserer forløpet av fibroelastose betydelig. Hvis kombinert endokardiell fibroelastose oppdages i den intrauterine perioden, er det upassende å opprettholde svangerskapet. Det er mye mer humant å avbryte det.
Diagnose av pulmonal fibroelastose
Diagnostisering av pulmonal fibroelastose krever også viss kunnskap og ferdigheter fra legen. Faktum er at symptomene på sykdommen er ganske heterogene. På den ene siden indikerer de kongestiv lungesykdom (ikke-produktiv hoste, kortpustethet), og på den andre siden kan de også være en manifestasjon av hjertesykdom. Derfor kan ikke diagnosen av sykdommen reduseres til kun å angi symptomer og auskultasjon.
Blodprøver av pasienten bidrar til å utelukke inflammatoriske lungesykdommer, men gir ikke informasjon om kvantitative og kvalitative endringer i vev. Tilstedeværelsen av tegn på eosinofili bidrar til å skille sykdommen fra lungefibrose, som er lik i manifestasjoner, men avviser eller bekrefter ikke faktumet om fibroelastose.
Instrumentelle studier anses som mer indikative: røntgen av brystet og tomografisk undersøkelse av luftveiene, samt funksjonelle analyser, som består av å bestemme respirasjonsvolum, lungenes vitalkapasitet og trykk i organet.
Ved pulmonal fibroelastose er det verdt å være oppmerksom på nedgangen i funksjonen til ekstern respirasjon, målt under spirometri. Nedgangen i aktive alveolære hulrom påvirker lungenes vitale kapasitet (VCL) betydelig, og fortykkelsen av veggene i indre strukturer påvirker organets diffusjonskapasitet (DCL), som sikrer ventilasjon og gassutvekslingsfunksjoner (enkelt sagt, absorpsjon av karbondioksid fra blodet og avgivelse av oksygen).
Karakteristiske tegn på pleeuroparenkymal fibroelastose er en kombinasjon av begrenset luftstrøm inn i lungene (obstruksjon) og nedsatt lungeekspansjon under innånding (restriksjon), forverring av ekstern respirasjonsfunksjon, moderat pulmonal hypertensjon (økt trykk i lungene), diagnostisert hos halvparten av pasientene.
En lungevevsbiopsi viser karakteristiske endringer i organets indre struktur. Disse inkluderer: fibrose i pleura og parenkym i kombinasjon med elastose i alveolveggene, akkumulering av lymfocytter i området med kompakte alveolære septa, transformasjon av fibroblaster til muskelvev som ikke er typisk for dem, og tilstedeværelse av ødematøs væske.
Tomogrammet viser skader på lungene i de øvre delene i form av pleuralkompakteringsfokus og strukturelle endringer i parenkymet. Det forstørrede bindevevet i lungene ligner muskelvev i farge og egenskaper, men lungevolumet avtar. Ganske store luftholdige hulrom (cyster) finnes i parenkymet. Irreversibel fokal (eller diffus) ekspansjon av bronkiene og bronkiolene (traktjonsbronkiektasi) og en lav posisjon av diafragmakuppelen er karakteristisk.
Radiologiske undersøkelser avdekker områder med «slipt glass» og «bikake-lunge» hos mange pasienter, noe som indikerer ujevn ventilasjon av lungene på grunn av tilstedeværelsen av foci av vevskomprimering. Omtrent halvparten av pasientene har forstørrede lymfeknuter og lever.
Pulmonal fibroelastose bør differensieres fra fibrose forårsaket av parasittinfeksjon og tilhørende eosinofili, endokardiell fibroelastose, lungesykdommer med nedsatt ventilasjon og et "bikake-lunge"-bilde, den autoimmune sykdommen histicotitis X (en form for denne patologien med lungeskade kalles Hand-Schüller-Christian sykdom), manifestasjoner av sarkoidose og lungetuberkulose.
Behandling fibroelastose
Fibroelastose, uansett hvor den befinner seg, regnes som en farlig og praktisk talt uhelbredelig sykdom. Patologiske forandringer i pleura og lungeparenkym kan ikke gjenopprettes med medisiner. Og selv bruk av hormonelle antiinflammatoriske legemidler (kortikosteroider) i kombinasjon med bronkodilatatorer gir ikke ønsket resultat. Bronkodilatatorer bidrar til å lindre pasientens tilstand litt, og lindrer det obstruktive syndromet, men de påvirker ikke prosessene som forekommer i lungene, så de kan bare brukes som støttende terapi.
Kirurgisk behandling for pulmonal fibroelastose er også ineffektiv. Den eneste operasjonen som kan endre situasjonen er en donororgantransplantasjon. Men lungetransplantasjon har dessverre den samme ugunstige prognosen. [ 11 ]
Ifølge utenlandske forskere kan fibroelastose også betraktes som en av de hyppigste komplikasjonene ved lunge- eller benmargsstamcelletransplantasjon. I begge tilfeller skjer det endringer i bindevevsfibrene i lungene, noe som påvirker funksjonen til ekstern respirasjon.
Sykdommen utvikler seg uten behandling (og effektiv behandling mangler for tiden), og omtrent 40 % av pasientene dør av respirasjonssvikt innen 1,5–2 år. Forventet levealder for de som blir igjen er også sterkt begrenset (opptil 10–20 år), i likhet med deres arbeidsevne. Personen blir ufør.
Hjertefibroelastose regnes også som en medisinsk uhelbredelig sykdom, spesielt hvis det er en medfødt patologi. Vanligvis lever ikke barn til de blir 2 år gamle. De kan bare reddes ved en hjertetransplantasjon, som i seg selv er en vanskelig operasjon med høy grad av risiko og uforutsigbare konsekvenser, spesielt i så ung alder.
Hos noen babyer er det mulig å korrigere medfødte hjertefeil kirurgisk, slik at de ikke forverrer tilstanden til det syke barnet. Ved stenose av arterien installeres en vaskulær dilatator - en shunt (aortokoronær bypass). Ved utvidelse av venstre hjertekammer gjenopprettes formen raskt. Men selv en slik operasjon garanterer ikke at barnet vil kunne klare seg uten transplantasjon. Omtrent 20-25 % av babyer overlever, og de lider av hjertesvikt hele livet, dvs. de regnes ikke som friske.
Hvis sykdommen er ervervet, er det verdt å kjempe for barnets liv ved hjelp av medisiner. Men det er viktig å forstå at jo tidligere sykdommen manifesterer seg, desto vanskeligere vil det være å bekjempe den.
Medikamentell behandling tar sikte på å bekjempe og forebygge forverring av hjertesvikt. Pasienter får foreskrevet følgende hjertemedisiner:
- ACE-hemmere (angiotensin-konverterende enzym) som påvirker blodtrykket og opprettholder det innenfor normale grenser (kaptopril, enalapril, benazepril, etc.),
- betablokkere som brukes til å behandle hjerterytmeforstyrrelser, arteriell hypertensjon og forebygge hjerteinfarkt (anaprilin, bisoprolol, metoprolol),
- hjerteglykosider, som ved langtidsbruk ikke bare støtter hjertets funksjon (øker kaliuminnholdet i kardiomyocytter og forbedrer hjertemuskelens ledningsevne), men også er i stand til å redusere graden av endokardiell fortykkelse noe (digoksin, gitoksin, strofantin),
- kaliumsparende diuretika (spironolakton, veroshpiron, decriz), som forhindrer vevsødem,
- antitrombotisk behandling med antikoagulantia (kardiomagnyl, magnicor), som forhindrer dannelse av blodpropper og sirkulasjonsforstyrrelser i koronarkarene.
Ved den medfødte formen for endokardiell fibroelastose fremmer ikke støttende behandling bedring, men reduserer risikoen for død som følge av hjertesvikt eller tromboembolisme med 70–75 %. [ 12 ]
Medisiner
Som vi kan se, er behandlingen av endokardiell fibroelastose praktisk talt ikke forskjellig fra behandlingen av hjertesvikt. I begge tilfeller tar kardiologer hensyn til alvorlighetsgraden av kardiopati. Forskrivning av medisiner er strengt individuell, og tar hensyn til pasientens alder, samtidige sykdommer, form og grad av hjertesvikt.
Ved behandling av ervervet endokardiell fibroelastose brukes legemidler fra 5 grupper. La oss vurdere ett legemiddel fra hver gruppe.
"Enalapril" er et legemiddel fra gruppen ACE-hemmere, produsert i form av tabletter i forskjellige doser. Legemidlet øker koronar blodstrøm, utvider arteriene, reduserer blodtrykket uten å påvirke hjernesirkulasjonen, bremser og reduserer utvidelsen av venstre ventrikkel. Legemidlet forbedrer blodtilførselen til myokardiet, reduserer effekten av iskemi, reduserer blodpropp litt, forhindrer dannelse av blodpropper og har en svak vanndrivende effekt.
Ved hjertesvikt foreskrives medisinen for en periode på mer enn seks måneder eller permanent. Medisinen startes med en minimumsdose (2,5 mg), og økes gradvis med 2,5–5 mg hver 3.–4. dag. Den permanente dosen vil være den som tolereres godt av pasienten og som opprettholder blodtrykket innenfor normalområdet.
Maksimal daglig dose er 40 mg. Den kan tas én gang eller deles inn i 2 doser.
Hvis blodtrykket er under normalt, reduseres dosen gradvis. Behandling med Enalapril bør ikke stoppes brått. Det anbefales å ta en vedlikeholdsdose på 5 mg per dag.
Legemidlet er beregnet for behandling av voksne pasienter, men kan også foreskrives til barn (sikkerheten er ikke offisielt fastslått, men ved fibroelastose står livet til en liten pasient på spill, så risikoforholdet tas i betraktning). ACE-hemmeren er ikke foreskrevet til pasienter med intoleranse mot stoffets komponenter, med porfyri, graviditet og amming. Hvis pasienten tidligere har hatt angioødem mens han tok legemidler i denne gruppen, er Enalapril forbudt.
Forsiktighet bør utvises ved forskrivning av legemidlet til pasienter med samtidig patologier: alvorlige nyre- og leversykdommer, hyperkalemi, hyperaldosteronisme, aorta- eller mitralklaffstenose, systemiske bindevevspatologier, hjerteiskemi, hjernesykdom, diabetes mellitus.
Ved behandling med legemidlet, ikke ta konvensjonelle diuretika for å unngå dehydrering og en sterk hypotensiv effekt. Samtidig administrering med kaliumsparende diuretika krever dosejustering, da det er høy risiko for hyperkalemi, som igjen fremkaller hjertearytmi, anfall, redusert muskeltonus, økt svakhet, etc.
Legemidlet "Enalapril" tolereres vanligvis godt, men noen pasienter kan oppleve bivirkninger. De vanligste er: en sterk reduksjon i blodtrykket opp til kollaps, hodepine og svimmelhet, søvnforstyrrelser, økt tretthet, reversibelt tap av balanse, hørsel og syn, forekomst av tinnitus, kortpustethet, hoste uten sputumsekresjon, endringer i blod- og urinsammensetningen, vanligvis indikerer feil funksjon av lever og nyrer. Mulig: hårtap, redusert seksuell lyst, symptomer på "hetetokter" (følelse av varme og hjertebank, hyperemi i ansiktshuden, etc.).
«Bisoprolol» er en betablokker med selektiv virkning, som har hypotensive og anti-iskemiske effekter, og som bidrar til å bekjempe manifestasjoner av takykardi og arytmi. Et rimelig legemiddel i tablettform som forhindrer progresjon av hjertesvikt ved endokardiell fibroelastose. [ 13 ]
Som mange andre legemidler som foreskrives mot koronar hjertesykdom og hjertesvikt, foreskrives bisoprolol over lengre tid. Det anbefales å ta det om morgenen før eller under måltider.
Når det gjelder anbefalte doser, velges de individuelt avhengig av blodtrykksmålingene og legemidlene som foreskrives parallelt med dette legemidlet. I gjennomsnitt er en enkelt (også daglig) dose 5–10 mg, men med en liten økning i blodtrykket kan den reduseres til 2,5 mg. Maksimal dose som kan foreskrives til en pasient med normalt fungerende nyrer er 20 mg, men kun ved vedvarende høyt blodtrykk.
Det er kun mulig å øke de angitte dosene med legens tillatelse. Men ved alvorlige lever- og nyresykdommer anses 10 mg som den maksimalt tillatte dosen.
Ved kompleks behandling av hjertesvikt mot bakgrunn av venstre ventrikkel dysfunksjon, som oftest forekommer ved fibroelastose, velges en effektiv dose ved gradvis å øke doseringen med 1,25 mg. I dette tilfellet starter de med den lavest mulige dosen (1,25 mg). Dosen økes med intervaller på 1 uke.
Når dosen når 5 mg, økes intervallet til 28 dager. Etter 4 uker økes dosen med 2,5 mg. Ved å følge dette intervallet og normen når de 10 mg, som pasienten må ta over lengre tid eller kontinuerlig.
Hvis en slik dosering tolereres dårlig, reduseres den gradvis til et komfortabelt nivå. Behandling med en betablokker bør heller ikke stoppes brått.
Legemidlet bør ikke foreskrives ved overfølsomhet for virkestoffene og hjelpestoffene i legemidlet, akutt og dekompensert hjertesvikt, kardiogent sjokk, atrioventrikulær blokk grad 2-3, bradykardi, vedvarende lavt blodtrykk og noen andre hjertesykdommer, alvorlig bronkial astma, bronkoobstruksjon, alvorlige perifere sirkulasjonsforstyrrelser, metabolsk acidose.
Forsiktighet bør utvises ved forskrivning av kompleks behandling. Kombinasjon av bisoprolol med noen antiarytmika (kinidin, lidokain, fenytoin, etc.), kalsiumantagonister og sentralhypotensive legemidler anbefales derfor ikke.
Ubehagelige symptomer og lidelser som er mulige under behandling med Bisoprolol: økt tretthet, hodepine, hetetokter, søvnforstyrrelser, blodtrykksfall og svimmelhet når man står opp av sengen, hørselstap, mage-tarmsymptomer, lever- og nyresykdommer, redusert potens, muskelsvakhet og kramper. Noen ganger klager pasienter over perifere sirkulasjonsforstyrrelser, som manifesterer seg i form av temperaturfall eller nummenhet i ekstremiteter, spesielt fingre og tær.
Ved samtidig sykdom i bronkopulmonalsystemet, nyrer, lever og diabetes mellitus er risikoen for bivirkninger høyere, noe som indikerer en forverring av sykdommen.
«Digoksin» er et populært, budsjettvennlig hjerteglykosid basert på revebjelleplanten, som utleveres strengt på resept (i tabletter) og bør brukes under tilsyn av lege. Injeksjonsbehandling utføres på sykehus under forverring av koronar hjertesykdom og hjertesvikt, tabletter foreskrives kontinuerlig i minimalt effektive doser, siden legemidlet har en toksisk og narkotisk effekt.
Den terapeutiske effekten består i å endre styrken og amplituden til myokardkontraksjonene (gir hjertet energi, støtter det under iskemiske tilstander). Legemidlet har også en vasodilatorisk (reduserer tetthet) og en viss vanndrivende effekt, som bidrar til å lindre hevelse og redusere alvorlighetsgraden av respirasjonssvikt, manifestert som kortpustethet.
Faren ved digoksin og andre hjerteglykosider er at de, hvis de overdoseres, kan provosere hjertearytmi forårsaket av økt eksitabilitet i myokardiet.
Ved forverring av hjertesvikt foreskrives legemidlet i form av injeksjoner, og en individuell dosering velges med tanke på alvorlighetsgraden av tilstanden og pasientens alder. Når tilstanden stabiliserer seg, byttes til tabletter.
Vanligvis er standard enkeltdose av legemidlet 0,25 mg. Administrasjonshyppigheten kan variere fra 1 til 5 ganger daglig med jevne intervaller. I det akutte stadiet av hjertesvikt kan den daglige dosen nå 1,25 mg, og når tilstanden stabiliserer seg permanent, er det nødvendig å ta en vedlikeholdsdose på 0,25 (sjeldnere 0,5) mg per dag.
Ved forskrivning av legemidlet til barn tas pasientens vekt i betraktning. En effektiv og sikker dose beregnes som 0,05–0,08 mg per kg kroppsvekt. Men legemidlet foreskrives ikke konstant, men i 1–7 dager.
Doseringen av hjerteglykosid bør foreskrives av lege, med tanke på pasientens tilstand og alder. Samtidig er det svært farlig å justere dosene uavhengig eller ta to legemidler med en slik effekt samtidig.
"Digoksin" er ikke foreskrevet for ustabil angina, alvorlige hjertearytmier, AV-hjerteblokk grad 2-3, hjertetamponade, Adams-Stokes-Morgagni syndrom, isolert bikuspidalklaffstenose og aortastenose, medfødt hjerteanomali kalt Wolff-Parkinson-White syndrom, hypertrofisk obstruktiv kardiomyopati, endo-, peri- og myokarditt, thorakal aortaaneurisme, hyperkalsemi, hypokalemi og noen andre patologier. Listen over kontraindikasjoner er ganske lang og inkluderer syndromer med flere manifestasjoner, så avgjørelsen om muligheten for å bruke dette legemidlet kan kun tas av en spesialist.
Digoksin har også bivirkninger. Disse inkluderer hjerterytmeforstyrrelser (som følge av feil dosevalg og overdose), tap av matlyst, kvalme (ofte med oppkast), tarmproblemer, alvorlig svakhet og høy tretthet, hodepine, forekomst av "fluer" foran øynene, reduksjon i blodplatenivået og blodproppforstyrrelser, allergiske reaksjoner. Oftest er forekomsten av disse og andre symptomer forbundet med å ta store doser av legemidlet, sjeldnere med langvarig behandling.
«Spironolakton» er en mineralokortikoid-antagonist. Den har en vanndrivende effekt, og fremmer utskillelsen av natrium, klor og vann, men beholder kalium, som er nødvendig for hjertets normale funksjon, siden dets ledende funksjon hovedsakelig er basert på dette elementet. Det bidrar til å lindre ødem. Det brukes som et hjelpemiddel ved hjertesvikt.
Ved hjertesvikt foreskrives legemidlet avhengig av sykdomsfasen. Ved forverring kan legemidlet foreskrives både i form av injeksjoner og i tabletter med en dosering på 50–100 mg per dag. Når tilstanden stabiliserer seg, foreskrives en vedlikeholdsdose på 25–50 mg over lengre tid. Hvis balansen mellom kalium og natrium forstyrres, i retning av en reduksjon i kalium og natrium, kan dosen økes til en normal konsentrasjon av sporstoffer er etablert.
I pediatrisk behandling beregnes den effektive dosen basert på et forhold på 1-3 mg spironolakton per kilogram av pasientens kroppsvekt.
Som vi kan se, er valget av anbefalt dose også her individuelt, slik tilfellet er med forskrivning av mange andre legemidler som brukes i kardiologi.
Kontraindikasjoner for bruk av vanndrivende midler kan være: overskudd av kalium eller lavt natriumnivå i kroppen, patologi forbundet med manglende vannlating (anuri), alvorlig nyresykdom med nedsatt ytelse. Legemidlet er ikke foreskrevet for gravide og ammende mødre, samt for de som har intoleranse mot komponentene i legemidlet.
Forsiktighet bør utvises ved bruk av legemidlet hos pasienter med AV-hjerteblokk (kan forverres), kalsiumoverskudd (hyperkalsemi), metabolsk acidose, diabetes mellitus, menstruasjonsuregelmessigheter og leversykdom.
Bruk av legemidlet kan forårsake hodepine, døsighet, tap av balanse og koordinasjon av bevegelser (ataksi), forstørrelse av melkekjertlene hos menn (gynekomasti) og impotens, endringer i menstruasjonens natur, grovere stemme og overdreven hårvekst hos kvinner (hirsutisme), smerter i epigastrium og mage-tarmlidelser, tarmkolikk, nyresvikt og mineralubalanse. Hud- og allergiske reaksjoner er mulige.
Bivirkninger observeres vanligvis når den nødvendige dosen overskrides. Ødem kan oppstå når doseringen er utilstrekkelig.
"Magnicor" er et legemiddel som forhindrer dannelse av blodpropper, basert på acetylsalisylsyre og magnesiumhydroksid. Et av de effektive antitrombotiske midlene som er foreskrevet for hjertesvikt. Det har en smertestillende, betennelsesdempende og blodplatehemmende effekt, og påvirker respirasjonsfunksjonen. Magnesiumhydroksid reduserer den negative effekten av acetylsalisylsyre på mage-tarmslimhinnen.
Ved endomyokardiell fibroelastose foreskrives legemidlet profylaktisk, derfor overholdes den minste effektive dosen - 75 mg, som tilsvarer 1 tablett. Ved hjerteiskemi på grunn av trombedannelse og påfølgende innsnevring av koronarkarrenes lumen, er startdosen 2 tabletter, og vedlikeholdsdosen tilsvarer den profylaktiske dosen.
Overskridelse av anbefalt dose øker risikoen for blødning som er vanskelig å stoppe betydelig.
Dosene er indisert for voksne pasienter på grunn av at legemidlet inneholder acetylsalisylsyre, hvis bruk i en alder av under 15 år kan ha alvorlige konsekvenser.
Legemidlet er ikke foreskrevet til pasienter i barndommen og tidlig ungdomstid, ved intoleranse mot acetylsalisylsyre og andre komponenter i legemidlet, "aspirin" astma (i historien), akutt erosiv gastritt, magesår, hemoragisk diatese, alvorlig lever- og nyresykdom, ved alvorlig dekompensert hjertesvikt.
Under graviditet foreskrives Magnicor kun i ekstreme tilfeller og kun i 1.-2. trimester, tatt i betraktning mulige negative effekter på fosteret og svangerskapsforløpet. I 3. trimester av svangerskapet er slik behandling uønsket, da den bidrar til redusert livmors kontraktilitet (langvarig fødsel) og kan forårsake alvorlig blødning. Fosteret kan ha pulmonal hypertensjon og nyresvikt.
Bivirkninger av legemidlet inkluderer symptomer fra mage-tarmkanalen (dyspepsi, epigastriske og magesmerter, en viss risiko for mageblødning med utvikling av jernmangelanemi). Mot bakgrunnen av bruk av legemidlet er neseblødning, blødning fra tannkjøtt og urinveisorganer mulig.
Overdosering kan forårsake svimmelhet, besvimelse og øresus. Allergiske reaksjoner er ikke uvanlige, spesielt i forbindelse med overfølsomhet for salisylater. Anafylaksi og respirasjonssvikt er imidlertid sjeldne bivirkninger.
Valg av legemidler i kompleks terapi og anbefalte doseringer bør være strengt individuelt. Spesiell forsiktighet bør utvises ved behandling av gravide, ammende, barn og eldre pasienter.
Tradisjonell medisin og homeopati
Hjertefibroelastose er en alvorlig og alvorlig sykdom med et karakteristisk progressivt forløp og praktisk talt ingen sjanse for bedring. Det er tydelig at effektiv behandling av en slik sykdom med folkemedisiner er umulig. Tradisjonelle medisinske oppskrifter, som hovedsakelig er basert på urtebehandling, kan kun brukes som et hjelpemiddel og kun med tillatelse fra en lege, for ikke å komplisere en allerede dårlig prognose.
Når det gjelder homeopatiske midler, er bruken av dem ikke forbudt, og kan være en del av en omfattende behandling for hjertesvikt. I dette tilfellet snakker vi imidlertid ikke så mye om behandling som om å forhindre utviklingen av hjertesvikt.
Legemidlene bør foreskrives av en erfaren homeopat, og spørsmålet om muligheten for å inkludere dem i kompleks terapi er innenfor den behandlende legens kompetanse.
Hvilke homeopatiske medisiner bidrar til å forsinke utviklingen av hjertesvikt ved fibroelastose? Ved akutt hjertesvikt vender homeopater seg til hjelp av følgende medisiner: Arsenicum album, Antimonium tartaricum, Carbo vegetabilis, Acidum oxalicum. Til tross for likheten i indikasjonene, stoler legene på de ytre manifestasjonene av iskemi i form av cyanose (dens grad og prevalens) og arten av smertesyndromet når de velger en effektiv medisin.
Ved hjertesvikt kan følgende inkluderes i vedlikeholdsbehandlingen: Lachesis og Nayu, Lycopus (i de tidlige stadiene av hjerteforstørrelse), Laurocerasus (mot kortpustethet i hvile), Latrodectus mactans (mot klaffepatologier), hagtornpreparater (spesielt nyttige for endomyokardiale lesjoner).
Ved sterk hjerterytme kan følgende foreskrives for symptomatisk behandling: Spigelia, Glonoinum (mot takykardi), Aurum metallicum (mot hypertensjon).
For å redusere alvorlighetsgraden av kortpustethet, hjelper følgende: Grindelia, Spongia og Lahegis. For å lindre hjertesmerter kan følgende foreskrives: Cactus, Cereus, Naya, Cuprum, for å lindre angst mot denne bakgrunnen - Aconitum. Ved utvikling av hjerteastma er følgende indisert: Digitalis, Laurocerasus, Lycopus.
Forebygging
Forebygging av ervervet fibroelastose i hjerte og lunger består av forebygging og rettidig behandling av smittsomme og inflammatoriske sykdommer, spesielt når det gjelder skade på vitale organer. Effektiv behandling av den underliggende sykdommen bidrar til å forhindre farlige konsekvenser, som inkluderer fibroelastose. Dette er en utmerket grunn til å ta godt vare på helsen din og helsen til fremtidige generasjoner, det såkalte arbeidet for en sunn fremtid og et langt liv.
Prognose
Bindevevsendringene forbundet med hjerte- og lungefibroelastose anses som irreversible. Selv om noen legemidler kan redusere tykkelsen på endokardiet noe med langvarig behandling, garanterer de ikke en kur. Selv om tilstanden ikke alltid er dødelig, er prognosen fortsatt relativt dårlig. 4-års overlevelsesraten er 77 %. [ 14 ]
Den verste prognosen, som vi allerede har nevnt, er ved den medfødte formen for hjertefibroelastose, der manifestasjonene av hjertesvikt er synlige allerede i de første ukene og månedene av barnets liv. Bare en hjertetransplantasjon kan redde babyen, noe som i seg selv er en risikabel operasjon i en så tidlig periode, og den må gjøres før 2 år. Slike barn lever vanligvis ikke lenger.
Andre operasjoner gjør det bare mulig å unngå barnets tidlige død (og ikke alltid), men kan ikke kurere det fullstendig fra hjertesvikt. Døden inntreffer med dekompensasjon og utvikling av respirasjonssvikt.
Prognosen for pulmonal fibroelastose avhenger av sykdommens karakteristikker. Hvis symptomene utvikler seg raskt, er sjansene ekstremt små. Hvis sykdommen utvikler seg gradvis, kan pasienten leve i omtrent 10–20 år, inntil respirasjonssvikt oppstår på grunn av endringer i lungenes alveoler.
Mange vanskelige patologier kan unngås dersom forebyggende tiltak iverksettes. Ved hjertefibroelastose handler dette først og fremst om å forebygge de faktorene som kan påvirke utviklingen av hjertet og sirkulasjonssystemet til fosteret (med unntak av arvelig predisposisjon og mutasjoner, som leger er maktesløse mot). Hvis de ikke kan unngås, bidrar tidlig diagnostikk til å identifisere patologien på et stadium der svangerskapsavbrudd er mulig, noe som i denne situasjonen anses som humant.

