Medisinsk ekspert av artikkelen
Nye publikasjoner
Leveramyloidose
Sist anmeldt: 29.06.2025

Alt iLive-innhold blir gjennomgått med medisin eller faktisk kontrollert for å sikre så mye faktuell nøyaktighet som mulig.
Vi har strenge retningslinjer for innkjøp og kun kobling til anerkjente medieområder, akademiske forskningsinstitusjoner og, når det er mulig, medisinsk peer-evaluerte studier. Merk at tallene i parenteser ([1], [2], etc.) er klikkbare koblinger til disse studiene.
Hvis du føler at noe av innholdet vårt er unøyaktig, utdatert eller ellers tvilsomt, velg det og trykk Ctrl + Enter.
Amyloidose er vanligvis en systemisk, generell patologi som er karakterisert ved akkumulering av amyloid (et spesifikt glykoprotein) i vev og påfølgende forstyrrelse av normal organfunksjon. Leveramyloidose er mye mindre vanlig enn nyre og milt [ 1 ], men følger nesten alltid med systemisk skade på kroppen. Ingen av de eksisterende bildediagnostiske teknikkene kan spesifikt påvise tilstedeværelsen av amyloid. Selv ved klinisk og radiologisk mistanke avhenger diagnosen amyloidose av vevsbiopsi for å bekrefte tilstedeværelsen av amyloidavleiringer. [ 3 ] Behandlingen er kompleks, omfattende og inkluderer immunsuppressive og symptomatiske tiltak. I alvorlige tilfeller kan levertransplantasjon være nødvendig.
Epidemiologi
Behandlingens suksess avhenger direkte av rettidig diagnose av sykdommen, som forårsaker dannelsen av et protein-polysakkaridkompleks (amyloid) i ulike organer og leveren. Som praksis viser, er amyloidose vanskelig å anta eller mistenke, selv om det er mulig å identifisere og bekrefte den. Faktum er at i mer enn 80 % av uoppdagede tilfeller er sykdommen klinisk maskert av leverpatologi. Den mest effektive diagnostiske metoden er biopsi.
Leveramyloidose er et sjeldnere problem sammenlignet med renal amyloidose. Samtidig er alle tilfeller av leverlesjoner ledsaget av lesjoner i andre organer. Oftest påvirker patologien hovedsakelig strukturelle deler av levertriaden, som bestemmer minimum og uspesifisitet av symptomatologien. Det kliniske og morfologiske bildet av hepatocellulær defekt og portal hypertensjon manifesterer seg i diffus og intralobulær type patologi.
En leverbiopsi er berettiget når hepatomegali foreligger uten tidligere leversymptomer og i fravær av nefrotisk syndrom.
Diffus leveraffeksjon ses i omtrent 25 % av tilfellene, og hos 75 % av pasientene er det bare portaltraktene som er affisert.
Primær amyloidose påvirker leveren i 90 % av tilfellene, mens sekundær amyloidose påvirker leveren i bare 47 % av tilfellene.
Isolert leverpåvirkning er ekstremt sjelden. Nyrer (ca. 93 % av tilfellene), milt (72 %), hjerte (57 %), bukspyttkjertel (36 %), binyrer (29 %), tarmer og lunger (21 % hver) påvirkes vanligvis samtidig.
Kvinner får sykdommen nesten dobbelt så ofte som menn. Gjennomsnittlig levealder for amyloidosepasienter er 52–64 år.
Fører til hepatisk amyloidose
Amyloidose skjer med dannelse og akkumulering av et komplekst polysakkarid-proteinkompleks - amyloid - i levervevet. Problemet med forekomsten av den primære lesjonen er til dags dato ikke tilstrekkelig studert. Når det gjelder sekundær patologi, er dens forekomst vanligvis forbundet med slike sykdommer:
- Kroniske infeksjonsprosesser (tuberkulose, syfilis, aktinomykose);
- Purulente inflammatoriske prosesser (mikrobiell endokarditt, osteomyelitt, bronkiektatisk sykdom, etc.);
- Ondartede sykdommer (leukemi, visceral kreft, lymfogranulomatose).
Den reaktive formen for amyloidose finnes hos pasienter med samtidig aterosklerose, revmatologiske sykdommer (Bechterews sykdom, revmatoid artritt), psoriasis, kroniske inflammatoriske og multisystemiske prosesser (inkludert sarkoidose). De viktigste risikofaktorene: arvelig predisposisjon, cellulære immunitetsforstyrrelser, hyperglobulinemi.
Patogenesen
Det finnes en rekke antagelser angående opprinnelsen til leveramyloidose. De fleste spesialister holder seg til versjonen av dysproteinose, sykdommens immunologiske og mutasjonsmessige natur, samt lokal cellulær genese. Versjonen av cellulær genese inkluderer endringer i reaksjoner som virker på cellenivå (dannelse av fibrillære forløpere til amyloid av et kompleks av makrofager), selv om amyloid dannes og akkumuleres utenfor cellestrukturene.
Versjonen av dysproteinose er basert på det faktum at amyloid er et produkt av feil proteinmetabolisme. Den grunnleggende patogenetiske koblingen til problemet ligger i dysproteinemi og hyperfibrinogenemi, som fører til akkumulering av grovt dispergert protein og paraproteinfraksjoner i plasmaet.
Ifølge den immunologiske versjonen er amyloiddannelse forårsaket av en antigen-antistoff-reaksjon, der vevsnedbrytningsprodukter eller fremmede proteiner fungerer som antigener. Amyloidopphopning finnes hovedsakelig i området med antistoffdannelse og overdreven tilstedeværelse av antigener.
Den mest troverdige versjonen vurderer forskere som mutasjonsteori, som tar hensyn til en rekke mutagene faktorer som kan føre til abnormiteter i proteinsyntesen.
Amyloid er et komplekst hypoprotein som består av globulære og fibrillære proteiner kombinert med polysakkarider. Amyloid-opphopninger påvirker intima og adventitia i det vaskulære nettverket, stroma i parenkymatiske organer, strukturen til kjertler, osv. Amyloid-opphopninger forårsaker ikke funksjonsskade. Små opphopninger forårsaker ikke funksjonsforstyrrelser, men ved intens amyloid-tilstedeværelse i leveren øker volum, endrer organets utseende og utvikler funksjonssvikt.
Leveramyloidose er karakterisert ved avsetning av amyloidfibriller i Dysse-rommet, som vanligvis begynner i periportalregionen, selv om den noen ganger er sentrilobulær og også kan avsettes i leverens vaskulatur. [ 4 ], [ 5 ] I alvorlige tilfeller fører amyloidavsetning til trykkatrofi av hepatocytter, som forhindrer passasje av galle, noe som resulterer i kolestase, eller kan blokkere sinusoidene, noe som resulterer i portalhypertensjon. [ 6 ], [ 7 ], [ 8 ]
Symptomer hepatisk amyloidose
Det kliniske bildet ved leveramyloidose er variert og avhenger av intensiteten av amyloidopphopning, dens biokjemiske trekk, varigheten av den patologiske prosessen, graden av organskade og brudd på deres funksjonelle tilstand.
I det latente stadiet av amyloidose, når amyloidopphopninger i leveren kun kan oppdages ved mikroskopisk undersøkelse, er de første tegnene på sykdommen fraværende. Med videre utvikling og økende funksjonssvikt i organet, utvikler symptomatologien seg.
Leveren tykner gradvis og forstørres. Palpasjonsmetoden kan endres, men organets kanter er glatte og smertefrie. I sjeldne tilfeller er patologien ledsaget av smerter i subkostalområdet på høyre side, dyspepsi, forstørrelse av milten, gulfarging av hud, slimhinner og senehinner, hemoragisk syndrom.
De mest karakteristiske symptomene ved leveramyloidose: [ 9 ], [ 10 ]
- Amyloidopphopning i leveren forårsaker hepatomegali hos 33–92 % av pasientene;
- Mild gulsott
- Portal hypertensjon;
- Moderat til alvorlig kolestase.
Fordi amyloidose svært sjelden rammer bare ett organ, er det vanligvis ytterligere symptomer:
- Når nyreskade utvikler nefrotisk syndrom og arteriell hypertensjon med ytterligere nyresvikt, ødem, noen ganger nyretrombose, leukocyturi, hematuri, hypoproteinemi, azotemi og så videre;
- Når hjertet påvirkes, utvikles en tilstand som ligner på restriktiv kardiomyopati (rytmeforstyrrelser, kardiomegali, økende hjertesvikt, svakhet og dyspné, ødem, sjeldnere - væskeansamling i bukhulen og pleurahulen, perikarditt);
- Hvis fordøyelseskanalen påvirkes, kan makroglossi, svakhet og øsofageal peristaltikk, kvalme og halsbrann, forstoppelse eller diaré, osv. forekomme;
- Når bukspyttkjertelen er påvirket, er symptomene på kronisk pankreatitt tilstede;
- Hvis muskel- og skjelettmekanismen er involvert, utvikles symmetrisk polyartritt, karpaltunnelsyndrom og myopatier, og hvis nervesystemet påvirkes, oppdages polynevropatier, lammelse, ortostatisk lavt blodtrykk, økt svette og demens.
Hvis den patologiske reaksjonen sprer seg til huden, oppstår det en rekke voksaktige plakk i ansiktet, på halsen og i hudfoldene. Bildet av nevrodermatitt, rød plateepitelfeber og sklerodermi er mulig.
Kombinasjonen av flere amyloidlesjoner og variasjonen i symptomer gjør det mye vanskeligere å identifisere hepatisk amyloidose og krever en omfattende og fullstendig diagnose.
Skjemaer
I følge WHO-klassifiseringen skilles det mellom fem typer amyloidose:
- AL (primær);
- AA (sekundær);
- ATTR (arvelig og senil systemisk);
- Aβ2M (hos pasienter i hemodialyse);
- AIAPP (hos pasienter med insulinuavhengig diabetes mellitus);
- AB (for Alzheimers sykdom);
- AANF (senil atrieamyloidose).
Det er en lokal amyloidose i leveren, men oftere er det en systemisk lesjon, der den patologiske prosessen også involverer nyrer, hjerte, milt, nervesystem, samt andre organer og vev.
Komplikasjoner og konsekvenser
Systemisk amyloidose fører gradvis til utvikling av akutte patologiske prosesser som igjen kan føre til død. Blant de vanligste og livstruende komplikasjonene er følgende:
- Hyppige smittsomme (bakterielle, virale) patologier, inkludert lungebetennelse, pyelonefritt, glomerulonefritt;
- Kronisk lever- og nyresvikt;
- Kronisk hjertesvikt (kan gå forut for hjerteinfarkt);
- Hemoragiske slag.
Venøs trombose oppstår som et resultat av opphopning og avsetning av proteiner på veneveggene. Lumen i de berørte karene blir smalere, organsvikt utvikler seg. Over tid, på bakgrunn av langvarig hyperproteinemi, kan karet lukkes fullstendig. Enhver av komplikasjonene kan føre til et ugunstig utfall - død.
Diagnostikk hepatisk amyloidose
Ved mistanke om leveramyloidose utføres diagnostiske tiltak etter obligatoriske konsultasjoner med både gastroenterolog og terapeut, og revmatolog, kardiolog, hudlege, nevrolog, urolog. Det er viktig å gjøre en grundig vurdering av anamnese og kliniske manifestasjoner, og å gjennomføre en omfattende laboratorie- og instrumentell diagnostikk.
Testene inkluderer nødvendigvis urin- og blodprøve. Ved hepatisk amyloidose finnes ofte en kombinasjon av leukocyturi med proteinuri og sylindruri, og hypoproteinemi - med hyperlipidemi, anemi, hyponatremi og hypokalsemi, redusert blodplatetall. Paraproteiner påvises i urin og serumelektroforese.
Instrumentell diagnostikk inkluderer:
- EKG, ekko;
- Ultralyd av magen;
- Røntgenbilder av magesekken, spiserøret;
- Irrigografi, bariumrøntgenstråler;
- Endoskopi.
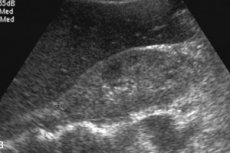
Radiologiske funn av hepatisk amyloidose inkluderer uspesifikk hepatomegali, økt ekogenisitet på ultralyd eller tetthet på computertomografi (CT), og økt T1-signalintensitet på magnetisk resonansavbildning (MR). [ 12 ] Scintigrafi med Tc-99m-relaterte indikatorer viser heterogent opptak, men det er uspesifikt. [ 13 ], [ 14 ] GC har vist seg å øke leverstivhet målt ved elastografi; [ 15 ], [ 16 ], [ 17 ] men det finnes få kasusrapporter. Magnetisk resonanselastografi (MRE) er for tiden den mest nøyaktige ikke-invasive metoden for å oppdage og stadiebestemme leverfibrose, [ 18 ], [ 19 ] MRE er nyttig for å oppdage progresjon, respons på behandling og forutsi leverdekompensasjon hos pasienter med leverfibrose. [ 20 ]
Leveramyloidose på ultralyd er vanskelig å bestemme: en forstørrelse av organet bestemmes, med den mest spesifikke hepatomegalien som overstiger 15 cm. Under kontroll av ultralyd utføres en biopsi, som blir en avgjørende indikator for diagnose. Ved hjelp av en spesiell nål tas en liten mengde levervev, deretter farges det med et spesielt fargestoff og undersøkes under et mikroskop, som lar deg se amyloidavleiringer direkte.
En endelig diagnose stilles først etter påvisning av amyloidfibriller i levervevet og andre organer. Den genetisk bestemte typen amyloidose bestemmes ved nøye genetisk-medisinsk undersøkelse av stamtavlen.
Differensiell diagnose
Amyloidose bør mistenkes hos alle pasienter med en kombinasjon av renal proteinuri, restriktiv kardiomyopati, autonom eller perifer nevropati og hepatomyeli, selv i fravær av monoklonalt paraprotein. Det er svært viktig å verifisere typen amyloidose fordi behandlingen av lesjoner med ulik etiologi er svært forskjellig.
Histologisk diagnose innebærer farging med Kongorødt etterfulgt av mikroskopisk undersøkelse i polariserende lys. Det anbefales å biopsiere flere vevsprøver samtidig. Hvis resultatet av fargingen blir positivt, utføres immunhistokjemisk analyse ved bruk av monoklonale antistoffer mot forløperproteiner for å identifisere typen amyloid.
DNA-analyse utføres for å skille mellom primær amyloidose og ulike varianter av genetisk bestemt amyloidose. Amyloidfibriller kan isoleres fra biopsiprøver og sekvestreres til individuelle aminosyrer.
Ytterligere studier for å bestemme plasmacelledyskrasi:
- Elektroforese av serumproteiner i blod og urin;
- Immunoassay for frie lette kjeder;
- Immunfiksering (immunoblotting) av serumproteiner;
- Benmargsaspirasjon og trepanobiopsi.
Diagnose av leveramyloidose er en langvarig og arbeidskrevende prosess, som krever økt oppmerksomhet fra spesialister og kvalitetsutstyr fra klinikker og laboratorier.
Hvem skal kontakte?
Behandling hepatisk amyloidose
Behandlingstiltakene tar sikte på å redusere konsentrasjonen av eksisterende amyloidproteiner i blodet (eliminere årsaken til amyloidose) og støtte tilstrekkelig leverfunksjon.
Sekundær amyloidose krever blokkering av den inflammatoriske prosessen (ved kroniske infeksjons- og autoimmune patologier). Ved autoimmune sykdommer anbefales bruk av cytostatika. For å eliminere kroniske infeksjonsprosesser fjernes ofte det betennelsesutsatte området kirurgisk. Ofte kan denne tilnærmingen stoppe videre progresjon av amyloidose og forbedre leverfunksjonen.
Primær amyloidose krever bruk av kjemopreventive legemidler og noen ganger benmargstransplantasjon.
Gjeldende retningslinjer anbefaler kombinasjonen av cyklofosfamid, bortezomib, deksametason (CyBorD) og daratumumab som førstelinjebehandling hos pasienter som nylig har fått diagnosen AL.
Bortezomib er en proteasomhemmer. Proteasomer er involvert i å redusere proteotoksisitet og regulere proteiner som kontrollerer cellulær progresjon og apoptose. Plasmaceller som genererer amyloid er spesielt følsomme for proteasomhemming fordi de er avhengige av proteasomet for å redusere de toksiske effektene av lette kjeder og forhindre apoptose.
Daratumumumab er et monoklonalt antistoff (mAb) som binder seg til CD38, et transmembrant glykoprotein uttrykt på overflaten av plasmaceller, og induserer apoptose. Det er det eneste legemidlet som er spesifikt godkjent for behandling av AL-amyloidose når det brukes sammen med CyBorD. Effekten av CyBorD-daratumumumab er svært høy, med 78 % av pasientene som oppnår en signifikant hematologisk respons (definert som en komplett respons eller svært god delvis respons). Median overlevelse i den lille gruppen pasienter som fikk CyBorD (n = 15) var 655 dager sammenlignet med 178 dager for pasienter som fikk annen melfalan-deksametason-basert behandling (n = 10).4
Disse terapiene har imidlertid en rekke bivirkninger, inkludert kardiotoksisitet, noe som fører til behov for dosereduksjon eller seponering av behandlingen, og bruk av andre mindre effektive, men mer tolererbare terapeutiske strategier.
Isatuximab, et monoklonalt antistoff mot CD38 som ligner på daratumumab, studeres for behandling av plasmacelledyskrasi som ligger til grunn for AL.
Tre monoklonale antistoffer, birtamimab, CAEL-101 og AT-03, studeres for tiden for fjerning av amyloidfibriller fra syke organer. Resultatene av disse studiene vil kunne gi direkte bevis for hypotesen om at ved å fjerne lettkjededeponerte fibriller fra organer skjer det en forbedring av organfunksjonen. [ 21 ]
For å støtte leverfunksjonen foreskrives legemidler basert på urso-deoksyolsyre (f.eks. Ursosan). Urso-deoksyolsyre bidrar til å stabilisere cellemembraner, reduserer den negative effekten av giftige fettsyrer i gallestase fremkalt av amyloidavleiringer, og bidrar til å gjenopprette normal galleutstrømning.
I tillegg gis symptomatisk behandling og støtte til funksjonen til andre vitale strukturer som nervesystem, hjerte, nyrer osv. Støttende behandling for pasienter med hepatisk amyloidose inkluderer ulike kliniske aspekter, inkludert behandling av hjertesvikt, arytmier, ledningsforstyrrelser, tromboembolisme og samtidig tilstedeværelse av aortastenose.
Andre behandlinger avhenger av typen amyloidose og hvilke deler av kroppen som er berørt. Behandlinger kan omfatte: [ 22 ]
- Legemidler som lindrer symptomer, som smertestillende midler, kvalmemedisiner eller medisiner som reduserer hevelse (vanndrivende midler);
- Medisiner for å redusere amyloid;
- Nyredialyse;
- Levertransplantasjon.
Leveren produserer 95 % av TTR (transthyretin, et protein involvert i tyroksin (T4)-transport og retinolbindende protein. Transthyretin syntetiseres hovedsakelig i leveren og er rikt på beta-tråder som har en tendens til å aggregere til uløselige amyloidfibriller) målt i serum. Derfor har levertransplantasjon historisk sett (siden 1990) blitt foreslått som førstelinjebehandling for å eliminere hovedkilden til amyloidogen TTR hos pasienter med den familiære formen (ATTRv), mens det ikke er indisert i ATTR-wt-formen. Levertransplantasjon av unge pasienter i tidlige stadier av sykdommen er assosiert med en høy 20-års overlevelsesrate. Levertransplantasjon ser ut til å være mer effektiv i noen mutasjoner og mindre effektiv i andre, for eksempel V122I (assosiert med kardiomyopati). Kombinert lever- og hjertetransplantasjon er også mulig hos unge ATTRv-pasienter med kardiomyopati, og litteraturdata om en liten gruppe pasienter tyder på at denne kombinasjonen har en bedre prognose enn hjertetransplantasjon alene.
Pasienter med hepatisk amyloidose er kontraindisert ved bruk av hjerteglykosider og kalsiumantagonister som Diltiazem eller Verapamil, som kan akkumuleres i amyloid. ACE-hemmere og betablokkere brukes med forsiktighet.
Ved ortostatisk hypotensjon foreskrives mineralokortikoider eller glukokortikoider, tatt i betraktning at de kan forårsake dekompensasjon av hjertesvikt. Det alfa-adrenomimetiske legemidlet midodrin (Gutron) brukes også med forsiktighet.
Antikonvulsiva og antidepressiva er passende ved nevropatier.
I noen tilfeller av leveramyloidose må legene vurdere organtransplantasjon.
Forebygging
På grunn av mangel på informasjon om patogenesen til leveramyloidose, kan ikke spesialister utvikle en spesifikk forebygging av sykdommen. Derfor er hovedinnsatsen redusert til rettidig oppdagelse og behandling av eventuelle kroniske patologier som kan provosere frem utviklingen av lidelsen. Hvis det er tilfeller av amyloidose av en hvilken som helst lokalisering i familien, anbefales det å systematisk oppsøke leger for dispensærundersøkelser.
Generelt sett er forebyggende tiltak redusert til rettidig eliminering av smittsomme sykdommer, spesielt de som har en tendens til å utvikle seg til en kronisk prosess. Det handler om å forhindre utvikling av tuberkulose, lungeinfeksjoner, etc. Det er viktig med rettidig oppdagelse og tilstrekkelig behandling av streptokokkinfeksjoner, som kan bli årsaken til kroniske former for autoimmune inflammatoriske prosesser. Vi snakker om scarlatina, streptokokkbetennelse i mandlene, etc.
Hvis pasienten allerede har en autoimmun sykdom, bør han systematisk konsultere en lege, observere patologiens aktivitet, bruke nødvendige medisiner som foreskrevet av legen, justere doseringer i henhold til indikasjoner.
Prognose
Prognosen for pasienter med hepatisk amyloidose er ugunstig. Sykdommen forverres sakte, men kontinuerlig, noe som til slutt forårsaker dysfunksjon i de berørte organene og dødelig utgang – spesielt på grunn av organsvikt.
Pasienter med systemisk patologi dør hovedsakelig som følge av utviklingen av kronisk nyresvikt, selv om hemodialyse eller kontinuerlig ambulerende peritonealdialyse i noen tilfeller forbedrer prognosen for slike pasienter. Overlevelsesraten for pasienter på hemodialyse, uavhengig av type, kan sammenlignes med overlevelsesraten for personer med andre systemiske patologier og diabetes mellitus.
Hovedårsaken til død under hemodialyse er utvikling av komplikasjoner fra det kardiovaskulære systemet.
Levertransplantasjon har lenge vært ansett som en av de viktigste behandlingsmetodene for sykdommen, og de mest optimistiske overlevelsesratene observeres hos pasienter som ikke overstiger 50 år (forutsatt at den patologiske prosessen er kortvarig og kroppsmasseindeksen er normal). Pasienter med leveramyloidose kombinert med perifer nevropati har en noe dårligere prognose.

