Medisinsk ekspert av artikkelen
Nye publikasjoner
Restenose
Sist anmeldt: 04.07.2025

Alt iLive-innhold blir gjennomgått med medisin eller faktisk kontrollert for å sikre så mye faktuell nøyaktighet som mulig.
Vi har strenge retningslinjer for innkjøp og kun kobling til anerkjente medieområder, akademiske forskningsinstitusjoner og, når det er mulig, medisinsk peer-evaluerte studier. Merk at tallene i parenteser ([1], [2], etc.) er klikkbare koblinger til disse studiene.
Hvis du føler at noe av innholdet vårt er unøyaktig, utdatert eller ellers tvilsomt, velg det og trykk Ctrl + Enter.
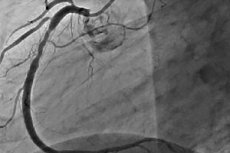
Restenose er utviklingen av en tilbakevendende innsnevring på 50 % eller mer på stedet for perkutan koronarintervensjon. Restenose er vanligvis ledsaget av tilbakevendende angina, som ofte krever gjentatte intervensjoner. Etter hvert som PCI har utviklet seg, har forekomsten av restenose sunket, og dens natur har også endret seg.
Restenose etter transluminal ballongkoronarangioplastikk (TBCA)
Etter TBCA er restenoseraten i løpet av de første 6 månedene 30–40 %. Hovedmekanismen for utviklingen er lokal negativ ombygging av karet, som i hovedsak er en elastisk kollaps av arterielumen, utvidet av ballongen under prosedyren. Lokal trombedannelse og neointimal vekst spiller også en relativ rolle. Det finnes kliniske (type 2 diabetes mellitus, akutt koronarsyndrom (ACS), historie med restenose), angiografiske (LAD-lesjon, liten kardiameter, kronisk total okklusjon (CTO), lang lesjon, degenererte venøse bypass-transplantater) og prosedyremessige (stor reststenose, liten økning i kardiameter som følge av ballongoppblåsing) risikofaktorer for restenose etter TBCA. Ved restenose utføres vanligvis en gjentatt intervensjon. Suksessen med gjentatt TBCA på restenosestedet er sammenlignbar med den første prosedyren. Imidlertid øker risikoen for tilbakevendende restenose betydelig med hver påfølgende TBCA for restenose. Etter det tredje forsøket når den 50–53 %. I tillegg er den utviklende restenose mer uttalt enn den første ved hver gjentatte TBCA. Risikofaktorer for restenose etter den andre TBCA er tidlig forekomst av den første restenose (60–90 dager etter prosedyren), LAD-skade, skade på flere kar, diabetes mellitus type 2, arteriell hypertensjon, ustabil angina og flere ballongoppblåsninger under den første prosedyren. Gitt den høye hyppigheten av restenose og mekanismen for dens utvikling, ble koronarstenter introdusert i klinisk praksis, noe som teoretisk sett burde ha eliminert negativ karremodellering etter TBCA.
De første studiene som demonstrerte effekten av stenting var STRESS- og BENESTENT-studiene publisert i 1993. BENESTENT inkluderte 516 pasienter med nydiagnostisert stenose i koronararterier større enn 3 mm i diameter, som ble randomisert til to grupper: konvensjonell TBCA (n = 257) og TBCA med stentplassering (n = 259). Etter 3 år var restenoseraten under angiografi 32 % i den konvensjonelle TBCA-gruppen og 22 % i stentgruppen. Den relative reduksjonen i restenoseraten var 31 % (p < 0,01). Stentgruppen hadde også et lavere behov for gjentatt myokardrevaskularisering (10 vs. 20,6 % i den konvensjonelle TBCA-gruppen; p < 0,01), noe som var assosiert med en lavere rate av angina-residiv i stentgruppen.
I følge STRESS-studien (n = 407) var restenoseraten også lavere i stentgruppen (n ~ 205) enn i den konvensjonelle PTCA-gruppen (n = 202) - 31,6 vs. 42,1 % (p < 0,01). Fordelen med å bruke stenter fremfor konvensjonell angioplastikk ved restenose på PTCA-stedet ble demonstrert i REST-studien, hvor 383 pasienter med restenose ble randomisert til stenting eller gjentatt perkutan transluminal koronarangioplastikk. Angiografisk påvist gjentatt restenose var 18 % lavere i stentgruppen (18 vs. 5,32 %; p < 0,03). Gjentatt myokardrevaskularisering, som er en indikator på klinisk signifikant restenose, var også nødvendig betydelig sjeldnere i gruppen pasienter som gjennomgikk stenting (10 vs. 27 %; p < 0,001). Dermed ble det vist bedre resultater med bruk av stenting ikke bare i native arterier, men også i tilfelle intervensjon for restenose som utviklet seg etter TBCA.
Restenose etter implantasjon av bar stent (BSI)
Selv om udekkede koronarstenter har redusert forekomsten av restenose med 30–40 % sammenlignet med TBCA, utvikler 17–32 % av pasientene restenose i stenten selv etter stenting, noe som krever gjentatt revaskularisering. Mekanismen for utvikling av stentstenose (ISS) er forskjellig fra den ved TBCA. Etter stenting er hovedbidraget til restenose dannelse av neointima, snarere enn negativ ombygging, som ved TBCA, som praktisk talt er fraværende på stentimplantasjonsstedet. Neointima dannes ved migrasjon og proliferasjon av glatte muskelceller som produserer ekstracellulær matriks, som sammen med celler utgjør neointima. I tillegg er trombepersistens på stentstedet også viktig hos pasienter med diabetes.
Hovedklassifiseringen av stentstenose (ISS) er klassifiseringen foreslått av Mehran, som inkluderer fire typer avhengig av omfanget og alvorlighetsgraden av lesjonen: I type ISS - lokal (< 10 mm i lengde), II type - diffus (> 10 mm i lengde), III type - proliferativ (> 10 mm og strekker seg utover stenten) og IV type - ISS som fører til okklusjon. Den første typen er delt inn i undertyper avhengig av plasseringen i stenten: 1a - på bøyen eller mellom stenter, 1b - marginal, 1c - inne i stenten, 1d - multifokal.
Risikofaktorer for utvikling av VRS er inngrep på venøse bypass-transplantater, kroniske okklusjoner, ostiale lesjoner, liten kardiameter, forekomst av reststenose, stenting for VRS, liten kardiameter etter prosedyren, LAD-lesjon, lang stentlengde, forekomst av diabetes, implantasjon av flere stenter i én lesjon. Det finnes indikasjoner på påvirkning av genetiske faktorer, spesielt polymorfisme av glykoprotein IIIa-genet og mutasjoner av metylentetrahydrofolatreduktasegenet - genet som koder for interleukin-1. Ved utvikling av marginal stentrestenose er den viktigste risikofaktoren en uttalt aterosklerotisk lesjon i det stenterte segmentet.
Restenose forekommer hovedsakelig i løpet av de første 6–8 månedene etter perkutan koronar intervensjon. De fleste pasienter utvikler kliniske symptomer omtrent samtidig. VRS manifesterer seg vanligvis ved tilbakevendende angina. Ustabil angina forekommer sjeldnere (11–41 % av tilfellene). AMI utvikles hos 1–6 % av pasientene. Dermed er den vanligste årsaken til angina i perioden 1–6 måneder etter stenting utviklingen av VRS, som som regel krever gjentatt revaskularisering. Det finnes flere metoder for behandling av VRS. Konvensjonell TBCA kan utføres, noe som fører til ytterligere stentekspansjon (56 % bidrag til den endelige økningen i kardiameter) og skyver neointima gjennom stentcellene (44 % bidrag til den endelige økningen i diameter). Imidlertid observeres gjenværende restenose i de fleste tilfeller på intervensjonsstedet (i gjennomsnitt 18 %). I tillegg er gjentatt revaskularisering nødvendig etter TBCA i 11 % av tilfellene, oftere hos pasienter med multikarsykdom, lav LVEF, ved intervensjoner på venøse bypass-transplantater eller tidlig forekomst av den første VRS. Risikoen for å utvikle gjentatt VRS etter TBCA avhenger også av lesjonstypen og varierer fra 10 % ved lokal restenose til 80 % ved okklusjon i stenten. Implantasjon av LES på stedet for VRS reduserer ikke risikoen for tilbakefall sammenlignet med TBCA alene.
Den andre metoden for behandling av VRS er brachyterapi, som innebærer å introdusere en radioaktiv kilde i lumen i koronararterien, noe som forhindrer spredning av glatte muskelceller og dermed reduserer risikoen for restenose. Imidlertid har den høye kostnaden for utstyr, prosedyrens tekniske kompleksitet og den økte forekomsten av sen stenttrombose (LT) nesten fullstendig utelukket brachyterapi fra klinisk bruk.
Et revolusjonerende øyeblikk i behandlingen av VRS var introduksjonen av medikamentavgivende stenter. Sammenlignet med LES i native arterier reduserer de risikoen for VRS med 70–80 %. De første dataene om effektiviteten til DES hos pasienter med allerede utviklet VRS ble innhentet i TAXUS III-pasientregisteret, der hyppigheten av VRS-tilbakefall bare var 16 % etter 6 måneder ved bruk av SPG1 hos slike pasienter, noe som er lavere enn i de tidligere nevnte studiene med TBCA. I TRUE-registeret, som inkluderte pasienter etter SES-implantasjon for LES-restenose, var gjentatt revaskularisering nødvendig etter 9 måneder hos mindre enn 5 % av pasientene, hovedsakelig med diabetes mellitus og ACS. TROPICAL-studien sammenlignet hyppigheten av gjentatt restenose hos pasienter etter DES-implantasjon på restenosestedet med dataene fra GAMMA I- og GAMMA II-studiene, der brachyterapi ble brukt som behandlingsmetode. Etter 6 måneder var forekomsten av tilbakevendende restenose signifikant lavere i SPS-gruppen (9,7 vs 40,3 %; p < 0,0001). Det er viktig å merke seg at forekomsten av stenttrombose og hjerteinfarkt også var lavere i SPS-gruppen (TS 0,6 vs 3,9 %; p = 0,08; MI - 1,8 vs 9,4 %; p = 0,004). Fordelen med SPS fremfor brachyterapi ble bekreftet i den randomiserte SISR-studien, der 384 pasienter med utviklet VRS i NSC ble randomisert til brachyterapi- eller SPS-implantasjonsgrupper. Etter 9 måneder var behovet for gjentatt revaskularisering høyere etter brachyterapi (19,2 %) enn i SPS-implantasjonsgruppen (8,5 %), noe som reflekterte en hyppigere tilbakefall av restenose. Etter 3 år var fordelen med SPS med tanke på å redusere behovet for gjentatt revaskularisering på grunn av tilbakevendende stentrestenose fortsatt til stede (19 vs 28,4 %). Det var ingen signifikant forskjell i forekomsten av trombose mellom gruppene.
Hovedfaktorene for utvikling av tilbakevendende VRS hos pasienter med LES ved SPS-implantasjon er liten kardiameter (< 2,5 mm), diffus restenose og tilstedeværelse av kronisk nyresvikt som krever hemodialyse. I den randomiserte studien TAXUS V ISR viste SPS også høy effektivitet i behandlingen av VRS, og reduserte forekomsten av tilbakevendende restenose med 54 % sammenlignet med brachyterapi.
Det ble også utført randomiserte studier som sammenlignet effekten av TBCA for VRS- og DES-implantasjon. I den randomiserte RIBS-II-studien var gjentatt restenose 72 % mindre vanlig etter 9 måneder etter DES-implantasjon enn etter TBCA, noe som reduserte behovet for gjentatt revaskularisering fra 30 til 11 %. ISAR DESIRE-studien sammenlignet effekten av TBCA for VRS med SPP- eller SPS-implantasjon. Etter 6 måneder viste det seg at begge DES-ene var mer effektive i å forhindre gjentatt restenose enn TBCA (forekomsten var 44,6 % med TBCA, 14,3 % i SPS-gruppen og 21,7 % i SPS-gruppen), noe som reduserte behovet for gjentatt revaskularisering. I en direkte sammenligning av SPP og SPS ble det funnet at SPS reduserte behovet for gjentatt revaskularisering betydelig mer effektivt enn SPP (8 vs. 19 %). DES-implantasjon reduserer dermed forekomsten av tilbakevendende LES VRS sammenlignet med både TBCA og brachyterapi, noe som reduserer antall gjentatte PCI-er og derfor gjør implantasjon av disse til den foretrukne prosedyren hos slike pasienter.
Restenose etter implantasjon av medikamentavgivende stent (DES)
Til tross for en reduksjon på 70–80 % i forekomsten av stenose i stenten ved bruk av DES sammenlignet med LES, kunne de ikke helt utelukke utviklingen av denne iatrogene konsekvensen av stenting. Den totale forekomsten er i gjennomsnitt fortsatt mindre enn 10 %. I tillegg til den kvantitative reduksjonen i forekomsten av restenose, endret de også typen restenose som oppstår betydelig. Etter DES-implantasjon er restenose derfor vanligvis fokal. Klinisk, som ved LES, manifesterer det seg oftest som et tilbakefall av stabil angina (77 %), sjeldnere (8 %) er det asymptomatisk. I 5 % av tilfellene manifesterer det seg som ustabil angina, og hos 10 % er det første symptomet ikke-Q-bølge hjerteinfarkt. Hovedfaktorene i utviklingen av DES-restenose er diabetes mellitus type 2, liten kardiameter og omfanget av lesjonen. Det finnes ingen klare anbefalinger for behandling av slike pasienter. Alternative alternativer er reimplantasjon av en DES (av samme type eller en annen), TBCA eller brachyterapi. Gjennomsnittlig rate av re-restenose med en andre DES er 24 %, og det er det samme enten samme type DES implanteres eller en annen.


 [
[