Nye publikasjoner
Forskere oppdager ny immunsuppressiv mekanisme i hjernekreft
Sist anmeldt: 02.07.2025

Alt iLive-innhold blir gjennomgått med medisin eller faktisk kontrollert for å sikre så mye faktuell nøyaktighet som mulig.
Vi har strenge retningslinjer for innkjøp og kun kobling til anerkjente medieområder, akademiske forskningsinstitusjoner og, når det er mulig, medisinsk peer-evaluerte studier. Merk at tallene i parenteser ([1], [2], etc.) er klikkbare koblinger til disse studiene.
Hvis du føler at noe av innholdet vårt er unøyaktig, utdatert eller ellers tvilsomt, velg det og trykk Ctrl + Enter.
Førsteamanuensis Filippo Veglia, Ph.D., og teamet hans ved Wistar-instituttet har oppdaget en nøkkelmekanisme der glioblastom – en alvorlig og ofte dødelig hjernekreft – undertrykker immunforsvaret slik at svulsten kan vokse uforstyrret av kroppens forsvar.
Oppdagelsen deres ble publisert i artikkelen «Glukosedrevet histonlaktylering promoterer den immunsuppressive aktiviteten til monocyttavledede makrofager i glioblastom» i tidsskriftet Immunity.
«Studien vår viser at kreftens selvopprettholdelsesmekanismer, hvis de er tilstrekkelig forstått, kan utnyttes mot sykdommen svært effektivt», sa Dr. Veglia.
«Jeg ser frem til fremtidige studier av metabolismemedierte immunsuppresjonsmekanismer ved glioblastom, og håper at vi vil fortsette å lære mer om hvordan vi bedre kan forstå og bekjempe denne kreften.»
Frem til nå har det blitt lite studert hvordan monocytt-avledede makrofager og mikroglia skaper et immunsuppressivt tumormikromiljø i glioblastom.
Veglia-laboratoriet undersøkte de cellulære mekanismene for immunsuppresjon ved glioblastom og fant at etter hvert som glioblastom utvikler seg, begynner monocytt-avledede makrofager å overgå mikroglia, noe som tyder på at overvekten av monocytt-avledede makrofager i tumormikromiljøet er gunstig for kreft når det gjelder immununngåelse.
Monocyttavledede makrofager, men ikke mikroglia, blokkerte faktisk aktiviteten til T-celler (immunceller som dreper tumorceller) i prekliniske modeller og hos pasienter. Teamet bekreftet dette ved å evaluere prekliniske glioblastommodeller med kunstig redusert antall monocyttavledede makrofager.
Som forventet viste modeller med færre ondartede makrofager i tumormikromiljøet forbedrede resultater sammenlignet med standard glioblastommodeller.
Glioblastom står for litt over halvparten av alle ondartede svulster som oppstår i hjernen, og prognosen for pasienter som får diagnosen er ekstremt dårlig: bare 25 % av pasientene overlever det første året etter diagnosen. Glioblastom er farlig ikke bare på grunn av plasseringen i hjernen, men også på grunn av det immunsuppressive svulstmikromiljøet, noe som gjør glioblastom resistent mot lovende immunterapier.
Ved å programmere visse immunceller, som makrofager (monocytt-avledede makrofager og mikroglia), til å arbeide for svulsten snarere enn mot den, skaper glioblastom et svulstmikromiljø for seg selv som lar kreften vokse aggressivt samtidig som den unngår immunresponser mot kreft.
Avklaring av mekanismen
Etter å ha bekreftet rollen til monocytt-avledede makrofager, forsøkte Weglias laboratorium å forstå nøyaktig hvordan disse kreftassosierte immuncellene virker mot immunsystemet.
De sekvenserte makrofagene for å avgjøre om cellene hadde noen unormale genuttrykksmønstre som kunne indikere gener som spiller en rolle i immunsuppresjon, og de undersøkte også makrofagenes metabolske mønstre for å se om det unormale genuttrykket var relatert til metabolisme.
Gen- og metabolsk analyse ledet dem til glukosemetabolismen. En serie tester viste at monocyttavledede makrofager med økt glukosemetabolisme og uttrykk av GLUT1, hovedtransportøren for glukose, blokkerte T-cellefunksjonen ved å frigjøre interleukin-10 (IL-10).
Teamet viste at glioblastom forstyrrer glukosemetabolismen i disse makrofagene, noe som forårsaker deres immunsuppressive aktivitet.
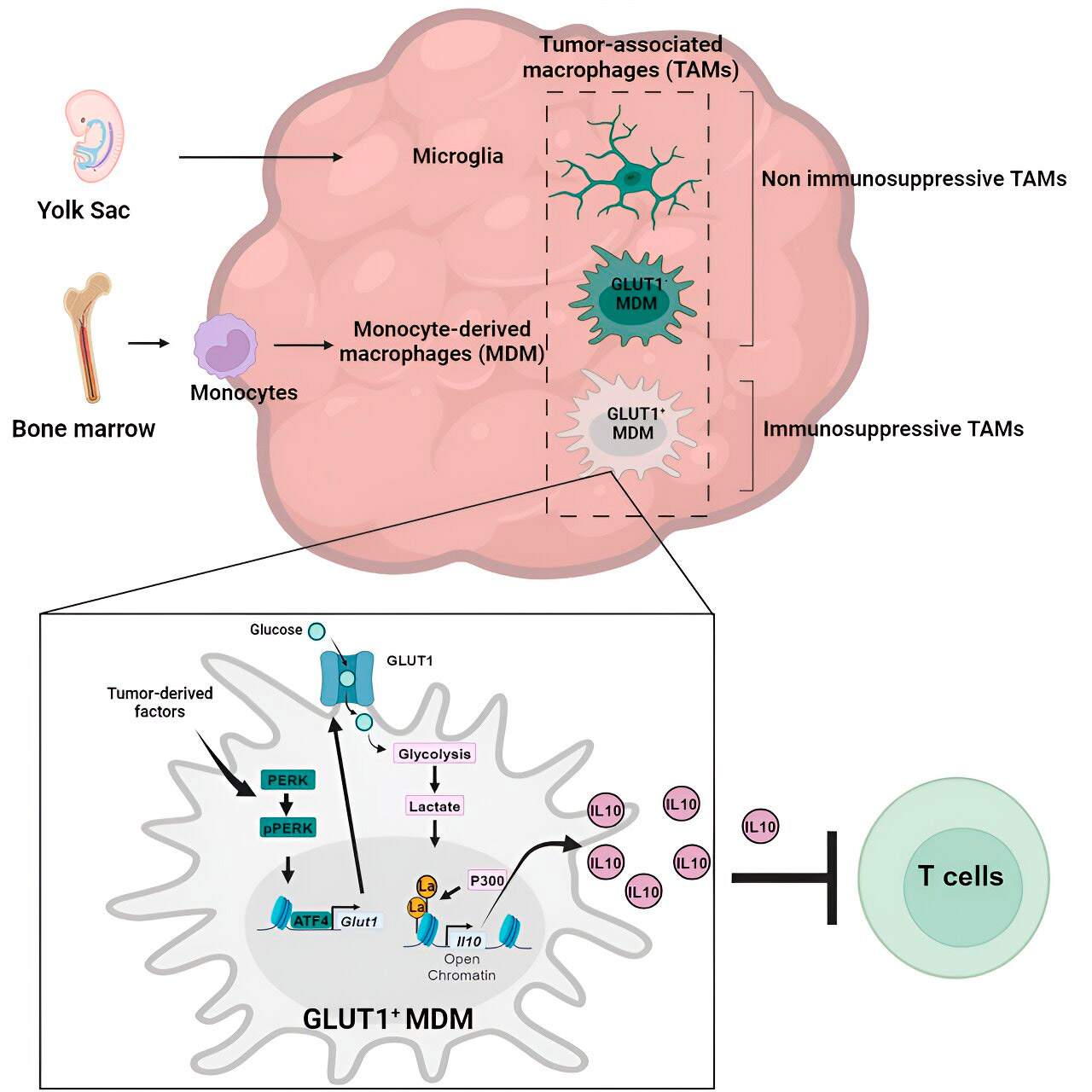
Histonlaktylering og dens rolle
Forskerne fant at nøkkelen til den glukosemetabolismerelaterte immunsuppressive aktiviteten til monocytt-avledede makrofager ligger i en prosess som kalles "histonlaktylering." Histoner er strukturelle proteiner i genomet som spiller en nøkkelrolle i uttrykket av gener som IL-10 i visse sammenhenger.
Ved å metabolisere glukose raskt produserer monocytt-avledede makrofager laktat, et biprodukt av glukosemetabolismen. Histoner kan bli "laktylerte" (dvs. laktat integreres i histonene) på en slik måte at histonorganiseringen fremmer uttrykket av IL-10, som produseres av monocytt-avledede makrofager for å støtte kreftcellevekst.
Løsning på problemet
Men hvordan kan den immunsuppressive aktiviteten til monocytt-avledede makrofager assosiert med glukosemetabolisme stoppes? Dr. Veglia og teamet hans identifiserte en mulig løsning: PERK, et enzym de identifiserte som en regulator av glukosemetabolisme og GLUT1-ekspresjon i makrofager.
I prekliniske modeller av glioblastom svekket målretting mot PERK histonlaktylering og makrofagimmunsuppressiv aktivitet, og når det kombineres med immunterapi, blokkerte det glioblastomprogresjon og induserte langsiktig immunitet som beskyttet hjernen mot tumorvekst. Dette tyder på at det å målrette PERK-histonlaktyleringsaksen kan være en levedyktig strategi for å bekjempe denne dødelige hjernekreften.
