Nye publikasjoner
FDA godkjenner Bimzelx for behandling av hidradenitt
Sist anmeldt: 02.07.2025

Alt iLive-innhold blir gjennomgått med medisin eller faktisk kontrollert for å sikre så mye faktuell nøyaktighet som mulig.
Vi har strenge retningslinjer for innkjøp og kun kobling til anerkjente medieområder, akademiske forskningsinstitusjoner og, når det er mulig, medisinsk peer-evaluerte studier. Merk at tallene i parenteser ([1], [2], etc.) er klikkbare koblinger til disse studiene.
Hvis du føler at noe av innholdet vårt er unøyaktig, utdatert eller ellers tvilsomt, velg det og trykk Ctrl + Enter.
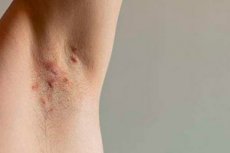
Det amerikanske mat- og legemiddeltilsynet (FDA) har godkjent UCBs Bimzelx (bimekizumab-bkzx) for behandling av voksne med moderat til alvorlig hidradenitt suppurativa.
Bimzelx er det første og eneste godkjente legemidlet som selektivt hemmer interleukin 17F (IL-17F) i tillegg til interleukin 17A (IL-17A). Dette er den femte indikasjonen for Bimzelx i USA.
Grunnlag for godkjenning:
Godkjenningen er basert på data fra to kliniske fase III-studier (BE HEARD I og BE HEARD II) utført på voksne pasienter med moderat til alvorlig hidradenitt suppurativa.
Nøkkelindikator for ytelse:
- HiSCR50: Ved uke 16 oppnådde en betydelig større andel av pasientene behandlet med Bimzelx ≥50 % forbedring i tegn og symptomer på hidradenitis suppurativa (målt ved Hidradenitis Suppurativa Clinical Response (HiSCR50)-skåre) sammenlignet med placebo.
Sekundærindikator:
- HiSCR75: Legemidlet ga også klinisk meningsfulle forbedringer hos pasienter som oppnådde ≥75 % forbedring (HiSCR75) ved uke 16, sammenlignet med placebo.
Bærekraft av resultater:
- Kliniske responser ble opprettholdt til uke 48, uten nye sikkerhetssignaler identifisert.
Ekspertuttalelse:
Dr. Alexa B. Kimball, BE HEARD-programforsker og hudlege ved Beth Israel Deaconess Medical Center i Boston, sa:
«Godkjenningen av Bimzelx for behandling av moderat til alvorlig hidradenitt suppurativa er en viktig utvikling gitt det betydelige udekkede kliniske behovet og det begrensede antallet behandlingsalternativer som er tilgjengelige i dag.»
