Nye publikasjoner
Hvorfor fotoreseptorcelleoverlevelse ikke når 100 %: Viktige mekanismer belyst
Sist anmeldt: 09.08.2025

Alt iLive-innhold blir gjennomgått med medisin eller faktisk kontrollert for å sikre så mye faktuell nøyaktighet som mulig.
Vi har strenge retningslinjer for innkjøp og kun kobling til anerkjente medieområder, akademiske forskningsinstitusjoner og, når det er mulig, medisinsk peer-evaluerte studier. Merk at tallene i parenteser ([1], [2], etc.) er klikkbare koblinger til disse studiene.
Hvis du føler at noe av innholdet vårt er unøyaktig, utdatert eller ellers tvilsomt, velg det og trykk Ctrl + Enter.
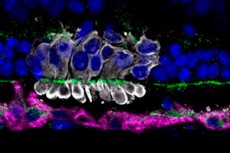
Forskere fra University of Pennsylvania, ledet av Raghavi Sudharsan, har oppdaget hvorfor omtrent 70 % av transplanterte fotosensoriske progenitorceller (PRPC-er) fra induserte pluripotente stamceller dør i løpet av de første dagene etter transplantasjon inn i netthinnen. Arbeidet deres, publisert i Stem Cell Research & Therapy, peker på metabolsk stress i donorceller som hovedårsaken til det tidlige tapet.
Forutsetninger
Transplantasjon av PRPC-er anses som en lovende metode for progressive degenerative sykdommer i netthinnen (retinitis pigmentosa, makuladegenerasjon). Den lave overlevelsesraten for donorceller begrenser imidlertid effektiviteten av behandlingen. Frem til nå har hovedfokuset vært å undertrykke immunresponsen, men selv med omfattende immunsuppresjon forble tapene katastrofale.
Design og metoder
Modeller:
Friske hunder og retinitis pigmentosa-modellhunder fikk subretinale injeksjoner av fluorescensmerkede PRPC-er.
Overlevelsesestimat:
Fluoresceinangiografi og optisk koherenstomografi (OCT) registrerte volumet av transplanterte celler på den første dagen, på den tredje og på den syvende dagen.
Enkeltcelletranskriptomikk (scRNA-sekvensering):
PRPC-er ble isolert fra netthinneområder på dag 3, og uttrykket av gener relatert til metabolisme og apoptose ble analysert.
Immunhistokjemi:
Oksidative stressmarkører (4-HNE), mitokondriell status (Tom20) og mikroglialaktivering (Iba1) ble vurdert i transplantasjonsområdet.
Viktige resultater
- Massivt celletap: omtrent 70 % av PRPC-ene forsvant innen dag 7 i både friske og degenererende netthinner til tross for immunsuppresjon.
- Metabolsk stress: scRNA-seq viste en dramatisk reduksjon i uttrykket av oksidative fosforyleringsgener (CYCS, COX4I1) og en økning i transkripsjonen av apoptotiske markører (BAX, CASP3).
- Mitokondriell dysfunksjon: Immunhistokjemi viste fragmentering og tap av Tom20-merking i transplanterte PRPC-er, og forhøyede 4-HNE-nivåer indikerte oksidativ skade.
- Mikroglias rolle: I transplantasjonsområdet økte Iba1⁺ mikrogliacelleaktiviteten som respons på PRPC-død, noe som kan forverre lokal betennelse og bidra til ytterligere tap.
Implikasjoner for celleterapier
Disse funnene endrer paradigmet: for å øke innpodingen av PRPC-er er det ikke bare nødvendig å undertrykke immunresponsen, men også å støtte energimetabolismen til donorceller. Mulige intervensjoner:
- Foreløpig "metabolsk fortrening" av PRPC-er under normale kulturforhold på kanten av substressbelastning for å forbedre deres mitokondrielle robusthet.
- Cocktailer av mitokondrielle stabilisatorer (koenzym Q₁₀, karnitin) under og umiddelbart etter transplantasjon.
- Modulering av det lokale netthinnemikromiljøet: tilførsel av antioksidanter eller mitokondrielle beskyttere til transplantasjonsområdet.
Praktiske konklusjoner og utsikter
- Metabolsk forkondisjonering: kondisjonering av PRPC-er under milde metabolske stressforhold før transplantasjon for å forbedre deres motstandskraft.
- Stillaslevering: bruk av biologisk nedbrytbare matriser som sikrer gradvis overgang av donorceller fra et rikt kulturmedium til netthinnemiljøet.
- Ernæringsstøtte: tilførsel av antioksidanter eller mitokondrielle respirasjonssubstrater i forbindelse med PRPC-er.
«Vi har lenge bare kjempet mot immunforsvaret, men nå er det klart at uten å løse problemet med metabolsk sjokk, er transplantasjoner dømt til tidlig død», konkluderer Raghavi Sudharsan.
Arbeidet, støttet av National Eye Institute, baner vei for mer levedyktige celleterapier for å gjenopprette synet hos pasienter med degenerative netthinnesykdommer.
